Субъединица C АТФ-синтазы - ATP synthase subunit C
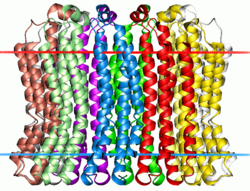 V-образный натрий АТФаза от Enterococcus hirae. Расчетные углеводородные границы липидный бислой показаны красными и синими точками | |||||||||
| Идентификаторы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Символ | ATP-synt_C | ||||||||
| Pfam | PF00137 | ||||||||
| ИнтерПро | IPR002379 | ||||||||
| PROSITE | PDOC00526 | ||||||||
| SCOP2 | 1aty / Объем / СУПФАМ | ||||||||
| OPM суперсемейство | 5 | ||||||||
| Белок OPM | 2bl2 | ||||||||
| |||||||||
АТФаза, субъединица C комплекса Fo / Vo является основной трансмембранной субъединицей V-типа, A-типа и F-типа АТФ-синтазы. Субъединица C (также называется субъединица 9, или протеолипид в F-АТФазах или Протеолипид 16 кДа in V-ATPases) был обнаружен в Fo или Vo комплексе F- и V-ATPases соответственно. Субъединицы образуют олигомерный c кольцо которые составляют ротор Fo / Vo / Ao, где фактическое количество субъединиц сильно варьируется среди конкретных ферментов.[1]
АТФазы (или АТФ-синтазы) представляют собой мембраносвязанные комплексы ферментов / переносчиков ионов, которые сочетают синтез и / или гидролиз АТФ с переносом протонов через мембрану. АТФазы могут использовать энергию протонного градиента, используя поток ионов через мембрану через протонный канал АТФазы, чтобы управлять синтезом АТФ. Некоторые АТФазы работают в обратном направлении, используя энергию гидролиза АТФ для создания протонного градиента. Существуют различные типы АТФаз, которые различаются по функции (синтез и / или гидролиз АТФ), структуре (F-, V- и A-АТФазы содержат вращающиеся двигатели) и по типу переносимых ими ионов.[2][3]
Каждая из F-ATPases (или F1Fo ATPases) и V-ATPases (или V1Vo ATPases) состоит из двух связанных комплексов: комплекс F1 или V1 содержит каталитическое ядро, которое синтезирует / гидролизует ATP, и комплекс Fo или Vo, который образует мембранные поры. Все F- и V-АТФазы содержат роторные двигатели, один из которых управляет перемещением протонов через мембрану, а другой - синтез / гидролиз АТФ.[4][5]
В F-ATPases поток протонов через канал ATPase управляет вращением кольца C-субъединицы, которое, в свою очередь, связано с вращением ротора комплексной гамма-субъединицы F1 из-за постоянного связывания между гамма- и эпсилон-субъединицами F1. и кольцо субъединицы C Fo. Последовательное протонирование и депротонирование Asp61 субъединицы C связано со ступенчатым движением ротора.[6]
В V-АТФазах есть три протеолипидные субъединицы (c, c 'и c' '), которые образуют часть протонпроводящей поры, каждая из которых содержит скрытый остаток глутаминовой кислоты, который важен для транспорта протонов.[7][8]
В недавнем исследовании c-субъединица была указана как критический компонент поры перехода проницаемости митохондрий.[9]
Подсемейства
- АТФаза, комплекс Vo, протеолипидная субъединица C, ИнтерПро: IPR000245
- АТФаза, комплекс Fo, субъединица C ИнтерПро: IPR000454
Белки человека, содержащие этот домен
ATP5G1; ATP5G2; ATP5G3; ATP6V0B; ATP6V0C;
Смотрите также
использованная литература
- ^ Кюльбрандт В., Дэвис К.М. (январь 2016 г.). «Роторные АТФазы: новый поворот к древней машине». Тенденции в биохимических науках. 41 (1): 106–116. Дои:10.1016 / j.tibs.2015.10.006. PMID 26671611.
- ^ Мюллер В., Кросс Р.Л. (2004). «Эволюция АТФ-синтаз и АТФаз A-, F- и V-типа: реверсирование функции и изменения соотношения сочетания H + / ATP». FEBS Lett. 576 (1): 1–4. Дои:10.1016 / j.febslet.2004.08.065. PMID 15473999. S2CID 25800744.
- ^ Чжан X, Нива Х, Раппас М (2004). «Механизмы АТФаз - мультидисциплинарный подход». Curr Protein Pept Sci. 5 (2): 89–105. Дои:10.2174/1389203043486874. PMID 15078220.
- ^ Ито Х, Йошида М, Ясуда Р., Нодзи Х, Киносита К. (2001). «Разрешение различных подшагов вращения с помощью субмиллисекундного кинетического анализа F1-АТФазы». Природа. 410 (6831): 898–904. Bibcode:2001Натура.410..898л. Дои:10.1038/35073513. PMID 11309608. S2CID 3274681.
- ^ Вилкенс С., Чжэн И, Чжан З (2005). «Структурная модель вакуолярной АТФазы из просвечивающей электронной микроскопии». Микрон. 36 (2): 109–126. Дои:10.1016 / j.micron.2004.10.002. PMID 15629643.
- ^ Fillingame RH, Анжевин CM, Дмитриев OY (2003). «Механика сопряжения протонных движений с вращением с-кольца в АТФ-синтазе». FEBS Lett. 555 (1): 29–34. Дои:10.1016 / S0014-5793 (03) 01101-3. PMID 14630314. S2CID 38896804.
- ^ Иноуэ Т., Форгак М. (2005). «Опосредованное цистеином перекрестное связывание указывает на то, что субъединица C V-АТФазы находится в непосредственной близости к субъединицам E и G домена V1 и субъединице a домена V0». J. Biol. Chem. 280 (30): 27896–27903. Дои:10.1074 / jbc.M504890200. PMID 15951435.
- ^ Джонс Р., Финдли Дж. Б., Харрисон М., Дуроз Л., Сонг С. Ф., Барратт Е., Триник Дж. (2003). «Структура и функция вакуолярной H + -АТФазы: переход от моделей с низким разрешением к структурам с высоким разрешением». J. Bioenerg. Биомер. 35 (4): 337–345. Дои:10.1023 / А: 1025728915565. PMID 14635779. S2CID 43788207.
- ^ Бонора, М; Бонони, А; Де Марчи, E; Георгий, C; Лебедзинская, М; Марчи, S; Патергнани, S; Римесси, А; Suski, JM; Войтала, А; Вецковски, MR; Kroemer, G; Галлуцци, L; Пинтон, П. (15 февраля 2013 г.). «Роль c-субъединицы FO-АТФ-синтазы в переходе митохондриальной проницаемости». Клеточный цикл. 12 (4): 674–83. Дои:10.4161 / cc.23599. ЧВК 3594268. PMID 23343770.
