Анабасеин - Anabaseine - Wikipedia
 | |
| Имена | |
|---|---|
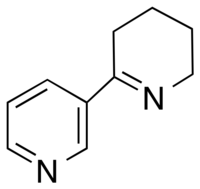
| Другие имена 3,4,5,6-тетрагидро-2,3'-бипиридин | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C10ЧАС12N2 | |
| Молярная масса | 160.220 г · моль−1 |
| Внешность | Масло |
| Запах | Без запаха |
| Точка кипения | 110-120℃ |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Анабасеин (3,4,5,6-Тетрагидро-2,3’-бипиридин) представляет собой алкалоид токсин произведено Немертинцы и Афаногастер муравьи.[1] Конструктивно похож на никотин и анабазин.[2] Точно так же было показано, что он действует как агонист на большинстве никотиновые рецепторы ацетилхолина в Центральная нервная система и периферическая нервная система.[2]
Механизм действия
В иминий Форма анабазеина связывается с большинством никотиновых рецепторов ацетилхолина как в периферической нервной системе, так и в центральной нервной системе. Но есть более высокая аффинность связывания рецепторов в мозге с субъединицей α7, а также рецепторов скелетных мышц.[3] Связывание вызывает деполяризация нейронов, и вызывает высвобождение обоих дофамин и норэпинефрин.[2]
Биологические эффекты
Анабасеин вызывает паралич у ракообразные и насекомые, но не в позвоночные, предположительно, действуя как агонист на периферические нервно-мышечные никотиновые рецепторы ацетилхолина.[2]
Структура
Молекула анабазеина состоит из не-ароматный тетрагидропиридиновое кольцо, связанное с 3-м атомом углерода 3-пиридил звенеть. Он может существовать в трех формах при физиологическом pH: кетон, я добываю, или же иминий структура.[2] Из-за конъюгации между иминным и 3-пиридильным кольцом анабазеин существует в виде почти компланарной молекулы.

Синтез
Спат и Мамоли впервые синтезировали анабазеин в 1936 году.[4] Исследователи отреагировали бензойный ангидрид с δ-валеролактам уступить N-бензоилпиперидон. Потом, N-бензоилпиперидон реагирует с этиловым эфиром никотиновой кислоты с образованием α-никотиноил-N-бензоил-2-пиперидон. Тогда этот продукт декарбоксилированный, проходит кольцо закрытия, и гидролиз амида с образованием анабазеина.

Дополнительные синтетические стратегии были с тех пор разработаны Блумом,[5] Золтевич,[6] Смит,[7] и Виллемен.[8]
Производные
Из-за довольно неспецифического связывания анабазеина с никотиновыми ацетилхолиновыми рецепторами от этой молекулы отказались как от полезного инструмента в исследованиях или медицине. Однако производные анабазеина были идентифицированы с более селективным профилем связывания α7. Одна такая производная (ГТС-21, 3- (2,4-диметоксибензилиден) -анабазеин) изучался как кандидат в лекарство от когнитивных нарушений и нарушений памяти, особенно связанных с шизофрения; это было изучено в фаза II клинических испытаний без перехода в III фазу.[9] Более того, модификация анабазеинпиридинового ядра привела к получению новых производных, наделенных связывающей и функциональной селективностью в отношении подтипа никотинового ацетилхолинового рецептора α3β4.[10]
Рекомендации
- ^ Уиллер, JW; Олубаджо, О; Шторм, CB; Даффилд, РМ (6 марта 1981 г.). «Анабазеин: ядовитый алкалоид афеногастра». Наука. 211 (4486): 1051–2. Дои:10.1126 / science.211.4486.1051. PMID 17744933.
- ^ а б c d е Кем, Уильям; Соти, Ференц; Уайлдебор, Кристин; ЛеФрансуа, Сьюзен; Макдугалл, Келли; Вэй, Дун-Цин; Чжоу, Куо-Чен; Ариас, Хьюго Р. (2006-04-06). «Немертин токсин анабазеин и его производное DMXBA (GTS-21): химические и фармакологические свойства». Морские препараты. 4 (3): 255–273. Дои:10.3390 / md403255. ЧВК 3663414.
- ^ Кемь, WR; Махнир, ВМ; Папке, Р.Л .; Лингл, CJ (декабрь 1997 г.). «Анабазеин является мощным агонистом мышечных и нейрональных альфа-бунгаротоксин-чувствительных никотиновых рецепторов». Журнал фармакологии и экспериментальной терапии. 283 (3): 979–92. PMID 9399967.
- ^ Падилья, Отредактированный Дином Ф. Мартином [и] Джорджем М. (1973). Морская фармакогнозия; действие морских биотоксинов на клеточном уровне (Первое изд.). Нью-Йорк: Academic Press. стр.54–55. ISBN 978-0124745506.CS1 maint: дополнительный текст: список авторов (связь)
- ^ Блум, Линда. «Влияние растворителя на равновесие кольцевого гидролиза анабазеина и синтез аналогов анабазеина и никотина». Университет Флориды. Получено 5 мая 2015.
- ^ Zoltewicz, John A .; Круски, Майкл П. (август 1995 г.). «Превосходный синтез холинергического анабазеина». Органические препараты и процедуры International. 27 (4): 510–513. Дои:10.1080/00304949509458490.
- ^ Смит, Аарон. «Синтез и радиоактивное мечение производных бензилиден-анабазеина трифторбората калия». Университет Теннесси - Ноксвилл. Цитировать журнал требует
| журнал =(помощь) - ^ Виллемен, Дидье; Хачеми, Мессауд (2001). «Фторид цезия на оксиде кальция в качестве сильного основного катализатора. Синтез флавонов и алкалоидов табака». Кинетика реакций и буквы катализа. 72 (1): 3–10. Дои:10.1023 / А: 1010597826749.
- ^ Селанир, Сильвен; Поли, Соня (13.10.2014). Терапия малыми молекулами при шизофрении. Springer. п. 248. ISBN 9783319115023. Получено 2015-04-20.
- ^ Матера, Карло; Куадри, Марта; Sciaccaluga, Мириам; Поме, Диего Юрий; Фасоли, Франческа; Де Амичи, Марко; Фучиле, Серджио; Готти, Сесилия; Далланоче, Клелия (27 января 2016 г.). «Модификация анабазеинпиридинового ядра позволяет достичь связывания и функциональной селективности в отношении подтипа никотинового ацетилхолинового рецептора α3β4». Европейский журнал медицинской химии. 108: 392–405. Дои:10.1016 / j.ejmech.2015.11.045. PMID 26706350.
