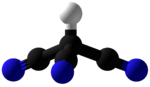
Цианоформ - Cyanoform
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Метантрикарбонитрил | |||
| Другие имена Трицианометан | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ChemSpider | |||
PubChem CID | |||
| |||
| |||
| Характеристики | |||
| C4ЧАСN3 | |||
| Молярная масса | 91.073 г · моль−1 | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Цианоформ (трицианометан) это цианоуглерод и производное метана с тремя циано группы. В течение многих лет химики не могли выделить это соединение в виде чистой свободной кислоты. Однако в сентябре 2015 года появились сообщения об успешной изоляции.[1]
Характеристики
Разбавленные растворы этой кислоты, а также ее солей хорошо известны давно. Цианоформ считается одним из самых кислых угольные кислоты с оценкой pKа -5,1 в воде и измеренное значение pKа 5,1 в ацетонитриле.[2] Реакция серная кислота с трицианометанид натрия в воде (реакция, впервые опробованная Г. Шмидтманном в 1896 г., не принесла окончательных результатов)[3]), как сообщается, приводит к образованию гидрата (NC)3C−ЧАС3О+ или образование (Z) -3-амино-2-циано-3-гидроксиакриламид (H2N) (ОН) C = C (CN) CONH2 в зависимости от конкретных условий.[4] Сообщается, что реакция газообразного HCl с трицианометанидом натрия, растворенным в ТГФ, дает 1-хлор-1-амино-2,2-дицианоэтилен ((NC)2С = С (NH2) Cl) и его таутомер.
Изоляция
В сентябре 2015 года цианоформ была успешно изолирована группой ученых из Мюнхенского университета Людвига Максимилиана. Команда обнаружила, что цианоформ стабилен при температурах ниже –40 ° C; Ранее считалось, что цианоформ стабилен при комнатной температуре. Выделение подтвердило, что цианоформ представляет собой бесцветную жидкость.[5]
Рекомендации
- ^ Солтнер, Т .; Häusler J .; Корнат А.Дж. «Существование трицианометана» Angewandte Chemie International Edition 2015. Дои:10.1002 / anie.201506753
- ^ Raamat, E .; Kaupmees, K .; Овсянников, Г .; Trummal, A .; Kütt, A .; Saame, J .; Koppel, I .; Кальюранд, I .; Губа, L .; Родима, Т .; Pihl, V .; Koppel, I.A .; Лейто, И. (2013). «Кислотности сильных нейтральных кислот Бренстеда в различных средах». J. Phys. Орг. Chem. 26 (2): 162–170. Дои:10.1002 / poc.2946.
- ^ Шмидтманн, Х. (1896 г.). "Ueber einige Derivate des Malonitrils" (PDF). Berichte der deutschen chemischen Gesellschaft. 29 (2): 1168–1175. Дои:10.1002 / cber.18960290204.
- ^ Шишак, Дубравка; McCusker, Lynne B .; Бакл, Андреа; Wuitschik, Георг; Ву И-Линь; Швейцер, В. Бернд; Дуниц, Джек Д. (2010). «В поисках трицианометана (цианоформа)». Химия: европейский журнал. 16 (24): 7224–30. Дои:10.1002 / chem.201000559. PMID 20480465.
- ^ Родинка, B - Наконец-то создана неуловимая кислота https://www.sciencenews.org/article/elusive-acid-finally-created