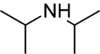
Диизопропиламин - Diisopropylamine
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC N- (Пропан-2-ил) пропан-2-амин | |
| Другие имена Ди (пропан-2-ил) амин N-Изопропилпропан-2-амин (Диизопропил) амин (Название диизопропиламин устарело.) | |
| Идентификаторы | |
3D модель (JSmol ) | |
| Сокращения | DIPA |
| 605284 | |
| ChemSpider | |
| ECHA InfoCard | 100.003.235 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1158 |
| |
| |
| Характеристики | |
| C6ЧАС15N | |
| Молярная масса | 101.193 г · моль−1 |
| Внешность | Бесцветная жидкость |
| Запах | Рыбный, аммиачный |
| Плотность | 0,722 г мл−1 |
| Температура плавления | -61,00 ° С; -77,80 ° F; 212,15 К |
| Точка кипения | От 83 до 85 ° С; От 181 до 185 ° F; От 356 до 358 К |
| смешивающийся[1] | |
| Давление газа | 9,3 кПа (при 20 ° C)[2] |
| Кислотность (пKа) | 11,07 (в воде) (конъюгированная кислота) |
| Основность (пKб) | 3.43[3] |
| 1.392–1.393 | |
| Термохимия | |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | От −173,6 до −168,4 кДж моль−1 |
Станд. Энтальпия горение (ΔcЧАС⦵298) | От −4,3363 до −4,3313 МДж моль−1 |
| Опасности | |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| H225, H302, H314, H332 | |
| P210, P280, P305 + 351 + 338, P310 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | -17 ° С (1 ° F, 256 К) |
| 315 ° С (599 ° F, 588 К) | |
| Пределы взрываемости | 1.1–7.1%[1] |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) |
|
LC50 (средняя концентрация ) | 1140 частей на миллион (крыса, 2 часа) 1000 частей на миллион (мышь, 2 часа)[4] |
LCLo (самый низкий опубликованный ) | 2207 частей на миллион (кролик, 2,5 часа) 2207 частей на миллион (морская свинка, 80 мин) 2207 частей на миллион (кошка, 72 мин)[4] |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 5 частей на миллион (20 мг / м3) [кожа][1] |
REL (Рекомендуемые) | TWA 5 частей на миллион (20 мг / м3) [кожа][1] |
IDLH (Непосредственная опасность) | 200 частей на миллион[1] |
| Родственные соединения | |
Родственные амины | |
Родственные соединения | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Диизопропиламин это вторичный амин с химическая формула (CH3)2HC-NH-CH (CH3)2. Он наиболее известен как литиевое производное сопряженного основания, диизопропиламид лития, известный как «LDA». LDA - это сильный, ненуклеофильное основание.
Диизопропиламин можно сушить дистилляцией от гидроксид калия (КОН) или высыхание натрий провод.[5]
Реакции и использование
Диизопропиламин в основном используется в качестве предшественника двух гербицидов, диаллата и триаллата, а также некоторых сульфенамиды используется в вулканизация резины.[6] Его также используют для приготовления N, N-диизопропилэтиламин (основание Хюнига) алкилированием диэтилсульфат.[7]
В бромид соль диизопропиламина, бромид диизопропиламмония, является органическим молекулярное твердое вещество чьи кристаллы сегнетоэлектрик при комнатной температуре.[8] Это делает его возможной более биосферно инертной альтернативой титанат бария.
Подготовка
Диизопропиламин коммерчески доступен. Он может быть подготовлен восстановительное аминирование из ацетон с аммиак используя модифицированный оксид меди, в общем хромит меди, как катализатор:[9][10]
- NH
3 + 2(CH
3)
2CO + 2ЧАС
2 → C
6ЧАС
15N + 2ЧАС
2О
Токсичность
Вызывает ожоги всеми путями воздействия. Вдыхание паров с высокой концентрацией может вызвать такие симптомы, как головная боль, головокружение, усталость, тошнота и рвота.[11]
Рекомендации
- ^ а б c d е Карманный справочник NIOSH по химической опасности. "#0217". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Апрель 2019 г. «ДИИЗОПРОПИЛАМИН» Проверять
| url =ценить (помощь). - ^ «ДИИЗОПРОПИЛАМИН». паб хим. Национальные институты здравоохранения США. Получено 20 октября 2015.
- ^ а б «Диизопропиламин». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ Армарего, В. Л. Ф. и Перрин, Д. Д. Очистка лабораторных химикатов 4-е изд. стр.186, Баттерворт и Хайнеманн: Бостон, 1996.
- ^ Карстен Эллер, Эрхард Хенкес, Роланд Россбахер, Хартмут Хёке «Амины, алифатические» Энциклопедия промышленной химии Ульмана, 2000, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a02_001
- ^ Hünig, S .; Киссель, М. (1958). "Spezifische Protonenacceptoren als Hilfsbasen bei Alkylierungs- und Dehydrohalogenierungsreaktionen". Chemische Berichte. 91 (2): 380–392. Дои:10.1002 / cber.19580910223.
- ^ «Органическая альтернатива оксидам? Молекула органического сегнетоэлектрика перспективна для микросхем памяти и сенсоров». Phys.org. 24 января 2013 г.
- ^ Карл Лёффлер (1910). "Über eine neue Bildungsweise primärer und sekundärer Amine aus Ketonen" (PDF). Берихте. 43 (2): 2031–2035. Дои:10.1002 / cber.191004302145.
- ^ США 2686811, Уиллард Булл, "Одностадийный процесс получения диизопропиламина"
- ^ «ПАСПОРТ БЕЗОПАСНОСТИ - Триэтиламин». ThermoFisher Scientific. 17 янв.2018 г.. Получено 18 июня, 2020.

