Правило Ле Бель – Ван т Гоффа - Le Bel–Van t Hoff rule - Wikipedia
В органическая химия, то Правило Ле Бель – Ван 'т Гоффа заявляет, что количество стереоизомеры органического соединения, не содержащего внутренних плоскости симметрии 2п, куда п представляет собой количество асимметричный углерод атомы. Джозеф Акилле Ле Бель[1] и Якобус Хенрикус ван 'т Хофф[2] оба заявили об этой гипотезе в 1874 году, и это объясняло всю известную в то время молекулярную асимметрию.[3]
Например, четыре атома углерода альдогексоза класс молекул асимметричен, поэтому правило Ле Беля – Ван'та Гоффа дает вычисление 24 = 16 стереоизомеров. Это действительно так: этих химикатов два энантиомеры каждый из восьми разных диастереомеры: аллозе, Altrose, глюкоза, манноза, Gulose, идоз, галактоза, и таран.
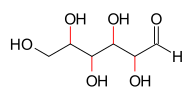 Четыре асимметричных атома углерода в глюкозе (четыре связи углерод-кислород отмечены красным)
Четыре асимметричных атома углерода в глюкозе (четыре связи углерод-кислород отмечены красным)
Рекомендации
- ^ Ле Бель, Жозеф Ахилл (1874). "Sur les Relations qui existing entre les formules atomiques des corps organiques et le pouvoir rotatoire de leurs disolutions" [О связи между атомными формулами органических веществ и вращательной способностью их растворов]. Bulletin de la Société Chimique de Paris (На французском). 22: 337–347. Cite имеет пустой неизвестный параметр:
|1=(помощь) - ^ Ван 'т Хофф, Якобус Хенрикус (1874). "Sur les formules de structure dans l'espace" [О структурных формулах в космосе]. Archives Néerlandaises des Sciences Exactes et Naturelles (На французском). 9: 445–454.
- ^ «Правило Ле Бель – ван 'т Гоффа». Медицинский словарь TheFreeDictionary.
| Этот органическая химия статья - это заглушка. Вы можете помочь Википедии расширяя это. |

