Неф реакция - Nef reaction
| Неф реакция | |
|---|---|
| Названный в честь | Джон Ульрик Неф |
| Тип реакции | Реакция замещения |
| Идентификаторы | |
| Портал органической химии | неф-реакция |
| RSC ID онтологии | RXNO: 0000157 |
В Неф реакция является органическая реакция описывая кислота гидролиз соли первичного или вторичного нитроалкан (1) чтобы альдегид или кетон (3) и оксид азота (4). Реакция была предметом нескольких обзоров литературы.[1][2][3]

О реакции сообщил в 1894 г. химик. Джон Ульрик Неф,[4] кто лечил натриевую соль нитроэтан с серная кислота в результате 85–89% Уступать закиси азота и выход не менее 70% ацетальдегид. Тем не менее, реакция была впервые высказана годом ранее, в 1893 году, Коноваловым:[5] который превратил калиевую соль 1-фенилнитроэтана с серной кислотой в ацетофенон.
В Неф реакция не следует путать с Неф синтез.
Механизм реакции
В механизм реакции начиная с нитронат соль как резонансные структуры 1а и 1b изображено ниже:
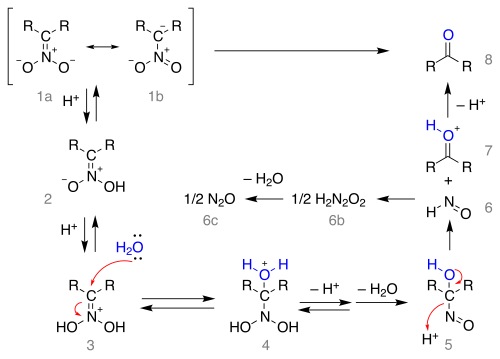
Соль протонируется с образованием нитроновая кислота 2 (в некоторых случаях эти нитронаты были изолированы) и еще раз до иминий ион 3. Этот промежуточный продукт подвергается атаке воды в нуклеофильное присоединение формирование 4 который теряет протон, а затем воду в 1-нитрозо -алканол 5 который, как полагают, отвечает за темно-синий цвет реакционной смеси во многих реакциях Нефа. Это промежуточное звено перестраивается в азотистая кислота 6 (формирование оксид азота 6c через 6b) и оксониевый ион 7 который теряет протон, чтобы сформировать карбонил соединение.
Обратите внимание, что для образования нитронатной соли из нитросоединения требуется альфа-водород атома, и поэтому реакция с третичными нитросоединениями не удается.
Объем
Реакция Нефа часто встречается в органический синтез. Он был применен в химия углеводов как метод расширения цепи для альдозы например в маркировка изотопов из C14-D-манноза и C14-D-глюкоза от D-арабиноза и C14-нитрометан (первый шаг здесь Реакция Генри ):

Противоположная реакция - это Деградация Воля.
Реакция также используется в сочетании с Реакция Майкла в синтезе γ -кето-карбонилы, такие как:[6]
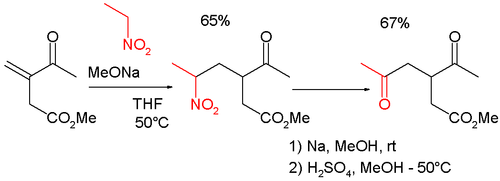
или 2,5-гептандион[7]
Гидролиз нитросоединений сильной кислотой без промежуточной солевой стадии приводит к образованию карбоновые кислоты и гидроксиламин соли.
Стадия гидролиза реакции Нефа также может быть выполнена с Кислоты Льюиса такие как хлорид олова (IV)[8] и хлорид железа (III)[9] или окислители, такие как оксон.[10]
использованная литература
- ^ Ноланд, Вэйланд Э. (1955). «Реакция НЭФ». Химические обзоры. 55 (1): 137–155. Дои:10.1021 / cr50001a003.
- ^ Пинник, Гарольд В. (1990). «Нефская реакция». В пакете, Лео А. (ред.). Объем органических реакций 38 (1-е изд.). Нью-Йорк: Вили. С. 655–792. Дои:10.1002 / 0471264180.or038.03. ISBN 9780471515944.
- ^ Грирсон, Дэвид С .; Хассон, Анри-Филипп (1991). «4.7 - Реакции типа Полоновского, Пуммерера и реакция Нефа». В Тросте, Барри; Флеминг, Ян (ред.). Комплексный органический синтез: селективность, стратегия и эффективность в современном органическом синтезе, том 6 (1-е изд.). Нью-Йорк: Пергамон. С. 909–947. Дои:10.1016 / B978-0-08-052349-1.00175-X. ISBN 9780080359298.
- ^ Неф, Джон Ульрик (1894). "Ueber die Construction der Salze der Nitroparaffine". Юстус Либигс Аннален дер Хеми. 280 (2–3): 263–291. Дои:10.1002 / jlac.18942800209.
- ^ Коновалов.,: Журн. Phys. Chem. Soc. 2 1893, 6 (I), 509.
- ^ Удобный синтез γ-функционализированных циклопентенонов Нур Лахмар, Таицир Бен Айед, Монсеф Беллассуед и Хассен Амри Журнал органической химии Байльштейна 2005, 1:11 Дои:10.1186/1860-5397-1-11
- ^ Макмерри, Джон Э .; Мелтон, Джек (1977). «Превращение нитро в карбонил озонолизом нитронатов: 2,5-гептандион». Органический синтез. 56: 36. Дои:10.15227 / orgsyn.056.0036.
- ^ Миясита, Масааки; Янами, Тецудзи; Йошикоши, Акира (1981). «Синтез 1,4-дикетонов из эфиров силил енола и нитроолефинов: 2- (2-оксопропил) циклогексанон». Органический синтез. 60: 117. Дои:10.15227 / orgsyn.060.0117.
- ^ Хайнцельман, Р. В. (1955). «о-Метоксифенилацетон». Органический синтез. 35: 74. Дои:10.15227 / orgsyn.035.0074.
- ^ Чекерелли, Паоло; Куриния, Массимо; Маркотуллиоа, Мария Карла; Эпифаноа, Франческо; Росатия, Орнелио (1998). "Oxone® способствует реакции Нефа. Простое превращение нитрогруппы в карбонил". Синтетические коммуникации. 28 (16): 3057–3064. Дои:10.1080/00397919808004885.
