Тетрабензилцирконий - Tetrabenzylzirconium
 | |
| Идентификаторы | |
|---|---|
3D модель (JSmol ) | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| C28ЧАС28Zr | |
| Молярная масса | 455.756 г · моль−1 |
| Внешность | оранжевое твердое вещество |
| Плотность | 1,34-1,39 г / см3[1] |
| Температура плавления | 133–134 ° С (271–273 ° F, 406–407 К) |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Тетрабензилцирконий является циркониевое соединение с формулой Zr (CH2C6ЧАС5)4. В молекуле присутствует диамагнитный Zr (IV), связанный с четырьмя бензиловые лиганды. Это оранжевое, чувствительное к воздуху и свету твердое вещество, растворимое в углеводородных растворителях. Соединение является предшественником катализаторов полимеризации олефинов.[2][3]
Строение, синтез, реакции
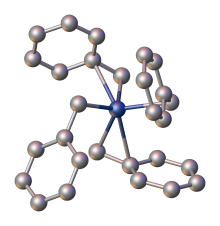
Структура тетрабензилциркония, определенная с помощью рентгеновской кристаллографии, без атомов H для ясности.[1]
Рентгеновская кристаллография демонстрирует высокую гибкость бензильных лигандов: один полиморф имеет четыре η2-лиганды, а другой - два η1- и два η2-бензил лиганды.[1]
Соединение получают путем объединения хлорида бензилмагния и тетрахлорид циркония в диэтиловом эфире. Он легко подвергается протонолизу, например с хлороводородом:
- Zr (CH2C6ЧАС5)4 + HCl → Zr (CH2C6ЧАС5)3Cl + CH3C6ЧАС5
Смотрите также
- Тетрабензилтитан (RN = 17520-19-3)[4]
Рекомендации
- ^ а б c Ронг, Йи; Аль-Харби, Ахмед; Паркин, Жерар (2012). "Zr – CH с высокой степенью изменчивости2–Ph-связывающие углы в тетрабензилцирконии: анализ режимов координации бензиллиганда ». Металлоорганические соединения. 31 (23): 8208–8217. Дои:10.1021 / om300820b.
- ^ Tshuva, Edit Y .; Гольдберг, Израиль; Кол, Моше (2000). «Изоспецифическая живая полимеризация 1-гексена легкодоступным неметаллоценом C2-Симметричный циркониевый катализатор ». Журнал Американского химического общества. 122 (43): 10706–10707. Дои:10.1021 / ja001219g.
- ^ Zucchini, U .; Albizzati, E .; Джаннини, У. (1971). «Синтез и свойства некоторых производных бензила титана и циркония». Журнал металлоорганической химии. 26: 357–372. Дои:10.1016 / S0022-328X (00) 82618-2.
- ^ Дэвис, Гвинет Р .; Jarvis, J. A. J .; Килборн, Б. Т. (1971). «Кристаллическая и молекулярная структура (при –40 ° C) тетрабензилов титана, гафния и олова». J. Chem. Soc. D (23): 1511–1512. Дои:10.1039 / C29710001511.
