Ацетилендиол - Acetylenediol
 | |
| Имена | |
|---|---|
| Другие имена этиндиол, дигидроксиацетилен | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| C2ЧАС2О2 | |
| Молярная масса | 58,07 г / моль |
| Точка кипения | разлагается |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
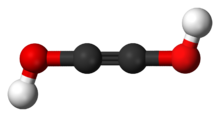
Ацетилендиол, или же этиндиол, это химическая субстанция с формулой HO − C≡C − OH (an Инол ). Это диол из ацетилен. Ацетилендиол нестабилен в конденсированной фазе, хотя его таутомер глиоксаль (CHO)2 хорошо известен.
Обнаружение
Ацетилендиол впервые был обнаружен в газовой фазе масс-спектрометрии.[1] Позднее соединение было получено фотолизом квадратная кислота в матрица из твердого аргона при 10 К (-263 ° С).[2]
Производные
Производные алкоксидов
Хотя диол существует лишь временно в концентрированной форме, соли ацетилендиолат (этиндиолат) дианион −O − C≡C − O− хорошо известны. Эти металлоорганические соединения (конкретно, алкоксиды ) формально являются производными этиндиола потерей двух ионы водорода, но обычно они не создаются таким образом.
Типичный путь синтеза этих солей - восстановление монооксида углерода. Ацетилендиолат калия (K2C2О2) был впервые получен Либих в 1834 г., по реакции монооксид углерода с металлическим калий;[3] но долгое время считалось, что это «карбонил калия» (KCO). В течение следующих 130 лет были описаны «карбонилы» натрий (Йоханнис, 1893 г.), барий (Гунц и Ментрель, 1903 г.), стронций (Roederer, 1906) и литий, рубидий, и цезий (Пирсон, 1933).[4] В конечном итоге было показано, что реакция дает смесь ацетилендиолата калия. K
2C
2О
2 и бензолгексолат калия K
6C
6О
6.[5]
Истинное строение этих солей было выяснено только в 1963 г. Вернер Бюхнер и Э. Вайс.[6][7]
Ацетилендиолаты также могут быть получены быстрой реакцией CO и раствора соответствующего металла в жидкости. аммиак при низкой температуре.[4] Ацетилендиолат калия представляет собой бледно-желтое твердое вещество, которое взрывоопасно реагирует с воздухом, галогенами, галогенированными углеводородами, спиртами, водой и любым веществом, содержащим кислый водород.[8]
Координационные комплексы
Ацетилендиол может образовывать координационные соединения, например [TaH (HOC≡COH) (dmpe)2Cl]+Cl− где dmpe бис (диметилфосфино) этан.[9]
Ацетилендиолат и родственные анионы, такие как дельтат C
3О2−
3 и скварат C
4О2−
4 были получены из монооксида углерода в мягких условиях путем восстановительного связывания лигандов CO в органоурановые комплексы.[10]
Прочие производные
Хотя они и не являются производными ацетилендиола, известно множество структурно родственных соединений. Примеры включают диэфиры диизопропоксиэтин ((CH3)2CH) -O-C≡C-O- (CH (CH3)2) и ди-трет-бутоксиэтин ((CH3)3C) -O-C≡C-O- (C (CH3)3).[11]
Смотрите также
Рекомендации
- ^ Terlouw, Johan K .; Бургерс, Питер С .; ван Баар, Бен Л. М .; Вайске, Томас; Шварц, Гельмут (1986). «Образование в газовой фазе HO – CC – OH, H2N – CC – NH2, H2N – CC – OH и родственные соединения путем селективного восстановления их катионов ». Chimia. 40: 357–359. Получено 1 августа 2009.
- ^ Майер, Гюнтер; Рор, Кристин (1995). «Этиндиол: фотохимическая генерация и матрично-спектроскопическая идентификация». Либигс Аннален. 1996 (3): 307–309. Дои:10.1002 / jlac.15719960304.
- ^ Юстус Либих (1834), Annalen der Chemie und Pharmacie, том 11, стр. 182. Цитируется Раймондом Н. Вртисом и др. (1988), JACS p. 7564.
- ^ а б Т. Г. Пирсон (1933), Карбонилы лития, рубидия и цезия. Nature, volume 131, стр. 166–167 (4 февраля 1933 г.). Дои:10.1038 / 131166b0
- ^ Вернер Бюхнер, Э. Вайс (1964) Zur Kenntnis der sogenannten «Alkalicarbonyle» IV [1] Über die Reaktion von geschmolzenem Kalium mit Kohlenmonoxid. Helvetica Chimica Acta, Volume 47 Issue 6, Pages 1415–1423.Дои:10.1002 / hlca.19640470604
- ^ Вернер Бюхнер, Э. Вайс (1963) Zur Kenntnis der sogenannten «Алкаликарбонил» I Die Kristallstruktur des Kalium-acetylendiolats, KOC≡COK. Helvetica Chimica Acta, том 46, выпуск 4, страницы 1121–1127. Дои:10.1002 / hlca.19630460404
- ^ Э. Вайс, Вернер Бюхнер (1963), Zur Kenntnis der sogenannten Alkalicarbonyle. II. Die Kristallstrukturen des Rubidium- und Cesium-acetylendiolats, RbOC≡CORb und CsOC≡COCs. Zeitschrift für anorganische und allgemeine Chemie, том 330, выпуск 5-6, страницы 251–258. Дои:10.1002 / zaac.19643300504
- ^ Чарльз Кеннет Тейлор (1982), Химическое поведение ацетилендиолатов щелочных металлов. Диссертация, Университет штата Пенсильвания; также Техническая записка A642321, Лаборатория прикладных исследований Парка Пенсильванского университета. 227 страниц.
- ^ Раймонд Н. Вртис, гл. Пулла Рао, Саймон Г. Ботт и Стивен Дж. Липпард (1988), Синтез и стабилизация тантал-координированного дигидроксиацетилена из двух восстановительно связанных лигандов окиси углерода Варенье. Chem. Soc., Том 110, выпуск 22, стр. 7564–7566. Дои:10.1021 / ja00230a062
- ^ Алистер С. Фрей, Ф. Джеффри Н. Клок, Питер Б. Хичкок (2008 г.), Механистические исследования восстановительной циклоолигомеризации CO смешанными сэндвич-комплексами U (III); Молекулярная структура [(U (η-C8ЧАС6{Si'Pr3-1,4}2) (η-Cp*)]2(μ-η1: η1-C2О2) Журнал Американского химического общества, том 130, выпуск 42, страницы 13816–13817. Дои:10.1021 / ja8059792
- ^ Анна Боу, Микель А. Перикас и Феликс Серратоса (1981), Диизопропокси и ди-трет-бутоксиэтин: стабильные диэфиры ацетилена. Тетраэдр, том 37, выпуск 7, страницы 1441-1449. Дои:10.1016 / S0040-4020 (01) 92464-0
