Атомарный углерод - Atomic carbon - Wikipedia
| Имена | |
|---|---|
| Предпочтительное название IUPAC Атомарный углерод | |
| Систематическое название ИЮПАК Метандиилиден (заместитель) Углерод (присадка) | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.028.321 |
PubChem CID | |
| |
| |
| Характеристики | |
| C | |
| Молярная масса | 12.011 г · моль−1 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Атомарный углерод, систематически названный углерод и λ0-метан, также называемый моноуглеродом, представляет собой бесцветный газообразный неорганический химический с химическая формула C (также пишется [C]). Он кинетически нестабилен при температуре и давлении окружающей среды, удаляется автополимеризацией.
Атомарный углерод - простейшая форма углерода, а также предшественник углеродных кластеров. Кроме того, его можно рассматривать как мономер графита.
Номенклатура
В банальное имя моноуглерод является наиболее часто используемым и предпочтительное название ИЮПАК. Систематическое название углерод, действительный ИЮПАК название, построено по композиционной номенклатуре. Однако, как композиционное название, оно не различает разные формы чистого углерода. Систематическое название λ0-метан, также действительное название IUPAC, строится в соответствии с замещающей номенклатурой. Вместе с моноуглерод, это имя действительно отличает названное соединение, поскольку оно получено с использованием структурной информации о молекуле. Чтобы лучше отразить его структуру, свободный атомарный углерод часто обозначают как [C]. λ2-метилий ([CH]+
) это ион в результате увеличения ЧАС+
атомарным углеродом.
Характеристики
Амфотеричность
А Кислота Льюиса может соединяться с электронной парой атомарного углерода, а электронная пара основания Льюиса может соединяться с атомарным углеродом посредством присоединения:[1]
- : [C] + M → [MC]
- [C] +: L → [CL]
Из-за этого пожертвования или принятия присоединенной пары электронов атомарный углерод имеет амфотерный характер Льюиса.[2] Атомарный углерод может отдавать до двух электронных пар кислотам Льюиса или принимать до двух пар от оснований Льюиса.
Протон может соединиться с атомарным углеродом путем протонирования:
- C + ЧАС+
→ CH+
Из-за этого захвата протона (ЧАС+
), атомарный углерод и его аддукты оснований Льюиса, такие как вода, также имеют основной характер Бренстеда – Лоури. Конъюгированная кислота атомарного углерода λ2-метилий (CH+
).
- ЧАС
3О+
+ C ⇌ ЧАС
2О + CH+
Однако водные растворы аддуктов нестабильны из-за гидратации углеродного центра и λ2-метилиевая группа для получения λ2-метанол (CHOH) или λ2-метан (CH
2) или гидроксиметилий (CH
2ОЙ+
) группы соответственно.
- ЧАС
2О + C → CHOH - ЧАС
2О + CH+
→ CH
2ОЙ+
Λ2-метанольная группа в аддуктах потенциально может изомеризоваться с образованием формальдегид, или дополнительно гидратироваться с образованием метандиол. Группа гидроксиметилия в аддуктах потенциально может быть дополнительно гидратирована с образованием дигидроксиметилий (СН (ОН)+
2), или окисляться водой с образованием формилия (HCO+
).[1]
Электромагнитные свойства
Электроны в атомарном углероде распределяются по атомным орбиталям в соответствии с принципом aufbau для создания уникальных квантовых состояний с соответствующими уровнями энергии. Состояние с самым низким уровнем энергии или основное состояние является триплетным бирадикальным состоянием (3п0). Первые два относительно близких по энергии возбужденных состояния представляют собой синглет (1D2) и синглетный бирадикал (1S0). Нерадикальное состояние атомарного углерода систематически называют λ2-метилиден, а бирадикальные состояния, которые включают основное состояние, называют углеродом (2 •) или λ2-метандиил. 1D2 и 1S0 состояний 121,9 кДж моль−1 и 259,0 кДж моль−1 над основным состоянием соответственно. Переходы между этими тремя состояниями формально запрещены из-за требования переворота спина и / или спаривания электронов. Это означает, что атомарный углерод фосфоресцирует в ближней инфракрасной области электромагнитного спектра при 981,1 нм. Он также может флуоресцировать в инфракрасном диапазоне и фосфоресцировать в синей области при 873,0 нм и 461,9 нм соответственно при возбуждении ультрафиолетовым излучением.
Различные состояния атомарного углерода демонстрируют различное химическое поведение. Например, реакции триплетного радикала с нерадикальными частицами обычно включают отщепление, тогда как реакции синглетного нерадикального соединения включают не только отрыв, но также добавление путем вставки.
- [C]2•(3п0) + ЧАС
2О → [CHOH] → [CH] + [HO] - [C] (1D2) + ЧАС
2О → [CHOH] → CO + ЧАС
2 или же ЧАС
2CO
Производство

Этот очень короткоживущий вид создается путем пропускания большого тока через два соседних углеродных стержня, в результате чего возникает электрическая дуга. При этом образуется атомарный углерод. Профессор Фил Шевлин проделал основную работу в этой области на базе Обернский университет в США.
Способ создания этого вида тесно связан с образованием фуллеренов. C60, главное отличие состоит в том, что при образовании атомарного углерода используется гораздо более низкий вакуум.
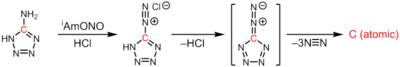
Атомарный углерод образуется при термолизе 5-диазотетразола при экструзии 3 эквивалентов диазота:[3]
CN6 →: C: + 3N2
Чистый источник атомарного углерода можно получить на основе термическое разложение из карбид тантала. В разработанном источнике[4] уголь загружается в тонкостенный тантал трубка. После герметизации он нагревается прямым электрический ток. Сольватированные атомы углерода диффундируют к внешней поверхности трубки, и при повышении температуры наблюдается испарение атомарного углерода с поверхности танталовой трубки. Источник содержит чисто углеродные атомы без каких-либо дополнительных частиц.
Декарбонилирование недооксида углерода
Атомарный углерод может производиться недооксидом углерода. декарбонилирование. В этом процессе недокись углерода разлагается с образованием атомарного углерода и монооксид углерода согласно уравнению:
- C
3О
2 → 2 CO + [C]
Процесс включает монооксид дикарбона в качестве промежуточного звена и происходит в два этапа. Фотолитическое дальнее ультрафиолетовое излучение необходимо для обоих процессов декарбонилирования.
- OCCCO → [CCO] + CO
- [CCO] → CO + [C]
Использует
Обычно образец атомарного углерода существует как смесь возбужденных состояний в дополнение к основному состоянию в термодинамическом равновесии. Каждое состояние по-разному влияет на механизмы реакции, которые могут иметь место. Простой тест, используемый для определения вовлеченного состояния, заключается в использовании диагностической реакции триплетного состояния с O2, если выход реакции не меняется, это указывает на синглетное состояние. Основное бирадикальное состояние обычно претерпевает реакции отрыва. Атомарный углерод был использован для создания «истинного» карбены за счет абстракции кислород атомы из карбонил группы:
- р2С = О +: С: → R2C: + CO
Карбены, образованные таким образом, будут проявлять истинное карбеническое поведение. Карбены, полученные другими методами, такими как диазосоединения, могут проявлять свойства, лучше приписываемые диазосоединению, используемому для получения карбена (которое имитирует поведение карбена), чем самому карбену. Это важно с точки зрения механистического понимания истинного поведения карбена.
Реакции
Поскольку атомарный углерод является электронодефицитной разновидностью, он самопроизвольно автополимеризуется в чистом виде или превращается в аддукт при обработке кислотой или основанием Льюиса. Окисление атомарного углерода дает окись углерода, тогда как восстановление дает λ2-метан.Неметаллы, включая кислород, сильно атакуют атомарный углерод, образуя соединения двухвалентного углерода:
- 2 [C] + О
2 → 2 СО
Атомарный углерод очень реактивен, большинство реакций очень экзотермичны. Обычно их проводят в газовой фазе при температуре жидкого азота (77 К). Типичные реакции с органическими соединениями включают:[5]
- Вставка в связь C-H в алканах с образованием карбена
- Деоксигенация карбоксильных групп в кетонах и альдегидах с образованием карбена, 2-бутанона с образованием 2-бутанилидена.
- Вставка в двойные связи углерод-углерод с образованием циклопропилидена, который подвергается раскрытию цикла, простым примером является вставка в алкен с образованием кумулена.
При введении воды в связь O-H образуется карбен H-C-OH, который перестраивается в формальдегид, HCHO.
Рекомендации
- ^ а б Husain, D .; Кирш, Л. Дж. (1 января 1971 г.). «Реакции атомарного углерода C (23пJ) методом кинетической абсорбционной спектроскопии в вакуумном ультрафиолете ». Труды общества Фарадея. 67: 2025–2035. Дои:10.1039 / TF9716702025.
- ^ Housecroft, Catherine E .; Шарп, Алан Г. (2012). «Кислоты, основания и ионы в водном растворе». Неорганическая химия (4-е изд.). Pearson Education, Ltd. стр. 227. ISBN 978-0-273-74275-3.
- ^ Шевлин, Филипп Б. (2002-05-01). «Образование атомарного углерода при разложении хлорида 5-тетразолилдиазония». Журнал Американского химического общества. 94 (4): 1379–1380. Дои:10.1021 / ja00759a069.
- ^ Краснокутский, С. А .; Хуйскен, Ф. (15 сентября 2014 г.). «Простой и чистый источник низкоэнергетического атомарного углерода». Письма по прикладной физике. 105 (11): 113506. Bibcode:2014АпФЛ.105к3506К. Дои:10.1063/1.4895806.
- ^ Реакционная промежуточная химия, Роберт А. Мосс, Мэтью С. Платц и Мейтленд Джонс-младший, Wiley-Blackwell, (2004), ISBN 978-0471233244
Эта статья включает в себя список общих Рекомендации, но он остается в основном непроверенным, потому что ему не хватает соответствующих встроенные цитаты. (Сентябрь 2010 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
дальнейшее чтение
- Уайт Г. Дж .; Падман Р. (1991). «Изображения атомарного углерода в межзвездной среде». Природа. 354 (6354): 511–513. Bibcode:1991 Натур. 354..511Вт. Дои:10.1038 / 354511a0. S2CID 4262147.
- П. Б. Шевлин (1972). «Образование атомарного углерода при разложении хлорида 5-тетразоилдиазония». Варенье. Chem. Soc. 94 (4): 1379–1380. Дои:10.1021 / ja00759a069.
- П. Б. Шевлин (1980). «Получение и реакция атомарного углерода». В Р. А. Абрамовича (ред.). Реактивные промежуточные продукты. 1. Нью-Йорк: Пленум Пресс. п. 1.
- М. Дж. С. Дьюар; Д. Дж. Нельсон; П. Б. Шевлин; К. А. Бьесида (1981). «Экспериментальное и теоретическое исследование механизма деоксигенации карбонильных соединений атомарным углеродом». Варенье. Chem. Soc. 103 (10): 2802. Дои:10.1021 / ja00400a052.
- Biesiada, Keith A .; Шевлин, Филипп Б. (1984). «Внутримолекулярное улавливание промежуточного соединения при дезоксигенировании карбонильного соединения атомарным углеродом». Журнал органической химии. 49 (6): 1151. Дои:10.1021 / jo00180a047.
- Мосс, Роберт А; Джонс, Мейтленд (2004). «Атомный углерод». Реакционная промежуточная химия. стр.463–500. ISBN 978-0-471-23324-4.
