DPPH - DPPH
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК ди (фенил) - (2,4,6-тринитрофенил) иминоазан | |
| Другие имена 2,2-дифенил-1-пикрилгидразил 1,1-дифенил-2-пикрилгидразил радикал 2,2-дифенил-1- (2,4,6-тринитрофенил) гидразил Дифенилпикрилгидразил | |
| Идентификаторы | |
3D модель (JSmol ) | |
| Сокращения | DPPH |
| ChemSpider | |
| ECHA InfoCard | 100.015.993 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C18ЧАС12N5О6 | |
| Молярная масса | 394,32 г / моль |
| Внешность | Порошок от черного до зеленого, фиолетовый в растворе |
| Плотность | 1,4 г / см3 |
| Температура плавления | 135 ° С (275 ° F, 408 К) (разлагается) |
| нерастворимый | |
| Растворимость в метанол | 10 мг / мл |
| Опасности | |
| Паспорт безопасности | MSDS |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
DPPH это обычное сокращение для органических химическое соединение 2,2-дифенил-1-пикрилгидразил. Это кристаллический порошок темного цвета, состоящий из стабильных свободный радикал молекулы. DPPH имеет два основных применения, как в лабораторных исследованиях: одно - это монитор химических реакций с участием радикалов, в первую очередь это обычная антиоксидант проба[1] а другой - эталон положения и интенсивности электронный парамагнитный резонанс сигналы.
Свойства и приложения
DPPH имеет несколько кристаллических форм, которые различаются симметрией решетки и температура плавления (т.пл.). Коммерческий порошок представляет собой смесь фаз, плавящуюся при температуре ~ 130 ° C. DPPH-I (т.пл.106 ° C) ромбический, DPPH-II (т.пл.137 ° C) является аморфным, а DPPH-III (т.пл.128–129 ° C) является аморфным. триклинический.[2]
DPPH - хорошо известный радикал и ловушка («поглотитель») для других радикалов. Следовательно, снижение скорости химической реакции при добавлении DPPH используется в качестве индикатора радикального характера этой реакции. Из-за сильной полосы поглощения с центром около 520 нм радикал DPPH в растворе имеет темно-фиолетовый цвет, а при нейтрализации он становится бесцветным или бледно-желтым. Это свойство позволяет визуально контролировать реакцию, а количество исходных радикалов можно подсчитать по изменению оптического поглощения при 520 нм или сигнала ЭПР DPPH.[3]
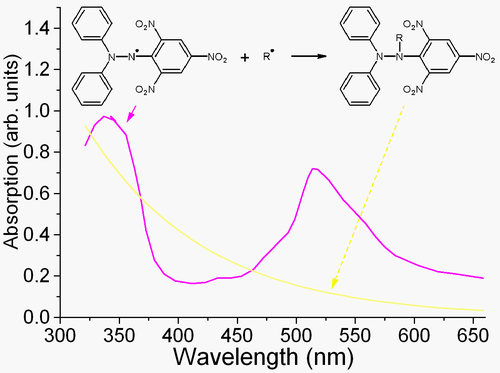
Поскольку DPPH является эффективным уловителем радикалов, он также является сильным ингибитором радикально-опосредованная полимеризация.[4]

Как стабильный и хорошо охарактеризованный твердый источник радикалов, DPPH является традиционным и, возможно, самым популярным стандартом положения (g-маркер) и интенсивности электронный парамагнитный резонанс (ЭПР) сигналы - количество радикалов для свежеприготовленного образца может быть определено путем взвешивания, а коэффициент расщепления ЭПР для DPPH откалиброван при g = 2,0036. Сигнал DPPH удобен тем, что он обычно сосредоточен в одной линии, интенсивность которой линейно увеличивается с корнем квадратным из микроволновой мощности в более широком диапазоне мощностей. Разбавленный характер радикалов DPPH (один неспаренный спин на 41 атом) приводит к относительно небольшой ширине линии (1,5–4,7 Гаусс). Однако ширина линии может увеличиваться, если молекулы растворителя остаются в кристалле и если измерения проводятся с помощью высокочастотной установки ЭПР (~ 200 ГГц), где становится заметной небольшая g-анизотропия DPPH.[5][6]
Хотя DPPH обычно является парамагнитным твердым телом, он превращается в антиферромагнитный состояние при охлаждении до очень низких температур порядка 0,3 К. Впервые об этом явлении сообщил Александр Прохоров в 1963 г.[7][8][9][10]
Рекомендации
- ^ Пересмотр антиоксидантного анализа DPPH. Ом П. Шарма и Тедж К. Бхат, пищевая химия, том 113, выпуск 4, 15 апреля 2009 г., страницы 1202–1205, Дои:10.1016 / j.foodchem.2008.08.008
- ^ Kiers, C.T .; De Boer, J. L .; Olthof, R .; Спек, А. Л. (1976). «Кристаллическая структура модификации 2,2-дифенил-1-пикрилгидразил (DPPH)». Acta Crystallographica Раздел B. 32 (8): 2297. Дои:10.1107 / S0567740876007632.
- ^ Марк С. М. Алджер (1997). Словарь по науке о полимерах. Springer. п. 152. ISBN 0-412-60870-7.
- ^ Cowie, J. M. G .; Арриги, Валерия (2008). Полимеры: химия и физика современных материалов (3-е изд.). Шотландия: CRC Press. ISBN 978-0-8493-9813-1.
- ^ М.Дж. Дэвис (2000). Электронный парамагнитный резонанс. Королевское химическое общество. п. 178. ISBN 0-85404-310-1.
- ^ Чарльз П. Пул (1996). Электронный спиновой резонанс: исчерпывающий трактат по экспериментальным методам. Courier Dover Publications. п. 443. ISBN 0-486-69444-5.
- ^ Прохоров А. Федоров. ЖЭТФ 16 (1963) 1489.
- ^ Теруаки Фухито (1981). «Магнитное взаимодействие в комплексах DPPH и DPPH – растворитель без растворителей». Бюллетень химического общества Японии. 54 (10): 3110. Дои:10.1246 / bcsj.54.3110.[постоянная мертвая ссылка ]
- ^ Стиг Лундквист (1998). "А.М. Прохоров". Нобелевские лекции по физике, 1963-1970 гг.. World Scientific. п. 118. ISBN 981-02-3404-Х.
- ^ Александр Михайлович Прохоров, Нобелевская премия по физике 1964 г.

