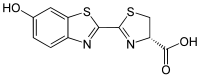
Люциферин светлячка - Firefly luciferin
 | |
| Имена | |
|---|---|
| Название ИЮПАК (4S) -2- (6-гидрокси-1,3-бензотиазол-2-ил) -4,5-дигидротиазол-4-карбоновая кислота | |
| Другие имена D- (-) - Люциферин, люциферин жука | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.018.166 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C11ЧАС8N2О3S2 | |
| Молярная масса | 280.32 г · моль−1 |
| УФ-видимый (λМаксимум) | 330 нм (нейтральные и несколько кислые водные растворы) [1] |
| Абсорбция | ε330 = 18,2 мМ−1 см−1 [1] |
| Опасности | |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H315, H319, H335 | |
| P261, P264, P271, P280, P302 + 352, P304 + 340, P305 + 351 + 338, P312, P321, P332 + 313, P337 + 313, P362, P403 + 233, P405, P501 | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Люциферин светлячка (также известный как жук люциферин) это люциферин, или светоизлучающее соединение, используемое для Светлячок (Lampyridae ), железнодорожный червь (Phengodidae ), звездный червь (Rhagophthalmidae ), и жук-щелкунчик (Пирофорини ) биолюминесцентные системы. Это субстрат люцифераза (EC 1.13.12.7), который отвечает за характерное излучение желтого света от многих Светлячок разновидность.
Как и для всех других люциферинов, для получения света необходим кислород; однако также было обнаружено аденозинтрифосфат (АТФ) и магний необходимы для светового излучения.[2][3]
История
Большая часть ранних работ по химии люминесценции светлячков проводилась в лаборатории Уильям Д. МакЭлрой в Университет Джона Хопкинса. Люциферин был впервые выделен и очищен в 1949 году, хотя потребовалось несколько лет, чтобы разработать метод кристаллизации соединения с высоким выходом. Это, наряду с синтезом и выяснением структуры, было выполнено доктором Эмилем Х. Уайтом на химическом факультете Университета Джона Хопкинса.[4] Процедура была кислотно-щелочная экстракция, Учитывая карбоновая кислота группа по люциферину. Люциферин можно эффективно извлечь, используя ацетат этила при низком pH из порошка примерно 15 000 фонарей светлячков.[5] Позднее структура была подтверждена комбинированным использованием ИК-спектроскопия, УФ-видимая спектроскопия и синтетические методы разложения соединения на идентифицируемые фрагменты.[6]
Характеристики
Кристаллический люциферин оказался флуоресцентный, поглощая ультрафиолетовый свет с пиком на 327 нм и излучающий свет с пиком на 530 нм. Видимое излучение происходит при релаксации оксилюциферина из синглетного возбужденного состояния до его основного состояния.[7] Щелочные растворы вызвали красное смещение поглощения, вероятно, из-за депротонирования гидроксил группа по бензотиазол, но не влияли на эмиссию флуоресценции. Было обнаружено, что люцифериладенилат ( AMP сложный эфир люциферина) спонтанно излучает свет в растворе.[8]Различные виды светлячков используют один и тот же люциферин, однако цвет излучаемого света может сильно различаться. Свет от Photuris pennsylvanica был измерен как 552 нм (зелено-желтый), в то время как Pyrophorus plagiophthalamus было измерено, чтобы излучать свет при 582 нм (оранжевый) в вентральном органе. Такие различия, вероятно, связаны с pH изменения или различия в первичная структура люциферазы.[9] Модификация субстрата люциферина светлячка привела к излучению с "красным смещением" (до длины волны излучения 675 нм).[10]
Биологическая активность
В in vivo синтез люциферина светлячков до конца не изучен. Изучен только последний этап ферментативного пути, которым является реакция конденсации из D-цистеин с 2-циано-6-гидроксибензотиазол Эта же реакция используется для получения соединения синтетическим путем.[11] Это подтвердил радиоактивная маркировка атомов в двух соединениях и путем идентификации люциферин-регенерирующий фермент.[12]
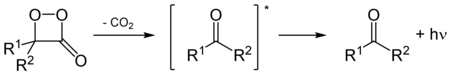
В Светлячок, окисление люциферинов, которое катализируется люциферазами, дает пероксисоединение 1,2-диоксетан. Диоксетан нестабилен и самопроизвольно распадается на углекислый газ и взволнован кетоны, которые высвобождают избыточную энергию, излучая свет (биолюминесценция ).[13]
Люциферин светлячка и модифицированные субстраты являются имитаторами жирных кислот и используются для локализации амидгидролазы жирных кислот (FAAH) in vivo.[14] Люциферин светлячка является субстратом переносчика ABCG2 и использовался как часть высокопроизводительного анализа биолюминесцентного изображения для скрининга ингибиторов переносчика.[15]
Рекомендации
- ^ а б «Информация о продукте D-люциферина» (PDF). Сигма Олдрич.
- ^ МакЭлрой WD (1947). «Источник энергии для биолюминесценции в изолированной системе». Proc Natl Acad Sci USA. 33 (11): 342–345. Bibcode:1947ПНАС ... 33..342М. Дои:10.1073 / pnas.33.11.342. ЧВК 1079070. PMID 16588763.
- ^ Грин А., МакЭлрой В.Д. (1956). «Функция аденозинтрифосфата в активации люциферина». Arch Biochem Biophys. 64 (2): 257–271. Дои:10.1016/0003-9861(56)90268-5. PMID 13363432.
- ^ Стрелер Б.Л., МакЭлрой В.Д. (1949). «Очистка люциферина светлячка». J Cell Physiol. 34 (3): 457–466. Дои:10.1002 / jcp.1030340310. PMID 15406363.
- ^ Битлер Б., МакЭлрой В.Д. (1957). «Получение и свойства кристаллического огненного люциферина». Arch Biochem Biophys. 72 (2): 358–368. Дои:10.1016/0003-9861(57)90212-6. PMID 13479120.
- ^ Уайт Э. Х., МакКапра Ф, Филд Г. Ф., МакЭлрой У. Д. (1961). «Структура и синтез люциферина светлячка». J Am Chem Soc. 83 (10): 2402–2403. Дои:10.1021 / ja01471a051.
- ^ Маркес С.М., Жоаким (2009). «Биолюминесценция светлячков: механистический подход реакций, катализируемых люциферазой». IUBMB Life. 61 (1): 6–17. Дои:10.1002 / iub.134. PMID 18949818.
- ^ Родс WC, МакЭлрой WD (1958). «Синтез и функции люцифериладенилата и оксилюцифериладенилата». J Biol Chem. 233 (6): 1528–1537. PMID 13610868.
- ^ Селигер HH, Бак JB, Fastie WG, McElroy WD (1964). "Спектральное распределение света светлячков". J Gen Physiol. 48 (1): 95–104. Дои:10.1085 / jgp.48.1.95. ЧВК 2195396. PMID 14212153.
- ^ Кияма М, Сайто Р., Ивано С., Обата Р., Нива Х, Маки С.А. (2016). «Многоцветная биолюминесценция, полученная с использованием люциферина светлячка». Актуальные темы медицинской химии. 16 (24): 2648–2655. Дои:10.2174/1568026616666160413135055. PMID 27072707.
- ^ Уайт EH, Worther H, Field GF, McElroy WD (1965). «Аналоги Люциферина Светлячка». J. Org. Chem. 30 (7): 2344–2348. Дои:10.1021 / jo01018a054.
- ^ Гоми К., Кадзияма Н. (2001). «Оксилюциферин, продукт люминесценции люциферазы светлячков, ферментативно регенерируется в люциферин». J Biol Chem. 276 (39): 36508–36513. Дои:10.1074 / jbc.M105528200. PMID 11457857.
- ^ Альдо Рода Хемилюминесценция и биолюминесценция: прошлое, настоящее и будущее, п. 57, Королевское химическое общество, 2010 г., ISBN 1-84755-812-7
- ^ Моффорд Д.М., Адамс С.Т., Кумар Редди Г.С., Рандхир Редди Г., Миллер СК (2015). «Амиды люциферина позволяют in vivo биолюминесцентное определение активности эндогенной гидролазной амид жирной кислоты». Варенье. Chem. Soc. 137 (27): 8684–8687. Дои:10.1021 / jacs.5b04357. ЧВК 4507478. PMID 26120870.
- ^ «Идентификация ингибиторов ABCG2 с помощью высокопроизводительного анализа на основе биолюминесценции». Рак Res. 69.
внешняя ссылка
- Страница биолюминесценции показаны основные типы люциферина
