Моноизотопный элемент - Monoisotopic element
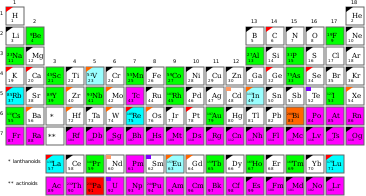
А моноизотопный элемент это элемент, который имеет только один стабильный изотоп (нуклид). Всего 26 элементов обладают этим свойством. Список приведен в следующем разделе.
Для химических элементов стабильность определяется экспериментально, поскольку существует ряд стабильных нуклидов с атомными номерами более ~ 40, которые теоретически нестабильны, но, очевидно, имеют настолько длительный период полураспада, что они не наблюдались прямо или косвенно (по результатам измерения продуктов) до распада.
Моноизотопные элементы характеризуются, за исключением единственного случая, нечетным числом протонов (нечетным Z) и четное число нейтронов. Из-за увеличения энергии за счет эффектов спаривания ядер нечетное число протонов придает нестабильность изотопам нечетного Z, который в более тяжелых элементах требует полностью спаренного набора нейтронов, чтобы компенсировать эту тенденцию к стабильности. (Четыре стабильных нуклида с нечетным Z а нечетные числа нейтронов - водород-2, литий-6, бор-10 и азот-14.)
Единственное мононуклидное исключение из странного Z правило - бериллий; его единственный стабильный первичный изотоп, бериллий-9, имеет 4 протона и 5 нейтронов. Этот элемент не может иметь стабильный изотоп с равным числом нейтронов и протонов (бериллий-8, по 4 каждого) из-за его нестабильности к альфа-распад, которому отдают предпочтение из-за чрезвычайно плотного связывания гелий-4 ядра. Он не может иметь стабильный изотоп с 4 протонами и 6 нейтронами из-за очень большого несоответствия в соотношении протон / нейтрон для такого легкого элемента. (Тем не менее, бериллий-10 имеет период полураспада 1,36 миллиона лет, что слишком мало, чтобы быть изначальный, но все же указывает на необычную стабильность для легкого изотопа с таким дисбалансом.)
Дифференциация от мононуклидных элементов
Набор моноизотопных элементов перекрывается, но не такой, как набор из 21 мононуклидные элементы, которые характеризуются наличием только одного изотопа (нуклида), встречающегося в природе.[1] Причина этого - появление некоторых долгоживущих радиоактивных первичные нуклиды в природе, которые могут образовывать примеси с моноизотопами и, таким образом, препятствовать тому, чтобы они были естественными мононуклидами. Так бывает в случаях 7 (26 − 19 = 7) моноизотопных элементов. Эти изотопы моноизотопны, но из-за присутствия долгоживущего радиоактивного первичного нуклида не являются мононуклидами. Эти элементы ванадий, рубидий, индий, лантан, европий, рений и лютеций. См. Список ниже; в двух отмеченных случаях (индий и рений) долгоживущий радионуклид на самом деле является наиболее распространенным изотопом в природе, а стабильный изотоп - менее распространенным.
В 2 дополнительных случаях (висмут[2] и протактиний ), мононуклидные элементы встречаются изначально которые не являются моноизотопами, потому что встречающийся в природе нуклид радиоактивен, и, следовательно, элемент вообще не имеет стабильных изотопов. Чтобы элемент был моноизотопным, он должен иметь один стабильный нуклид.
Список (стабильных в наблюдениях) моноизотопных элементов, упорядоченных по атомному номеру и весу
Не-мононуклидные элементы отмечены звездочкой, а долгоживущие изначальный радиоизотоп данный. В двух примечательных случаях (индий и рений) наиболее распространенным изотопом природного происхождения является умеренно радиоактивный изотоп, а в случае европия - почти половина.
- Бериллий-9
- Фтор-19
- Натрий-23
- Алюминий-27
- Фосфор-31
- Скандий-45
- Ванадий-51 * в природе встречается с 0,25% радиоактивных ванадий-50
- Марганец-55
- Кобальт-59
- Мышьяк-75
- Рубидий-85 * в природе встречается с 27,835% радиоактивных рубидий-87
- Иттрий-89
- Ниобий-93
- Родий-103
- Индий-113 * естественно встречается с большинство (95,7%) радиоактивный изотоп индий-115
- Йод-127
- Цезий-133
- Лантан-139 * в природе встречается с 0,09% радиоактивных лантан-138
- Празеодим-141
- Европий-153 * в природе встречается с 47,8% радиоактивных европий-151
- Тербий-159
- Гольмий-165
- Тулий-169
- Лютеций-175 * в природе встречается с 2,59% радиоактивных лютеций-176
- Рений-185 * естественно встречается с большинство (62,6%) радиоактивный изотоп рений-187
- Золото-197
Смотрите также
использованная литература
- ^ Н.Э. Холден, "Стандартные значения атомной массы мононуклидных элементов - 2001 г." BNL-NCS-68362, Брукхейвенская национальная лаборатория (2001)
- ^ До 2003 г. 209Считалось, что Би принадлежит к первой категории. Затем было обнаружено, что период полураспада из 1019 лет, что примерно в миллиард раз превышает возраст Вселенной. Увидеть Висмут
