Оптическое отображение - Optical mapping
Оптическое отображение[1] это метод построения упорядоченных, общегеномных, с высоким разрешением карты ограничений из одиночных окрашенных молекул ДНК, называемых «оптическими картами». Путем картирования местоположения сайтов рестрикционных ферментов вдоль неизвестной ДНК организма спектр образующихся фрагментов ДНК в совокупности служит уникальным «отпечатком пальца» или «штрих-кодом» для этой последовательности. Первоначально разработан доктором Дэвидом Шварцем и его лабораторией в Нью-Йоркском университете в 1990-х годах. [2] С тех пор этот метод стал неотъемлемой частью процесса сборки многих крупномасштабных проектов секвенирования как микробных, так и эукариотических геномов. Более поздние технологии используют плавление ДНК,[3] Конкурентное связывание ДНК[4] или ферментативное мечение[5][6] для создания оптических отображений.
Технологии
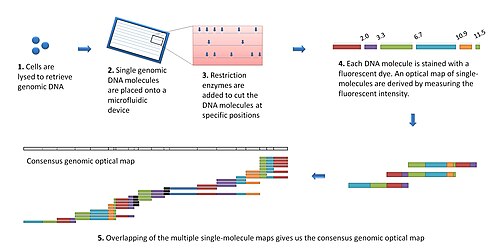
Современная платформа оптического картографирования работает следующим образом:[7]
- Геномную ДНК получают из лизированных клеток и случайным образом разрезают для получения «библиотеки» больших геномных молекул для оптического картирования.
- Отдельная молекула ДНК растягивается (или удлиняется) и удерживается на предметном стекле под флуоресцентным микроскопом за счет взаимодействия зарядов.
- Молекула ДНК переваривается добавленными рестрикционными ферментами, которые расщепляются на определенных участках переваривания. Образовавшиеся фрагменты молекул остаются прикрепленными к поверхности. Концы фрагментов в сайтах расщепления оттянуты назад (из-за эластичности линеаризованной ДНК), оставляя зазоры, которые можно идентифицировать под микроскопом.
- Фрагменты ДНК, окрашенные интеркалирующим красителем, визуализируются с помощью флуоресцентной микроскопии и измеряются путем измерения интегральной интенсивности флуоресценции. Это создает оптическую карту отдельных молекул.
- Индивидуальные оптические карты объединяются для получения согласованной геномной оптической карты.
История платформы оптического картографирования
Ранняя система
Молекулы ДНК фиксировали на расплавленной агарозе, образовавшейся между покровным стеклом и предметным стеклом микроскопа. Фермент рестрикции предварительно смешивали с расплавленной агарозой перед размещением ДНК, и расщепление запускалось добавлением магния.
Использование заряженных поверхностей
Вместо того, чтобы быть иммобилизованными в гелевой матрице, молекулы ДНК удерживались на месте за счет электростатических взаимодействий на положительно заряженной поверхности. Разрешение улучшилось таким образом, что фрагменты размером от ~ 30 kb до 800 bp могли иметь размер.
Автоматизированная система
Это включало разработку и интеграцию автоматизированной системы определения для определения нескольких отдельных молекул на слайде (например, микрочипа) для параллельной ферментативной обработки, автоматизированной флуоресцентной микроскопии для получения изображений, обработки изображений для обработки изображений, алгоритмов для построения оптических карт, кластера вычисления для обработки больших объемов данных
Система с высокой пропускной способностью с использованием микрофлюидики
Заметив, что микроматрицы, содержащие отдельные молекулы, не подходят для больших молекул геномной ДНК, микрофлюидный разработаны устройства с использованием мягкой литографии, обладающие серией параллельных микроканалов.
Система нового поколения с использованием технологии нанокодирования
Улучшение оптического картирования, называемое «Нанокодирование»,[8] имеет потенциал для повышения производительности за счет захвата удлиненных молекул ДНК в наноконфайнментах.
Сравнения
Другие методы картирования
Преимущество ОМ перед традиционными методами картирования заключается в том, что он сохраняет порядок фрагментов ДНК, тогда как порядок необходимо восстанавливать с помощью отображение ограничений. Кроме того, поскольку карты строятся непосредственно из молекул геномной ДНК, исключаются артефакты клонирования или ПЦР. Однако на каждый процесс ОМ по-прежнему влияют ложноположительные и отрицательные сайты, потому что не все сайты рестрикции расщепляются в каждой молекуле, а некоторые сайты могут быть разрезаны неправильно. На практике несколько оптических карт создаются из молекул одной и той же области генома, и для определения наилучшей консенсусной карты используется алгоритм.[9]
Другие методы анализа генома
Существует множество подходов к выявлению крупномасштабных геномных вариаций (таких как инделки, дупликации, инверсии, транслокации) между геномами. Другие категории методов включают использование микрочипы, гель-электрофорез в импульсном поле, цитогенетика и парные конечные теги.
Использует
Первоначально система оптического картирования использовалась для построения полногеномных рестрикционных карт бактерий, паразитов и грибов.[10][11][12] Он также использовался для построения и проверки бактериальных геномов.[13] Чтобы служить каркасом для сборки, собранные контиги последовательностей можно сканировать на предмет сайтов рестрикции. in silico использование известных данных о последовательностях и сопоставление их с собранной геномной оптической картой. Коммерческая компания Opgen предоставила оптические карты микробных геномов. Для более крупных геномов эукариот только лаборатория Дэвида С. Шварца (теперь в Мэдисоне-Висконсине) создала оптические карты для мышей,[14] человек,[15] рис,[16] и кукуруза.[17]
Оптическое секвенирование
Оптическое секвенирование представляет собой метод секвенирования одной молекулы ДНК, который следует за синтезом и использует технологию оптического картирования.[18][19] Подобно другим подходам к молекулярному секвенированию, таким как SMRT-секвенирование, этот метод анализирует одну молекулу ДНК, а не увеличивает исходный образец и секвенирует несколько копий ДНК. Во время синтеза нуклеотиды, меченные флуорохромом, включаются с помощью ДНК-полимераз и отслеживаются с помощью флуоресцентная микроскопия. Этот метод был первоначально предложен Дэвидом С. Шварцем и Арвиндом Раманатаном в 2003 году.
Цикл оптического секвенирования
Ниже приводится обзор каждого цикла процесса оптического секвенирования.[20]

Шаг 1: штрих-кодирование ДНК
Клетки лизируются для высвобождения геномной ДНК. Эти молекулы ДНК распутываются, помещаются на поверхность для оптического картирования, содержащую микрофлюидные каналы, и ДНК пропускается через каналы. Затем эти молекулы кодируются рестрикционными ферментами, чтобы обеспечить локализацию генома с помощью метода оптического картирования. См. Выше раздел о "Технологии" для этих шагов.
Шаг 2. Выбор шаблона
ДНКаза I добавляется для случайного разрыва установленных молекул ДНК. Затем выполняется промывка для удаления ДНКазы I. Среднее количество разрывов, возникающих на одной матрице, зависит от концентрации ДНКазы I, а также от времени инкубации.
Шаг 3: формирование разрыва
Добавляется экзонуклеаза Т7, которая использует зазоры в молекулах ДНК для расширения зазоров в направлении 5'– 3 '. Количество экзонуклеазы Т7 необходимо тщательно контролировать, чтобы избежать чрезмерно высоких уровней двухцепочечных разрывов.
Шаг 4: включение флуорохрома
ДНК-полимераза используется для включения нуклеотидов, меченных флуорохромом (FdNTP), во множественные участки с разрывом вдоль каждой молекулы ДНК. Во время каждого цикла реакционная смесь содержит один тип FdNTP и допускает множественные добавления этого типа нуклеотидов. Затем выполняются различные промывки для удаления невключенных fdNTP для подготовки к визуализации и следующему циклу добавления FdNTP.
Шаг 5: визуализация
На этом этапе с помощью флуоресцентной микроскопии подсчитывается количество включенных нуклеотидов, меченных флуорохромом, в областях разрыва.
Шаг 6: фотообесцвечивание
Лазерное освещение, которое используется для возбуждения флуорохрома, также используется здесь для уничтожения сигнала флуорохрома. Это по существу сбрасывает счетчик флуорохромов и подготавливает счетчик к следующему циклу. Этот этап является уникальным аспектом оптического секвенирования, поскольку он фактически не удаляет флуорохромную метку нуклеотида после его включения. отказ от удаления флуорохромной метки делает секвенирование более экономичным, но приводит к необходимости последовательного включения флуорохромных меток, что может привести к проблемам из-за громоздкости этикеток.
Шаг 7: повторите шаги 4–6.
Этапы 4-6 повторяются с этапом 4 с использованием реакционной смеси, которая каждый раз содержит другой меченный флуорохромом нуклеотид (FdNTP). Это повторяется до тех пор, пока желаемая область не будет секвенирована.
Стратегии оптимизации
Выбор подходящей ДНК-полимеразы имеет решающее значение для эффективности этапа добавления основания и должен соответствовать нескольким критериям:
- Способность эффективно включать FdNTP в последовательные позиции
- Отсутствие 3'– 5 'экзонуклеазы и активности корректора для предотвращения удаления вновь включенных FdNTP
- Высокая точность для минимизации ошибочного включения
- Хорошая работа с шаблонами, которые прикреплены к поверхностям (например, поверхность для оптического картирования)
Кроме того, различное предпочтение полимеразы для разных флуорохромов, длина линкера на флуорохром-нуклеотидах и состав буфера также являются важными факторами, которые следует учитывать для оптимизации процесса добавления оснований и максимального увеличения числа последовательных включений FdNTP.
Преимущества
Одномолекулярный анализ
Поскольку требуется минимальный образец ДНК, можно избежать трудоемкого и дорогостоящего этапа амплификации, чтобы упростить процесс подготовки образца.
Матрицы больших молекул ДНК (~ 500 кб) по сравнению с матрицами коротких молекул ДНК (<1 кб)В то время как большинство технологий секвенирования следующего поколения нацелены на получение огромных количеств небольших считываний последовательностей, эти считывания небольших последовательностей затрудняют попытки секвенирования de novo и затрудняют понимание повторяющихся участков генома. В оптическом секвенировании для секвенирования используются большие шаблоны молекул ДНК (~ 500 т.п.н.), что дает несколько преимуществ по сравнению с небольшими шаблонами:
- Эти большие ДНК-шаблоны могут быть «закодированы в ДНК», чтобы с уверенностью определять их геномную локализацию. Следовательно, любые считывания последовательности, взятые из большого шаблона, можно с высокой степенью достоверности сопоставить с геномом. Что еще более важно, считывания последовательности из областей с высоким числом повторов могут быть размещены с большей степенью уверенности, тогда как короткие чтения страдают от неопределенности картирования в областях с высоким числом повторов. Специальные алгоритмы и программное обеспечение, такие как оптическое картирование и нанокодирование, были разработаны для совмещения штрих-кодов одиночных молекул с эталонным геномом.
- Несколько последовательностей считываются из одной и той же большой молекулы-шаблона. Эти множественные считывания последовательностей уменьшают сложность сборки de novo, устраняют неоднозначность областей геномной перестройки и «по сути свободны от любых ошибок сборки».[20]
- Молекулярное штрих-кодирование больших молекулярных матриц ДНК с получением последовательностей обеспечивает широкий и специфический геномный анализ
Недостатки
- Секвенирование одиночной молекулы ДНК требует высокого уровня точности, чтобы соответствовать уверенности за счет избыточного покрытия считывания, обеспечиваемого современными технологиями секвенирования следующего поколения.
- Зарубки на обеих цепях в аналогичных положениях, приводящие к низкому уровню матрицы во время синтеза последовательности.
- Нуклеотиды, меченные флуорохромом, не удаляются после включения, и из-за этих объемных меток множественное включение может быть затруднено.
Рекомендации
- ^ Чжоу, Шигуо; Джилл Хершелеб; Дэвид С. Шварц (2007). Единая молекулярная система для анализа всего генома. Новые высокопроизводительные технологии для секвенирования ДНК и геномики. 2. Эльзевир. С. 269–304.
- ^ Schwartz, D. C., et al. «Упорядоченные рестрикционные карты хромосом Saccharomyces Cerevisiae, построенные с помощью оптического картирования». Science 262.5130 (1993): 110–4.
- ^ Рейснер, Вальтер; Ларсен, Нильс Б .; Силахтароглу, Асли; Кристенсен, Андерс; Томмеруп, Нильс; Тегенфельдт, Йонас О .; Фливбьерг, Хенрик (27 июля 2010 г.). «Картирование денатурации одной молекулы ДНК в наножидкостных каналах». Труды Национальной академии наук. 107 (30): 13294–13299. Дои:10.1073 / pnas.1007081107. ISSN 0027-8424. ЧВК 2922186. PMID 20616076.
- ^ Nilsson, Adam N .; Эмильссон, Густав; Ниберг, Лена К .; Благородный, Чарльстон; Стадлер, Лизелотт Свенссон; Фриче, Иоахим; Мур, Эдвард Р. Б.; Тегенфельдт, Йонас О .; Амбьёрнссон, Тобиас (02.09.2014). «Оптическое картирование ДНК на основе конкурентного связывания для быстрой идентификации бактерий - теория матрицы переноса нескольких лигандов и экспериментальные применения на Escherichia coli». Исследования нуклеиновых кислот. 42 (15): e118. Дои:10.1093 / нар / gku556. ISSN 0305-1048. ЧВК 4150756. PMID 25013180.
- ^ Грюнвальд, Ассаф; Дахан, Моран; Гисберц, Анна; Нильссон, Адам; Ниберг, Лена К .; Вайнхольд, Эльмар; Амбьёрнссон, Тобиас; Вестерлунд, Фредрик; Эбенштейн, Юваль (2015-10-15). «Типирование штаммов бактериофагов с помощью экспресс-анализа отдельных молекул». Исследования нуклеиновых кислот. 43 (18): e117. Дои:10.1093 / нар / gkv563. ISSN 0305-1048. ЧВК 4605287. PMID 26019180.
- ^ Вранкен, Шарлотта; Дин, Йохем; Дирикс, Лив; Стакенборг, Тим; Дехаен, Вим; Лин, Фолькер; Хофкенс, Йохан; Нили, Роберт К. (2014-04-01). «Оптическое картирование ДНК сверхвысокого разрешения с помощью химии щелчков ДНК-метилтрансферазы». Исследования нуклеиновых кислот. 42 (7): e50. Дои:10.1093 / nar / gkt1406. ISSN 0305-1048. ЧВК 3985630. PMID 24452797.
- ^ Дималанта, Э. и другие. Микрожидкостная система для больших массивов молекул ДНК. Анальный. Chem. 76 (2004): 5293–5301.
- ^ Джо К. и др. «Система штрих-кодирования одной молекулы с использованием нанощелей для анализа ДНК». Труды Национальной академии наук Соединенных Штатов Америки 104.8 (2007): 2673–8.
- ^ Валуев А., Шварц Д., Чжоу С., Уотерман М.С. «Алгоритм для сборки упорядоченных рестрикционных карт из отдельных молекул ДНК». RECOMB '98: Труды Национальной академии наук Соединенных Штатов Америки 103 (2006): 15770–15775.
- ^ Lai, Z., et al. «Оптическая карта для дробовика всего генома Plasmodium Falciparum». Генетика природы 23.3 (1999): 309–13.
- ^ Lim, A., et al. «Оптические карты дробовика всего генома Escherichia Coli O157: H7». Исследование генома 11.9 (2001): 1584-93.
- ^ Lin, J., et al. «Полногеномное оптическое картирование Deinococcus Radiodurans». Science 285.5433 (1999): 1558–62.
- ^ Нагараджан Н. и др. «Строительные леса и проверка сборок бактериального генома с использованием оптических ограничительных карт». Биоинформатика 24.10 (2008): 1229–35.
- ^ Церковь, Д. и другие. Специфическая биология клонов выявлена с помощью законченной сборки генома мыши. PLoS Biology, 7.5 (2009): e1000112.
- ^ Кидд, Дж. и другие. Картирование и секвенирование структурных вариаций восьми геномов человека. Nature 453 (2008): 56–64.
- ^ Чжоу, С. и другие.Проверка последовательности генома риса с помощью оптического картирования. BMC Genomics 8 (2007): 278.
- ^ Чжоу, С. и другие. Одномолекулярный каркас для генома кукурузы. PLoS Genetics, 5.11 (2009): epub.
- ^ Раманатан А. и др. «Интегративный подход к оптическому секвенированию отдельных молекул ДНК». Аналитическая биохимия 330.2 (2004): 227–41.
- ^ Раманатан, А., Пейпер, Л., и Шварц, Д. К. «Включение нуклеотидов, меченных флуорохромом, с помощью полимеразы высокой плотности». Аналитическая биохимия 337.1 (2005): 1–11.
- ^ а б Чжоу, С., Пейпер, Л., и Шварц, Д. К. «Оптическое секвенирование: сбор данных из нанесенных на карту шаблонов одиночных молекул». Секвенирование генома следующего поколения: к персонализированной медицине. Эд. Михал Яниц. 1-е изд. Вайли-ВЧ, 2008. 133–151.
