Поликрикос - Polykrikos
| Поликрикос | |
|---|---|
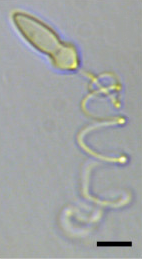 | |
| А световая микрофотография из Polykrikos kofoidii показ экструдированного нематоциста. Масштабная линейка = 10 мкм.[1] | |
| Научная классификация | |
| (без рейтинга): | |
| (без рейтинга): | |
| Тип: | |
| Учебный класс: | |
| Заказ: | |
| Семья: | |
| Род: | Поликрикос |
Поликрикос (от греч. «поли» - много, а «крикос» - кольцо или круг) - один из родов семейства. Polykrikaceae который включает атекатные псевдоколониеобразующие динофлагеллаты. Поликрикос характеризуются сложной баллистической аппаратурой,[2] назвал комплекс нематоциста-тениоциста, который позволяет видам охотиться на множество организмов. Поликрикос было обнаружено, что они регулируют цветение водорослей, поскольку они питаются токсичными динофлагеллятами.[3][4] Тем не менее, есть также некоторые данные о том, что поликрикос токсичен для рыб.[5]
История познания
Поликрикос был впервые замечен в 1868 году Ульяниным и ошибочно считался личинкой многоклеточного животного турбеллярного плоского червя. В 1873 году Бутчили повторно исследовал образец и пришел к выводу, что клетка была необычной инфузорией, а Берг позже, в 1881 году, уточнил. Поликрикос сродство к динофлагеллятам.[6]
Морфология
Поликрикос представляет собой колонию зооидов (единиц колониального организма), которые одновременно выполняют функции целой клетки.
Все Поликрикос виды имеют: 1) слегка изогнутую продольную борозду, борозду, идущую к заднему концу организма 2) петлевидное акробазу, являющееся передним продолжением борозды 3) поперечную борозду, цингулюм, со смещением 4) тениоцисту комплексы нематоцист 5) в два или четыре раза меньше ядер, чем у зооидов, и 6) способность распадаться на псевдоколонии с меньшим количеством зооидов и только одним ядром.[7]
Наиболее отличительной чертой этого рода является образование многоядерных псевдоколоний, состоящих из четного числа зооидов. Каждый зооид имеет пару жгутиков (поперечный и продольный жгутики) и имеет свою поперечную бороздку, цингулюм, но зооидные продольные борозды, борозды, срастаются.[8] Поперечный жгутик имеет общие для других динофлагеллят латеральные выросты, мастигонемы и поперечно-полосатую нить.[9] Часто Поликрикос имеют вдвое меньшее количество ядер, чем зооиды, и каждая пара зооидов разделяет ядро. Внутри группы есть некоторые вариации в том, в каких органеллах представлены, но трихоцисты, нематоцисты, тениоцисты, мукоцисты и пластиды наблюдались у разных членов внутри таксона.[8]
Цитоплазма Поликрикос характеризуется многочисленными грубыми сетками эндоплазматического ретикулума, комплексами Гольджи и вакуолями. Поликрикос Известно, что они производят эжектильные органеллы, экструсомы. Один из них - нематоциста, образовавшаяся в зооидах. Другой экструзом, обнаруженный в организме, представляет собой палочковидную тениоцисту, которая расположена дистальнее нематоцисты и ранее ошибочно считалась предшественником нематоцисты.[10] Вместе эти органеллы образуют комплекс тениоциста-нематоциста, который считается лучшей синапоморфией для Поликрикос клады.[8] Вакуоли, происходящие из Гольджи, являются общими для обеих органелл и снабжают каждую молекулами, необходимыми для ее роста, наряду с участием в артикуляции NTC.[10] Органеллы расположены рядом, но лежат внутри разных мембран и разделены проходом, называемым «желобом». Нематоциста - более крупная органелла, расположенная кзади от тениоцисты. Некоторые недавние исследования [3] показали, что работа двух органелл взаимосвязана: тениоциста прикрепляется к добыче, после чего следует выделение нематоцист, приводящее к прокалыванию добычи и, наконец, извлечение жертвы с помощью жгута нити, расположенного на конце нематоцист рядом с задним пузырьком. Трубочка, заключенная в нематоцисту, отводится к жертве и, как предполагается, будет использоваться для ее прокалывания.
Кроме того, Gavelis et al.[3] глубоко изученная морфология NTC и баллистический механизм, которые, как было показано, фундаментально отличаются от книдарий, демонстрируют, что нематоцисты эволюционировали независимо в одноклеточных динофлагеллатах. Обволакивающая капсула из спиральных канальцев, в отличие от книдарий, запечатана, что заставляет стилет при выстреле сначала прокалывать капсулу изнутри, чтобы высвободить нить, и только потом проткнуть жертву. Когда трубочка проходит через сопло, она открывает жаберную оболочку и затем разматывается. Баллистика нематоцист книдарий обусловлена синтезом осмотического пропеллента полигамма-глутамат-синтазы, PgsAA, в то время как в Поликрикос считается, что это происходит из-за индуцированного давления в результате сокращения капсульного волокна в стенке капсулы.[3]Ядро уникально характеризуется двухслойной фиброзной корой, которая подчеркивает выпяченную ядерную оболочку; Предполагается, что кора головного мозга обеспечивает прочность и форму ядра, в то время как ядерные эвагинации, как полагают, увеличивают площадь ядерно-цитоплазматического обмена в местах перфорации коры.[9]
В Поликрикосчетко определенные фиброзные ленты участвуют в ядерно-жгутиковых связях, и закрепление на жгутичном аппарате может служить для ориентации ядра по отношению к жгутикам во время процессов движения, митоза и деления клеток.[9]
Пластиды
Есть различия в усвоении питательных веществ среди Поликрикос виды, поскольку некоторые полагаются исключительно на фотосинтез, некоторые являются миксотрофами, а некоторые - облигатными гетеротрофами, что делает Поликрикос полезная группа для изучения эволюции органелл. Поликрикоиды раннего ветвления, Polykrikos geminatum и P. hartmanii, имеют трехмембранные пластиды с тройным уложением тилакоидов, что указывает на вторичные пластиды перидининового типа, общие для динофлагеллят. Однако миксотрофный P. lebouriaeфилогенетически гнездится среди гетеротропных поликрикоидов, имеет пластиды, нетипичные для динофлагеллят. Он имеет две мембраны и содержит тилакоиды с двойным слоем, которые встречаются у диатомовых водорослей и гаптофитов. Однако молекулярный анализ данных Gavelis et al.[11] продемонстрировал, что P. lebouriae имеют пластиды перидининового типа, которые, скорее всего, были получены от предковых поликрикоидов. Анализ транскриптомики продемонстрировал множественные потери у поликрикоидов, которые можно объяснить с точки зрения энергетики и физиологических ограничений. Постепенное увеличение размера Поликрикос делает эти организмы великими хищниками, но, как известно, увеличение размеров отдельных клеток приводит к увеличению самозатенения хлоропластов и уменьшению отношения площади поверхности к объему, что приводит к снижению эффективности фотосинтеза. Наличие специализированных NTC и большой размер клеток могли вызвать множественные потери фотосинтеза.[11]
Жизненный цикл P. kofoidii
Для рода Поликрикос, имеются подробные данные о воспроизводстве типового вида (голотипа) P. kofoidii, жизненный цикл которого напоминает общий цикл динофлагеллат, поскольку вегетативные клетки образуют гаметы, которые сливаются, образуя диплоидную (2n) зиготу, которая может энцистировать, но псевдоколониальная природа добавляет ряд особенностей к Поликрикос разработка.[12]
Когда организмы были сыты, они выглядели как псевдоколонии 4-зооид-2-ядер, а во время вегетативного размножения удвоилось количество зооидов с последующим делением ядер, приводящим к стадии 8-зооид-4-ядер с дальнейшим поперечным бинарным делением на два 4-ядерных. зооид-2-ядра Поликрикос. Формирование гамет было особым, поскольку псевдоколония продуцирует 4 гаметы разного размера и морфологии, чем вегетативные клетки. Вегетативная форма удвоила зооиды и впоследствии разделилась на четыре гаметы формы 2-зооид-1-ядро. Две гаметы соединились с брюшной стороной и слились, образуя планозиготу. За P. kofoidii две структуры в форме пальца копуляции наблюдались в гаметах, которые предположительно участвуют в контакте и слиянии гамет, но необходимы дополнительные данные, чтобы подтвердить это. Слившиеся вентрально гаметы потребовали сложной перестройки восьми жгутиков и образования бороздок и цингули. У 4-зооидной планозиготы было только одно ядро и два пути развития в зависимости от доступности пищи. В условиях голодания планозигота распалась на два 2-зооида с одним недостающим ядром, но дальнейшая судьба не исследовалась. В условиях культивирования большинство организмов претерпело мейоз и непосредственно вступило в вегетативный цикл. Очень немногие планозиготы прошли стадию кисты покоя. Стадия кисты сохранялась в течение 1 месяца, что считается относительно коротким периодом по сравнению с другими динофлагеллятами, у которых период облигатного покоя может достигать 6 месяцев. Продолжительность инцистирования связана с экологическими стратегиями поиска пищи. Короткий период покоя может способствовать быстрой смене стадий жизненного цикла, что может быть полезно для гетеротрофных видов в случае колебаний доступности пищи. Однако возможность передачи химических сигналов, участвующих в вылуплении кисты для Поликрикос еще предстоит определить.
Росток, единственная зооидная клетка, выходящая из цисты, имела уникальное развитие, которое никогда не было зарегистрировано ни для одной свободноживущей динофлагелляты. Его морфология явно перешла от ядра 1-зооид-1, ядра 2-зооид-1 и ядра 4-зооид-1 к стадии ядра 4-зооид-2. Эти данные вызывают вопрос, может ли такая штриховка отражать Поликрикос Филогения псевдоколоний.[12]
Среда обитания и экология (ниша, еда)
Все известные Поликрикос виды встречаются в морской среде. Большинство видов являются планктонными, за исключением Polykrikos lebouriae и Polykrikos herdmanae которые встречаются в донной среде обитания.[7]Существует также различие в экологии кормления, поскольку некоторые виды имеют пластиды и могут использовать фотосинтез для получения питательных веществ, но часто оказываются миксотрофами (P. barnegatensis, P. lebouriae, P. tanit, P. hartmannii). Только один вид известен как исключительно автотрофный (P. geminatum), а некоторые лишены пластиды и полностью гетеротрофны (P. grassei, P. herdmanae, P. kofoidii и P. schwartzii),.[13][8]
Polykrikos hartmannii является фототрофной динофлагеллатой, о которой сообщалось в водах Канады,[14] США, Мексика, Китай, Индия, Япония, Корея.[5][13] P. hartmanii питается видами водорослей путем поглощения после закрепления жертвы с помощью комплекса нематоциста-тениоциста (позже именуемого NTC).[13] Tang et al.[5] наблюдаемый P. hartmannii цветение, вызвавшее 100% гибель молоди гольянов (Ципринодон пестрый) в течение 24 часов, предлагая P. hartmannii это ихтиотоксичная, вредная водоросль. P.hartmannii питается цепочечными динофлагеллятами Cochlodinium polykrikoides и Gymnodinium catenatum которые, как известно, вызывают гибель рыб, и, следовательно, P. hartmannii считается, что у них есть ферменты, которые выводят токсины, вырабатываемые этими жертвами динофлагеллят.[13] Также сравнение трех Поликрикос кормление видов показало, что виды различаются по предпочтениям добычи, и некоторые из них более специализированы, чем другие, так что P. hartmanii добыча менее разнообразна (питается 2 видами добычи), чем P. kofoidii и P. lebouriae, который питался 14 различными видами водорослей.[13]
Хищничество гетеротрофными Поликрикос стал очень интересной темой, поскольку некоторые организмы питаются динофлагеллятами, вызывающими токсичное цветение. Высокая степень хищничества со стороны Polykrikos schwartzii Бучили о токсичной динофлагеллате Александрий тамаренс (Лебур) Балех был зарегистрирован в Аргентине, в то время как Polykrikos kofoidii Чаттон контролировал Gymnodium catenatum Грэхем в португальских и японских прибрежных водах.[4] G. catenatum является одним из видов, вызывающих паралитическое отравление моллюсками (PSP), и встречается в водах Австралии, Японии, Мексики и Испании.[15] Наблюдения за пищевым поведением предполагают P. kofoidii первоначально демонстрировал плавание по петле в непосредственной близости от жертвы, за которым следовало выделение нематоцисты, втягивание жертвы в тело через заднюю борозду и окончательное поглощение жертвы.[16]PSP вызывает социально-экономические и экологические проблемы, поскольку влияет на здоровье как морских млекопитающих, так и людей, а также на механизм регулирования популяции токсичных микроводорослей посредством P.kofoidii может иметь важное значение для мониторинга окружающей среды и устранения опасности для здоровья.
Практическое значение
Поедание токсичных микроводорослей гетеротрофными динофлагеллятами является одним из факторов, контролирующих цветение водорослей. Поликрикос как известно, модулируют популяции динофлагеллят, таких как Александрий тамаренс,[3][4] и G. catenatum,[17] которые являются одними из распространенных возбудителей токсичного цветения водорослей. Такие гетеротрофные поликрикоиды могут не только снижать уровни токсичности, вызываемой их добычей в морских пищевых сетях, но также могут прекращать токсичное цветение и могут использоваться для биоремедиации.[17] Таким образом, снижение токсичности воды может помочь регулировать баланс морских пищевых сетей и снизить уровень смертности рыб, морских млекопитающих и морских птиц. Дальнейшие исследования молекулярных механизмов детоксикации Поликрикос может быть полезным в области биомедицины и мониторинга окружающей среды.
Однако некоторые Поликрикос представляют опасность для здоровья некоторых рыб, в то время как рыбы, регулирующие цветение, часто становятся жертвами морских беспозвоночных, таких как амфиподы, который вернет токсины обратно в пищевую сеть.[17] Мониторинг популяции поликрикоидов и исследование динамики токсинов внутри тела травоядных могут обеспечить лучшее понимание пищевых сетей, основанных на планктоне, оценить степень отравления в экосистемах и предложить потенциальные пути выведения токсинов.
Список видов
В настоящее время таксономически приняты следующие 10 видов: Polykrikos barnegatensis Г. В. Мартин, Polykrikos geminatus (Ф.Шютт) Д. X. Цю и Сенджи Линь, Polykrikos grassei Лекаль, Polykrikos hartmannii В. Циммерманн,Polykrikos herdmaniae Хоппенрат и Леандер,Polykrikos kofoidii Чаттон,Polykrikos lebouriae Хердман, Polykrikos schwartzii Бючли, Поликрикос танит Рене,Polykrikos tentaculatus О. Ветцель [18]
Рекомендации
- ^ Хоппенрат, Мона; Бачварофф Цветан Р; Хэнди, Сара М; Delwiche, Charles F; Леандер, Брайан S (2009). «Молекулярная филогения динофлагеллят, содержащих оцеллоиды (Warnowiaceae), на основе последовательностей рДНК SSU и LSU». BMC Эволюционная биология. 9: 116. Дои:10.1186/1471-2148-9-116. ЧВК 2694157. PMID 19467154.
- ^ Джеймс Горман (31 марта 2017 г.). "Первый ясный вид одноклеточного гарпунера в действии". NYTimes.com. Получено 26 декабря 2017.
- ^ а б c d е Gavelis, G .; Wakeman, K .; Ripken, C .; Озебек, С .; Holstein, T .; Herranz, M .; Keeling, P .; Леандер, Б. (2017). «Гонка микробных вооружений: баллистические нематоцисты» в динофлагеллятах представляют собой новую крайность в сложности органелл ». Достижения науки. 3 (3): e1602552. Дои:10.1126 / sciadv.1602552. ЧВК 5375639. PMID 28435864.
- ^ а б c Nagai, S .; Matsuyama, Y .; Такаяма, H .; Котани, Ю. (2002). «Морфология Polykrikos kofoidii и P. schwartzii (Dinophyceae, Polykrikaceae) цисты, полученные в культуре ». Phycologia. 41 (4): 319. Дои:10.2216 / i0031-8884-41-4-319.1.
- ^ а б c Tang, Y.Z .; Harke, M.J .; Гоблер, Си Джей (2013). «Морфология, филогения, динамика и ихтиотоксичность Pheopolykrikos hartmannii (Dinophyceae) изолируется и цветет из Нью-Йорка, США ». Дж. Фикол. 49 (6): 1084–1094. Дои:10.1111 / иен.12114.
- ^ Тейлор, Ф. Дж. Р. (1987). «Биология динофлагеллят». Биологические монографии. 21.
- ^ а б Hoppenrath, M .; Леандер, Б. (2007b). «Морфология и филогения псевдоколониальных динофлагеллят. Polykrikos lebourae и Polykrikos herdmanae п. sp ". Протист. 158: 209–227. Дои:10.1016 / j.protis.2006.12.001.
- ^ а б c d Hoppenrath, M .; Леандер, Б. С. (2007a). «Эволюция характера поликрикоидных динофлагеллят». Дж. Фикол. 43: 366–377. Дои:10.1111 / j.1529-8817.2007.00319.x.
- ^ а б c Bradbury, P.C .; Westfall, J.A .; Таунсенд, Дж. (1983). «Ультраструктура динофлагелляты Поликрикос. Ядро и его связи с жгутиковым аппаратом ». Журнал исследований ультраструктуры. 85 (1): 24–32. Дои:10.1016 / с0022-5320 (83) 90113-2. PMID 6686618.
- ^ а б Westfall, J. A .; Bradbury, P.C .; Таунсенд, Дж. (1983). «Ультраструктура динофлагелляты Поликрикос. Развитие комплекса нематоциста-тениоциста и морфология участка экструзии ». J Cell Sci. 63: 245–261.
- ^ а б Gavelis, G .; Уайт, Р. А .; Suttle, C.A .; Килинг, П. Дж .; Леандер, Б. С. (2015). «Транскриптомика единичных клеток с использованием сплайсированной лидерной ПЦР: доказательства множественных потерь фотосинтеза у поликрикоидных динофлагеллятов». BMC Genomics. 16 (1). Дои:10.1186 / s12864-015-1636-8. ЧВК 4504456. PMID 26183220.
- ^ а б Tillmann, U .; Хоппенрат, М. (2013). "Жизненный цикл псевдоколониальной динофлагелляты Polykrikos kofoidii (Gymnodiniales, Dinoflagellata) ". Журнал психологии. 49 (2): 298. Дои:10.1111 / jpy.12037. PMID 27008517.
- ^ а б c d е Ли, М. Дж .; Jeong, H.J .; Lee, K. H .; Jang, S. H .; Kim, J. H .; Ким, К. Ю. (2015). "Миксотрофия в фототрофной динофлагеллате, несущей комплекс нематоциста-тениоциста. Polykrikos hartmannii". Вредные водоросли. 49: 124–132. Дои:10.1016 / j.hal.2015.08.006.
- ^ Hoppenrath, M .; Yubuki, N .; Бахварофф, С .; Леандер, Б. С. (2010). "Реклассификация Pheopolykrikos hartmannii в качестве Поликрикос (Dinophyceae) частично на основе ультраструктуры сложных экструзом ». Europ. J. Protistol. 46: 29–37. Дои:10.1016 / j.ejop.2009.08.003. PMID 19767184.
- ^ Мацуяма, Y; Миямото, М; Kotani, Y (1999). «Выпас гетеротрофной динофлагелляты. Polykrikos kofoidii на цветке Gymnodinium catenatum". Aquat Microb Ecol. 17: 91–98. Дои:10.3354 / ame017091.
- ^ Мацуока, К .; Cho, H.J .; Якобсон, Д. М. (2000). «Наблюдение за питанием и скоростью роста гетеротрофной динофлагелляты, Polykrikos kofoidii (Polykrikaceae. Dinophyceae) 39: 82-86 ". Phycologia. 39: 82–86. Дои:10.2216 / i0031-8884-39-1-82.1.
- ^ а б c Jeong, H .; Парк, К .; Kim, J .; Kang, H .; Kim, C .; Чой, H., ...; Парк, М. (2003). "Снижение токсичности динофлагеллат Gymnodinium catenatum при питании гетеротрофной динофлагеллатой Polykrikos kofoidii". Экология водных микробов. 31: 307–312. Дои:10.3354 / ame031307.
- ^ Гири, М.Д. "Поликрик Бучли, 1873 г.". Водоросли. Получено 20 февраля, 2017.
