Виром - Virome
Виром относится к скоплению вирусов [1][2] который часто исследуют и описывают с помощью метагеномного секвенирования вирусных нуклеиновых кислот. [3] которые обнаружены связанными с конкретной экосистемой, организмом или холобионт. Это слово часто используется для описания окружающей среды. вирусные метагеномы дробовика. Вирусы, в том числе бактериофаги, встречаются во всех средах, и исследования вирома дали представление о круговороте питательных веществ,[4][5] развитие иммунитета,[6] и главный источник генов через лизогенная конверсия.[7]
История
Первые всесторонние исследования виромов были проведены с помощью секвенирования сообществ.[8] что часто называют метагеномикой. В 2000-х годах лаборатория Rohwer секвенировала виромы из морской воды,[8][9] морские отложения,[10] стул взрослого человека,[11] детский стул человека,[12] почва,[13] и кровь.[14] Эта группа также выполнила первый РНК-виром с сотрудниками из Геномного института Сингапура.[15] Из этих ранних работ был сделан вывод, что большая часть геномного разнообразия содержится в глобальном вироме и что большая часть этого разнообразия остается не охарактеризованной.[16] Эта точка зрения была поддержана проектом индивидуального секвенирования генома, в частности фага микобактерий.[17]
Методы исследования
Для изучения вирома вирусоподобные частицы отделяют от клеточных компонентов, обычно используя комбинацию фильтрации, центрифугирования по плотности и ферментативной обработки, чтобы избавиться от свободных нуклеиновых кислот.[18] Затем нуклеиновые кислоты секвенируют и анализируют с использованием метагеномный методы. В качестве альтернативы, есть недавние вычислительные методы, которые используют непосредственно метагеномные собранные последовательности для обнаружения вирусов.[19]
Global Ocean Viromes (GOV) - это набор данных, состоящий из глубокое секвенирование из более чем 150 образцов, собранных в Мировом океане за два периода исследований международной группой.[20]
Хосты вирусов

Вирусы - самые распространенные биологические объекты на Земле, но проблемы с обнаружением, изоляцией и классификацией неизвестных вирусов не позволяют провести исчерпывающие исследования глобального вирома.[21] Более 5 ТБ метагеномный Для оценки глобального распространения, филогенетического разнообразия и специфичности вирусов к хозяевам были использованы данные о последовательностях из 3042 географически различных образцов.[21]

В августе 2016 года более 125000 частичных ДНК-вирусных геномов, включая самый крупный из выявленных фагов, увеличили количество известных вирусных генов в 16 раз.[21] Набор вычислительных методов использовался для идентификации предполагаемых соединений с хост-вирусами.[21] Информация о вирусном хозяине изолята была перенесена на группу, в результате чего были назначены хозяева для 2,4% вирусных групп.[21]
Тогда CRISPR –Как прокариотическая иммунная система, которая содержит «библиотеку» фрагментов генома фагов (прото-спейсеров), которые ранее инфицировали хозяина.[21] Спейсеры из изолированного микробного генома с совпадениями метагеномный вирусные контиги (mVC) были идентифицированы для 4,4% вирусных групп и 1,7% синглетонов.[21] Была исследована гипотеза о том, что гены вирусной транспортной РНК (тРНК) происходят от хозяина.[21]
Вирусные тРНК, идентифицированные в 7,6% мВК, были сопоставлены для выделения геномов одного вида или рода.[21] Специфичность отнесения вирусов-хозяев на основе тРНК была подтверждена совпадениями спейсеров CRISPR – Cas, показывающими 94% совпадение на уровне рода. Эти подходы идентифицировали 9992 предполагаемых ассоциации хозяин-вирус, позволяющих назначать хозяина 7,7% mVCs.[21] Большинство этих соединений были ранее неизвестны и включают хозяев из 16 прокариотических типов, для которых ранее не были идентифицированы вирусы.[21]
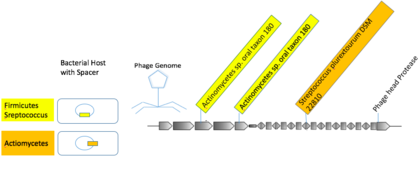
Многие вирусы специализируются на заражении связанных хостов.[21] Могут существовать универсальные вирусы, которые заражают хозяев в разных таксономических отрядах.[21] Большинство совпадений спейсеров CRISPR происходило от вирусных последовательностей к хозяевам в пределах одного вида или рода.[21] Некоторые mVC были связаны с несколькими хозяевами из более высоких таксонов. Вирусная группа, состоящая из макинтошей из образцов ротовой полости человека, содержала три отдельных фото-спейсера с почти точным соответствием спейсерам в Действиебактерии и Фирмикуты.[21]
В январе 2017 года система IMG / VR [22] - крупнейшая интерактивная общедоступная вирусная база данных, содержащая 265 000 метагеномных вирусных последовательностей и выделенных вирусов. В ноябре 2018 года это число выросло до 760 000 (IMG / VR v.2.0).[23] Системы IMG / VR служат отправной точкой для анализа последовательности вирусных фрагментов, полученных из метагеномных образцов.
использованная литература
- ^ Андерсон, Норман Дж. Герин, Джон Л; Андерсон, Н Ли (2003). «Глобальный скрининг вирусных патогенов человека». Возникающие инфекционные заболевания. 9 (7): 768–773. Дои:10.3201 / eid0907.030004. ЧВК 3023425. PMID 12890315.
- ^ Zárate, S; Табоада, B; Yocupicio-Monroy, M; Ариас, CF (2017). «Виром человека». Архив медицинских исследований. 48 (8): 701–716. Дои:10.1016 / j.arcmed.2018.01.005.
- ^ McDaniel, L; Брейтбарт, М.; Мобберли, Дж; Лонг, А; Хейнс, М; Rohwer, F; Пол, JH (23 сентября 2008 г.). «Метагеномный анализ лизогении в заливе Тампа: значение для экспрессии гена профага». PLOS ONE. 3 (9): e3263. Дои:10.1371 / journal.pone.0003263. ЧВК 2533394. PMID 18810270.
- ^ Вильгельм, Стивен У .; Саттл, Кертис А. (1999). «Вирусы и круговорот питательных веществ в море». Бионаука. 49 (10): 781–788. Дои:10.2307/1313569. ISSN 1525-3244. JSTOR 1313569.
- ^ Wegley, L; Эдвардс, Р. Родригес-Брито, B; Лю, H; Rohwer, F (ноябрь 2007 г.). «Метагеномный анализ микробного сообщества кораллов Porites astreoides». Экологическая микробиология. 9 (11): 2707–19. Дои:10.1111 / j.1462-2920.2007.01383.x. PMID 17922755.
- ^ Барр, JJ; Auro, R; Фурлан, М; Whiteson, KL; Erb, ML; Pogliano, J; Стотланд, А; Wolkowicz, R; Раскрой, AS; Доран, KS; Salamon, P; Юл, М; Ровер, Ф (25 июня 2013 г.). «Бактериофаг, прилипший к слизи, обеспечивает иммунитет, не связанный с хозяином». Труды Национальной академии наук Соединенных Штатов Америки. 110 (26): 10771–6. Дои:10.1073 / pnas.1305923110. ЧВК 3696810. PMID 23690590.
- ^ Шарон, я; Батчикова, Н; Аро, EM; Giglione, C; Meinnel, T; Glaser, F; Пинтер, шт. Breitbart, M; Rohwer, F; Бежа, О. (июль 2011 г.). «Сравнительная метагеномика микробных признаков в океанических вирусных сообществах». Журнал ISME. 5 (7): 1178–90. Дои:10.1038 / ismej.2011.2. ЧВК 3146289. PMID 21307954.
- ^ а б Breitbart, M; Salamon, P; Андресен, B; Mahaffy, JM; Сегал, AM; Я добавил; Азам, Ф; Rohwer, F (29 октября 2002 г.). «Геномный анализ некультивируемых морских вирусных сообществ». Труды Национальной академии наук Соединенных Штатов Америки. 99 (22): 14250–5. Дои:10.1073 / pnas.202488399. ЧВК 137870. PMID 12384570.
- ^ Энгли, ИП; Войлок, B; Breitbart, M; Salamon, P; Эдвардс, РА; Карлсон, К; Чан, AM; Хейнс, М; Келли, S; Лю, H; Mahaffy, JM; Мюллер, JE; Нултон, Дж; Олсон, Р. Парсонс, Р. Rayhawk, S; Саттл, Калифорния; Ровер, Ф (ноябрь 2006 г.). «Морские виромы четырех океанических регионов». PLOS Биология. 4 (11): e368. Дои:10.1371 / journal.pbio.0040368. ЧВК 1634881. PMID 17090214.
- ^ Breitbart, M; Войлок, B; Келли, S; Mahaffy, JM; Нултон, Дж; Salamon, P; Rohwer, F (22 марта 2004 г.). «Разнообразие и популяционная структура вирусного сообщества прибрежных морских отложений». Труды Королевского общества B: биологические науки. 271 (1539): 565–74. Дои:10.1098 / rspb.2003.2628. ЧВК 1691639. PMID 15156913.
- ^ Breitbart, M; Хьюсон, я; Войлок, B; Mahaffy, JM; Нултон, Дж; Salamon, P; Rohwer, F (октябрь 2003 г.). «Метагеномный анализ некультивируемого вирусного сообщества из человеческих фекалий». Журнал бактериологии. 185 (20): 6220–3. Дои:10.1128 / jb.185.20.6220-6223.2003. ЧВК 225035. PMID 14526037.
- ^ Breitbart, M; Хейнс, М; Келли, S; Angly, F; Эдвардс, РА; Войлок, B; Mahaffy, JM; Мюллер, Дж; Нултон, Дж; Rayhawk, S; Родригес-Брито, B; Salamon, P; Ровер, Ф (июнь 2008 г.). «Вирусное разнообразие и динамика в кишечнике младенца». Исследования в области микробиологии. 159 (5): 367–73. Дои:10.1016 / j.resmic.2008.04.006. PMID 18541415.
- ^ Фирер, N; Breitbart, M; Нултон, Дж; Salamon, P; Лозупон, С; Джонс, Р. Робсон, М; Эдвардс, РА; Войлок, B; Rayhawk, S; Рыцарь, R; Rohwer, F; Джексон, РБ (ноябрь 2007 г.). «Метагеномный анализ и анализ малых субъединиц рРНК выявляют генетическое разнообразие бактерий, архей, грибов и вирусов в почве». Прикладная и экологическая микробиология. 73 (21): 7059–66. Дои:10.1128 / aem.00358-07. ЧВК 2074941. PMID 17827313.
- ^ Breitbart, M; Ровер, Ф (ноябрь 2005 г.). «Метод обнаружения новых ДНК-вирусов в крови с использованием отбора вирусных частиц и секвенирования дробовиком». Биотехнологии. 39 (5): 729–36. Дои:10.2144/000112019. PMID 16312220.
- ^ Чжан, Т; Breitbart, M; Ли, WH; Беги, JQ; Wei, CL; Сох, ЮЗ; Хибберд, ML; Лю, ET; Rohwer, F; Руан, Й (январь 2006 г.). «Вирусное сообщество РНК в человеческих фекалиях: преобладание патогенных вирусов растений». PLOS Биология. 4 (1): e3. Дои:10.1371 / journal.pbio.0040003. ЧВК 1310650. PMID 16336043.
- ^ Эдвардс, РА; Ровер, Ф (июнь 2005 г.). «Вирусная метагеномика». Обзоры природы. Микробиология. 3 (6): 504–10. Дои:10.1038 / nrmicro1163. PMID 15886693.
- ^ Ровер, Ф (18 апреля 2003 г.). «Глобальное разнообразие фагов». Ячейка. 113 (2): 141. Дои:10.1016 / s0092-8674 (03) 00276-9. PMID 12705861.
- ^ Thurber, RV; Хейнс, М; Breitbart, M; Wegley, L; Ровер, Ф (2009). «Лабораторные процедуры для создания вирусных метагеномов». Протоколы природы. 4 (4): 470–83. Дои:10.1038 / nprot.2009.10. PMID 19300441.
- ^ Паез-Эспино Д., Павлопулос Г.А., Иванова Н.Н., Кирпидес NC (август 2017 г.). «Конвейер обнаружения ненаправленных вирусных последовательностей и кластеризация вирусов для метагеномных данных». Нат Проток. 12 (8): 1673–1682. Дои:10.1038 / nprot.2017.063. PMID 28749930.
- ^ Тан, Лэй (июль 2019 г.). "Межполярные океанические виромы". Основные моменты исследования. Природные методы (Бумага). 16: 575. Дои:10.1038 / s41592-019-0480-1. - через Springer Nature (требуется подписка)
- ^ а б c d е ж г час я j k л м п о Паез-Эспино Д., Элоэ-Фадрош Е.А., Павлопулос Г.А., Томас А.Д., Хантеманн М., Михайлова Н., Рубин Е., Иванова Н.Н., Кирпидес Н.К. (август 2016 г.). «Открытие вирома Земли». Природа. 536 (7617): 425–30. Дои:10.1038 / природа19094. PMID 27533034.
- ^ Паез-Эспино Д., Чен И.А., Паланиаппан К., Ратнер А., Чу К., Сзето Э. и др. (Январь 2017 г.). «IMG / VR: база данных культивируемых и некультивируемых ДНК-вирусов и ретровирусов». Нуклеиновые кислоты Res. 45 (D1): D457 – D465. Дои:10.1093 / нар / gkw1030. ЧВК 5210529. PMID 27799466.
- ^ Паез-Эспино Д., Ру С., Чен И.А., Паланиаппан К., Ратнер А., Чу К. и др. (2019). «IMG / VR v.2.0: интегрированная система управления и анализа данных для культивируемых и экологических вирусных геномов». Нуклеиновые кислоты Res. 47 (Проблема с базой данных): D678 – D686. Дои:10.1093 / нар / gky1127. ЧВК 6323928. PMID 30407573.
