Адсорбируемые органические галогениды - Adsorbable organic halides
Адсорбируемые органические галогениды (AOX) - это мера содержания органических галогенов в месте отбора проб, например в почве от свалки, в воде или сточных водах.[1] Процедура меры хлор, бром, и йод как эквивалентные галогены, но не измеряет уровни фтора в образце.[2]
Фон
Использование галогенсодержащих материалов в таких процессах, как очистка воды, отбеливание или даже общий синтез для создания конечного продукта, приводит к образованию ряда органических галогенидов. Эти органические галогениды выделяются со сточными водами нефтяной, химической и бумажной промышленности.[1] и попадают к потребителю, а в конечном итоге на свалки или океанические свалки. Внутри почвы соединения гало сопротивляются разложению и часто вступают в реакцию с ионами металлов, в результате чего образуются неразлагаемые комплексы металлов, повышается токсичность почвы и накапливается в пищевой цепи водных организмов.[3] До 2000 ppm этих биоаккумулятивных органических хлоридов было обнаружено в жире рыбы из вод, куда отбеливающие стоки сбрасывались бумажными фабриками.[4] где концентрация воды 2% считается токсичной для рыб.[5] Хотя строгие правительственные постановления позволили снизить высокий уровень выбросов в прошлом, эти соединения попадают в источники воды из-за неправильной утилизации потребителями предметов, содержащих хлорированные соединения.[нужна цитата ] Присутствие любых органических галогенидов в природной воде считается признаком загрязнения ксенобиотики.[6] Попадая в воду, естественные фульвокислоты и гуминовые кислоты может привести к образованию мутагенный соединения, такие как галогенированный фуранон MX (Z-3-хлор-4- (дихлорметил) -5-гидрокси-2 (5H) -фуранон).[7] Потребление этих мутагенный Соединения могут вызывать некоторые нарушения в развитии и воспроизводстве у людей из-за длительного периода полураспада и имитации рецепторов гормонов. Например, такие соединения, как диоксины может подавлять действие половых гормонов, связываясь со стероидными рецепторами, вызывая длительное разрушение клеток в некоторых тканях.[7]
Определение АОХ
Стойкие органические загрязнители, такие как дихлордифенилтрихлорэтан (ДДТ), полихлорированные бифенолы, диоксины, все оцениваются в анализе AOX. Как правило, чем выше количество хлора в органическом соединении, тем оно считается более токсичным.[8] Хотя существует несколько биохимических или электрохимических методов удаления органических галогенидов, предпочтение отдается АОХ из-за его низкой стоимости эксплуатации и простоты конструкции.[1]
В лаборатории определение параметра AOX заключается в адсорбции органических галогенидов из образца на Активированный уголь.[6] Активированный уголь можно порошкообразный[9] или гранулированный[6] и адсорбируется с помощью микроколонок[9] или пакетный процесс, если образцы богаты гуминовые кислоты.[нужна цитата ] В случае периодического процесса часто используется интенсивное встряхивание, чтобы способствовать адсорбции органического галогенида на активированном угле из-за его электроотрицательности и наличия неподеленных пар. Неорганические галогениды, которые также адсорбируются, вымываются сильной кислотой, такой как азотная кислота.[6] Уголь с адсорбированным органическим галогенидом получают фильтрованием, после чего фильтр, содержащий уголь, сжигают в присутствии кислорода. При сгорании углеводородной части соединений образуется CO2 и H2О, галогеновые кислоты образуются из галогенов. Эти галогенкислоты поглощаются уксусной кислотой. Последующее использование микроколуметрического титрования, электрохимического метода количественного определения, позволяет определить содержание АОХ в образце. Используя коэффициент разбавления, можно оценить общее содержание АОХ на участке.[10] В качестве альтернативы, хлорированные соединения в образце можно определить с помощью пентан экстракция с последующим капиллярным газовая хроматография и захват электронов (GC-ECD ).[6] Органический углерод, оставшийся после продувки азотной кислотой, может быть проанализирован с использованием влажного окисления УФ-персульфатом с последующим инфракрасным обнаружением (ИК ).[6] Несколько других аналитических методов, таких как высокоэффективная жидкостная хроматография (ВЭЖХ) также может быть реализовано для количественной оценки уровней АОХ.[1] Генерал адсорбция процедура приведена ниже:
Где это активированный уголь и любой органический галогенид.
представляет собой комплекс органического галогенида и активированного угля, который можно отфильтровать.
Уход
Физическое разделение
На водоочистных сооружениях органические галогениды адсорбируются с помощью GAC или PAC в танках с волнением.[6] Загруженный углерод отделяется с помощью мембраны из таких материалов, как полипропилен. [9] или нитрат целлюлозы.[1] Измерение уровней АОХ в зоне обработки и за ее пределами показывает падение концентрации органических галогенидов. Некоторые процессы используют двухэтапный GAC фильтрация для удаления прекурсоров АОХ и, таким образом, уменьшения количества АОХ в очищенной воде.[11] Двухступенчатый процесс фильтрации состоит из двух последовательно соединенных фильтров GAC. В первый фильтр загружается отработанный GAC, а во второй фильтр - свежий GAC. Такая установка предпочтительна из-за ее повышенной эффективности и пропускной способности. GAC заменяется циклически, а затем извлеченная смесь галогенида и углерода направляется на последующую биологическую или химическую обработку, такую как озонирование для регенерации GAC.[1][11] Часто эти химические обработки, хотя и эффективны, создают экономические проблемы для очистных сооружений.
Биологическое лечение
Более экономически привлекательным вариантом обработки органических галогенидов является использование биологических агентов. В последнее время бактерии (Ancylobacter aquaticus), грибы (Phanerochaete chrysosporium и Койриолус разноцветный), или синтетические ферменты были использованы при разложении хлорированных органических соединений.[3] Микроорганизмы разлагают галогенсодержащие соединения с использованием аэробных или анаэробных процессов. Механизмы разложения включают использование соединения в качестве источника углерода для получения энергии, кометаболита или в качестве акцептора электронов.[3][8] Обратите внимание, что ферментативное или микробное действие можно регулировать посредством ингибирования с обратной связью - конечный продукт в серии подавляет реакцию в процессе. Пример микроба, который может разлагать АОХ, показан на рисунках 1 ниже.[12] и 2.[13]
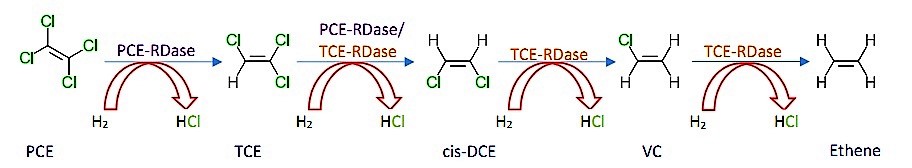
Образец дехлорирования хлорированных алифатических углеводородов (ХАУ), таких как перхлорэтилен (PCE) автор: Dehalococcoides ethenogenes проиллюстрировано выше. PCE - один из сильно хлорированных CAH, в котором отсутствуют известные микроорганизмы, способные к аэробному разложению.[12] Высота электроотрицательный Характер PCE предоставляет возможности окислителя за счет принятия электронов путем совместного метаболизма или дегалоидыхания. При совместном метаболизме снижение PCE становится возможным за счет использования основного метаболита для получения углерода и источника энергии. При дегалоидыхании перенос электронов в результате окисления малых молекул (H2 является основным источником; но также можно использовать глюкозу, ацетат, формиат и метанол), чтобы PCE генерировал энергию, необходимую для роста бактерий. Водород, участвующий в этом механизме, часто является продуктом другого процесса, такого как ферментация простых молекул, таких как сахара, или других сложных молекул, таких как жирные кислоты.[12] Более того, из-за конкуренции со стороны метаногены для ч2, низкий H2 концентрациям благоприятствует дехлорирование бактерий и часто достигается за счет ферментационных соединений с медленным высвобождением, таких как жирные кислоты и разлагающаяся бактериальная биомасса.[14] В то время как несколько ферментов и переносчиков электронов участвуют в процессе, два фермента выполняют реакции дехлорирования - редуктивная дегидрогеназа PCE (PCE-RDase) и TCE-редуктивная дегидрогеназа (TCE-RDase). PCE-RDase обычно свободно находится в цитоплазме, в то время как TCE-RDase находится прикрепленной к внешней цитоплазматической мембране. Эти ферменты обычно используют кластер ионов металла, такой как кластер Fe-S, для завершения цикла переноса электрона.[12] Водород окисляется с образованием двух протонов и двух электронов. Удаление первого хлорида, которое выполняется PCE-RDase, снижает PCE в TCE путем восстановительного дегалогенирования, когда гидрид заменяет хлор. Хлорид, потерянный из PCE, приобретает два электрона и протон, который их сопровождает, с образованием HCl. TCE можно сократить до СНГ-дихлорэтен (cis-DCE) с помощью PCE-RDase или TCE-RDase. Последующие сокращения до винилхлорид (VC) и этилен выполняются TCE-RDase. Дехлорирование PCE до цис-DCE происходит быстрее и термодинамически более выгодно, чем дехлорирование цис-DCE до VC. Превращение ВК в этилен является самой медленной стадией процесса и, следовательно, ограничивает общую скорость реакции.[14] Скорость восстановительного дехлорирования также напрямую коррелирует с количеством атомов хлора и, как таковая, уменьшается с уменьшением количества атомов хлора.[14] Кроме того, в то время как несколько групп бактерий, таких как Десульфомонил, Dehalobacter, Десульфуромонады...так далее. может выполнить дегалогенирование PCE в TCE, только Dehalococcoides группа может выполнить полное восстановительное дехлорирование из PCE к этен.[14]

Сообщается, что помимо дехлорирования CAH, микробы действуют на хлорированные ароматические углеводороды. Пример реакции, в которой было снижено содержание ароматических АО, показан на рисунке 2 выше.[8][15] Хотя мало что известно о механизмах дегалогенирования полигалогенированных фенолов (PHP) и полигалогенированных бензолов (PHB), наблюдалась региоселективность в отношении расположения галогенидов на ароматическом кольце.[8][14] Однако в этой региоселективности доминируют как окислительно-восстановительные потенциалы реакции, так и знакомство микробов с реакцией.[12] Более того, из-за специфичности большинства микробов наряду со сложными ароматическими структурами, для достижения полного дегалогенирования используется смесь более чем одного вида бактерий и / или грибов (часто называемая консорциумом).[8] Реакция на рисунке 2 показывает восстановительное дебромирование 2,4,6-трибромфенол (2,4,6-TBP) по Охрабактрум.[13] На основании относительной деградации молекулы наряду с аналитическими результатами было постулировано, что разложение 2,4,6-ТБФ происходит за счет дебромирования орто-бромин на первом этапе дегалогеназы с образованием 2,4-дибромфенол (2,4-ДАД). Поскольку есть два орто бромы, дебромирование либо орто углерод даст тот же продукт. Другие виды, такие как Pseudomonas galthei или Azotobacter sp. показал предпочтение параграф-Halide над мета- или орто -галогениды. Например, Azotobacter sp. деградирует 2,4,6-трихлорфенол (2,4,6-TCP) в 2,6-дихлоргидрохинон из-за различий в селективности TCP-4-монооксигеназы между орто- и параграф-галогенид. Эти различия в региоселективности между видами можно объяснить специфичностью трехмерной структуры фермента и ее препятствием для стерических взаимодействий.[13] Было высказано предположение, что протон теряется фенольной группой 2,4,6-ТБФ, что приводит к образованию отрицательно заряженного галогенфенолят-иона. Последующая атака пара-углерод с гидрид-анионом из NAD (P) H в результате нуклеофильной атаки, и резонансная перегруппировка приводит к замещению брома гидридом и образованию 2,4-DBP. Последующие шаги по аналогичной схеме дают 2-бромфенол и фенол на последнем этапе. Фенол может метаболизироваться микроорганизмами, чтобы сделать метан и углекислый газ или может быть извлечен легче, чем AOX.[12][13]
Связанные термины
Органические галогениды, экстрагируемые органические галогениды (EOX) и общие органические галогениды (TOX) относятся к этой теме. EOX предоставляет информацию о том, как можно экстрагировать галогениды с помощью растворителя, в то время как TOX предоставляет информацию об общем содержании органических галогенидов в образце. Это значение можно использовать для оценки биохимическая потребность в кислороде (BOD) или химическая потребность в кислороде (ХПК), ключевой фактор в оценке количества кислорода, необходимого для сжигания органических соединений, для оценки процентного содержания AOX и экстрагируемых органических галогенидов.
Рекомендации
- ^ а б c d е ж Ван Осман, Ван Хаснида; Шейх Абдулла, Сити Розаима; Мохамад, Абу Бейкер; Kadhum, Abdul Amir H .; Абд Рахман, Рамки (2013) [2013]. «Одновременное удаление AOX и ХПК из сточных вод из рециркулированной бумаги с использованием GAC-SBBR». Журнал экологического менеджмента. 121: 80–86. Дои:10.1016 / j.jenvman.2013.02.005. PMID 23524399.
- ^ Хайлман, Бетт; Лонг, Дженис Р.; Киршнер, Элизабет М. (1994-11-21). «Хлорная промышленность приходит в упадок, несмотря на постоянные опасения по поводу здоровья». Архив новостей химии и машиностроения. 72 (47): 12–26. Дои:10.1021 / cen-v072n047.p012. ISSN 0009-2347.
- ^ а б c Savant, D.V .; Абдул-Рахман, Р .; Ранаде, Д. (2005). «Анаэробное разложение адсорбируемых органических галогенидов (АОГ) из сточных вод целлюлозно-бумажной промышленности». Биоресурсные технологии. 97 (9): 1092–1104. Дои:10.1016 / j.biortech.2004.12.013. PMID 16551531.
- ^ Бьёрсет, Альф; Карлберг, Джордж Э .; Мёллер, Мона (1979-03-01). «Определение галогенированных органических соединений и испытание на мутагенность отработанных отбеливателей». Наука об окружающей среде в целом. 11 (2): 197–211. Bibcode:1979ScTEn..11..197B. Дои:10.1016/0048-9697(79)90027-5.
- ^ Хатчинс, Флойд Э (1979). Токсичность сточных вод целлюлозно-бумажных комбинатов: обзор литературы. Национальный сервисный центр экологических публикаций. п. 2.
- ^ а б c d е ж грамм Грон, Кристиан (1993-08-01). «Параметры группы органических галогенов как индикаторы загрязнения подземных вод». Мониторинг и восстановление грунтовых вод. 13 (3): 148–158. Дои:10.1111 / j.1745-6592.1993.tb00084.x. ISSN 1745-6592.
- ^ а б Лонгвик, Виви-Энн; Холмбом, Бьярн (1994-03-01). «Образование мутагенных органических побочных продуктов и АОХ при хлорировании фракций гуминовой воды». Водные исследования. 28 (3): 553–557. Дои:10.1016 / 0043-1354 (94) 90006-Х.
- ^ а б c d е Баджпай, Пратима; Баджпай, Прамод К. (1 января 1997 г.). Эрикссон, К.-Э. L .; Babel, Prof Dr W .; Бланч, профессор д-р Х. В .; Куни, профессор доктор Ч.Л .; Enfors, Prof Dr S.-O .; Эрикссон, профессор д-р К.-Э. L .; Fiechter, Prof Dr A .; Клибанов, проф. Д-р А.М .; Маттиассон, профессор д-р Б. (ред.). Биотехнологии в целлюлозно-бумажной промышленности. Достижения в области биохимической инженерии / биотехнологии. Springer Berlin Heidelberg. стр.213 –259. Дои:10.1007 / bfb0102076. ISBN 9783540618683.
- ^ а б c Bornhardt, C .; Drewes, J. E .; Екель, М. (1 января 1997 г.). «Удаление органических галогенов (AOX) из городских сточных вод путем обработки порошкообразным активированным углем (PAC) / активным илом (AS)». Водные науки и технологии. Расширенная очистка сточных вод: удаление питательных веществ и анаэробные процессы. 35 (10): 147–153. Дои:10.1016 / S0273-1223 (97) 00207-2.
- ^ «ИЛИАС 3». cgi.tu-harburg.de. Получено 2016-10-11.
- ^ а б Vahala, R .; Långvik, V. -A .; Лаукканен, Р. (1999-01-01). «Контроль образования адсорбируемых органических галогенов (AOX) и тригалометанов (THM) с помощью озонирования и двухступенчатой фильтрации с использованием гранул с активированным углем (GAC)». Водные науки и технологии. 40 (9): 249–256. Дои:10.1016 / S0273-1223 (99) 00663-0.
- ^ а б c d е ж Чжан, Чуньлун; Беннетт, Джордж Н. (26 января 2005 г.). «Биодеградация ксенобиотиков анаэробными бактериями». Прикладная микробиология и биотехнология. 67 (5): 600–618. Дои:10.1007 / s00253-004-1864-3. ISSN 0175-7598. PMID 15672270.
- ^ а б c d ЯМАДА, Такаши; ТАКАХАМА, Юки; ЯМАДА, Ясухиро (23 мая 2008 г.). «Биодеградация 2,4,6-трибромфенола штаммом TB01 Ochrobactrum sp.». Биология, биотехнология и биохимия. 72 (5): 1264–1271. Дои:10.1271 / bbb.70755. ISSN 0916-8451. PMID 18460800.
- ^ а б c d е Тием, Андреас; Шмидт, Катрин Р. (2011). «Последовательное анаэробное / аэробное биоразложение хлорэтенов - аспекты полевого применения». Текущее мнение в области биотехнологии. 22 (3): 415–421. Дои:10.1016 / j.copbio.2011.02.003. PMID 21377349.
- ^ Песня, Сюэпин; Пей, Юн; Су, Цзинцзин; Цинь, Чэнжун; Ван, Шуанфэй; Не, Шуанси (19.07.2016). «Кинетика восстановления адсорбируемых органических галогенидов (AOX) при отбеливании жомовой пульпы с помощью лакказы диоксидом хлора». Биоресурсы. 11 (3): 7462–7475. Дои:10.15376 / biores.11.3.7462-7475. ISSN 1930-2126.




