Хлорсульфонилизоцианат - Chlorosulfonyl isocyanate
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Хлорсульфонилизоцианат | |
| Другие имена N-Карбонилсульфамилхлорид Хлоропиросульфонилизоцианат Изоцианат сульфурилхлорида | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.013.378 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| CNClO3S | |
| Молярная масса | 141,53 г / моль |
| Внешность | бесцветная жидкость |
| Плотность | 1,626 г / см3 |
| Температура плавления | -44 ° С (-47 ° F, 229 К) |
| Точка кипения | 107 ° С (225 ° F, 380 К) |
| разложение | |
| Растворимость в других растворителях | Хлороуглероды MeCN |
| 1.447 | |
| Структура | |
| тетраэдр в S | |
| Опасности | |
| Главный опасности | токсичный, коррозионный, легковоспламеняющийся, бурно реагирует с водой |
| Паспорт безопасности | «Внешний паспорт безопасности материала» |
| Пиктограммы GHS |     |
| Сигнальное слово GHS | Опасность |
| H302, H312, H314, H330, H332, H334 | |
| P260, P261, P264, P270, P271, P280, P284, P285, P301 + 312, P301 + 330 + 331, P302 + 352, P303 + 361 + 353, P304 + 312, P304 + 340, P304 + 341, P305 + 351 + 338, P310, P312, P320, P321, P322, P330, P342 + 311, P363, P403 + 233 | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Родственные соединения | Тионил хлорид Цианоген бромид Фосфорилхлорид |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Хлорсульфонилизоцианат химическое соединение ClSO2NCO, известный как CSI. Это соединение является универсальным реагентом в органический синтез.
Подготовка, состав, обращение
CSI получают путем обработки цианоген хлорид с триоксид серы, продукт отгоняют непосредственно из реакционной смеси.[1]
- ТАК3 + ClCN → ClSO2Унтер-офицер
В этом превращении функционализированы как углеродные, так и азотные концы CN.
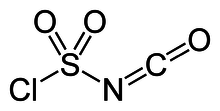
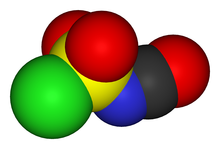
Структура CSI представлена как ClS (O)2-N = C = O. Он состоит из двух электроноакцепторных компонентов, хлорсульфонильной группы (SO2Cl) и изоцианат группа (-N = C = O). Из-за получаемой электрофильности использование CSI в химическом синтезе требует относительно инертных растворителей, таких как хлоруглероды, ацетонитрил и простые эфиры.[2]
Использует
Молекула имеет два электрофильных центра, углеродный и S (VI) центр.[3]
CSI использовался для получения β-лактамы, некоторые из которых имеют важное медицинское значение. Таким образом, алкены подвергаются [2 + 2] -циклоприсоединению с образованием сульфонамида. SO2Группу Cl можно удалить простым гидролизом, оставив вторичный амид.[4]Другие реакции CSI:
- Циклоприсоединение к алкинам с образованием 1,2,3-оксатиазин-2,2-диоксид-6-хлоридов.
- Превращение первичных спиртов в карбаматы.[5]
- Преобразование карбоновые кислоты и хлорангидриды в нитрилы.
- Получение N, N-дизамещенного сульфамиды, Р2НСО2NH2
- Подготовка Реагент Берджесса
Соображения безопасности
CSI токсичен, вызывает коррозию и бурно реагирует с водой. Нравиться плавиковая кислота, его нельзя хранить в стеклянной посуде, вместо этого требуются полиэтиленовые бутылки.
Рекомендации
- ^ Граф Р. "Хлорсульфонилизоцианат" Органический синтез, Собрание тома 5, страницы 226ff.
- ^ Миллер, М. Дж .; Ghosh, M .; Guzzo, P.R .; Vogt, P. F .; Hu, J .; Filzen, G.F .; Гейер, А. Г. «Хлорсульфонилизоцианат» в «Энциклопедии реагентов для органического синтеза», 2005 г. John Wiley & Sons: Нью-Йорк.
- ^ Д. Н. Дхар, К. С. К. Мурти "Последние достижения в химии хлорсульфонилизоцианата" Синтез 1986; страницы 437-449.
- ^ Кремлин, Р. Дж. «Введение в химию сероорганических соединений» Джон Уайли и сыновья: Чичестер (1996). ISBN 0-471-95512-4
- ^ Берджесс, Э. М .; Penton, Jr., H.R .; Тейлор, Э. А .; Уильямс, В. М. «Превращение первичных спиртов в уретаны через внутреннюю соль гидроксида триэтиламмония: метил (карбоксилсульфамоил) триэтиламмоний гидроксид метил-н-гексилкарбамат» Organic Syntheses, Coll. Vol. 6, стр.788

