Циннамилацетат - Cinnamyl acetate
 | |
| Имена | |
|---|---|
| Название ИЮПАК 3-фенилпроп-2-енилацетат | |
| Другие имена | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.002.838 |
| Номер ЕС |
|
| КЕГГ | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| C11ЧАС12О2 | |
| Молярная масса | 176.215 г · моль−1 |
| Внешность | Бесцветная жидкость |
| Запах | Сладкий, цветочный, бальзамический запах[3] |
| Плотность | 1,057 г / мл[4] |
| Точка кипения | 265 ° С (509 ° F, 538 К)[3] |
| 212,3 мг / л[1] | |
| бревно п | 2.85[5][6] |
| Давление газа | 0,008 мм рт. Ст. (20 ° C)[1] |
| 1.539 - 1.543[3] | |
| Опасности | |
| Главный опасности | Вызывает раздражение глаз, может вызвать аллергическую кожную реакцию.[7] |
| Пиктограммы GHS |  [7] [7] |
| Сигнальное слово GHS | Предупреждение[7] |
| H317, H319[7] | |
| P261, P264, P272, P280, P302 + 352, P305 + 351 + 338, P321, P333 + 313, P337 + 313, P363, P501[7] | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 103–113 ° С (217–235 ° F, 376–386 К)[3][8] |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Циннамилацетат (3-фенилпроп-2-енилацетат) представляет собой химическое соединение семейства коричных сложных эфиров, в котором переменная группа R замещена метильная группа. В результате неароматической двойной связи углерод-углерод циннамилацетат может существовать в Z и E конфигурация:[9]
Циннамилацетат естественным образом содержится в свежей коре корица (Cinnamomum zeylanicum Blume и другие виды Cinnamomum) с концентрациями 2 800–51 000 ppm.[10][5]
Циннамилацетат используется в качестве эфирного ароматизатора, например, в хлебе и кормах для животных и имеет сладкий цветочно-фруктовый аромат.[6][11][12] Кроме того, он используется в некоторых косметических средствах, некоторых туалетных принадлежностях, а также в некосметических продуктах, например, в моющих средствах.[9]
Законодательство и контроль
Циннамилацетат, используемый в ароматизаторах и в качестве ароматизатора, обсуждался несколькими организациями. В 1965 году ассоциация производителей ароматизаторов и экстрактов пометила это соединение как «Общепризнанное безопасным в качестве ароматизатора» (FEMA ). Ассоциация определила средние максимальные уровни использования нескольких продуктов, которые считались безопасными:[13]
| Напитки | Мороженое, лед и т. Д. | Конфеты | Выпечка | Жевательная резинка |
|---|---|---|---|---|
| 2,7 частей на миллион | 6,5 частей на миллион | 16 частей на миллион | 11 частей на миллион | 8,7 частей на миллион |
В Европейский парламент зарегистрировал циннамилацетат как ароматизатор и косметическое соединение в 1996 году.[14][15] Сустав (ФАО /ВОЗ ) Комитет экспертов по пищевым добавкам (JECFA ) в 2000 г. описал, что «это вещество не представляет опасности для безопасности при нынешних уровнях потребления при использовании в качестве ароматизатора».[1] В 2009 г. EFSA Группа по материалам, контактирующим с пищевыми продуктами, ферментам, ароматизаторам и технологическим добавкам (CEF) пришла к выводу, что циннамилацетат не вызывает проблем с безопасностью при использовании в качестве ароматизатора в пищевых продуктах.[6] Циннамилацетат также разрешен Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США для использования в качестве ароматизатора в пищевых продуктах, если используется минимальное количество, необходимое для его действия.[16]
Производство и потребление
Оценки среднегодового производства и суточного потребления циннамилацетата в качестве ароматизатора сообщаются ВОЗ. Согласно этому отчету, годовой объем производства в Европе составляет 1498 кг, а в США - 2255 кг. Суточная доза на человека в Европе оценивается в 210 мкг, а в США - 300 мкг. Согласно оценкам, суточная доза на кг массы тела для европейцев составляет 4 мкг / кг, а для американцев - 5 мкг / кг.[17]
Синтез
Поскольку циннамилацетат встречается в естественных условиях в растениях, его можно экстрагировать и очищать для получения соединения. Однако это имеет низкий выход и, следовательно, высокие производственные затраты. Использование химических методов может предложить более эффективные стратегии для производства циннамилацетата.[10]
Есть несколько способов синтезировать циннамилацетат. 2. Один из способов - синтез из циннамиловый спирт 1 и винилацетат. Эта реакция катализируется ферментом гидролаза сложного эфира триацилглицерина, который является липаза это очень характерно для сложноэфирной связи. Побочным продуктом этой реакции является ацетальдегид. Уравнение реакции для этой реакции:[18]
Поскольку ацетальдегид оказывает неблагоприятное дезактивирующее действие на липазу, используемую в синтезе, ацетат этила может использоваться в качестве реагента вместо винилацетата. В этом переэтерификация реакция коричный спирт 1 реагирует с этилацетатом с образованием циннамилацетата 2 и этиловый спирт. Этот синтез требует липазы Novozym 435 и проводится в системе без растворителей. Реакция следующая:[12]
Циннамилацетат 2 также может быть синтезирован неферментативной реакцией. Примером такой реакции является реакция с использованием бромистого циннамила. 3 и ацетат натрия в качестве реагентов. Поскольку эти соединения являются несмешивающимися субстратами, можно использовать катализ с переносом твердой фазы в жидкую (PTC), используя бромид четвертичного аммония в качестве катализатор межфазного переноса. Об этом свидетельствует следующая реакция:[19]
Помимо этих трех примеров, существует еще много способов синтеза ацетата циннамила.
В реакция присоединения из триоксид диазота к циннамилацетату образует промежуточное соединение при синтезе хлорамфеникол.[20]
Метаболизм
Циннамилацетат принадлежит к группе производных циннамила. Как правило, эти производные циннамила всасываются из кишечника очень быстро, после чего они метаболизируются и выводятся в виде полярных метаболитов с мочой или калом в течение 24 часов.[5][21]
Среди производных циннамила ацетат циннамила принадлежит к группе сложных эфиров корицы. После всасывания из кишечника эта группа соединений является первой. гидролизованный в коричный спирт карбоксилэстеразы. Карбоксилэстеразы - это группа ферментов. Наиболее важными ферментами в этой группе являются A-эстеразы. Они присутствуют в большинстве тканей тела, но преобладают в гепатоциты. Впоследствии циннамиловый спирт является окисленный что приводит к образованию коричный альдегид. Эта реакция катализируется человеком. НАД+ -зависимый алкогольдегидрогеназа. Теперь есть два пути для дальнейшего биотрансформация коричного альдегида. Второстепенный путь биотрансформации - это S-глутатионилирование. Однако основным путем является превращение коричного альдегида в коричная кислота ферментом альдегиддегидрогеназа. Далее коричная кислота превращается в циннамоил КоА который снова превращается либо в циннамоилглицин N-ацилтрансферазой, либо в бензоил-КоА через β-окисление, последний является основным маршрутом. Промежуточные метаболиты в пути β-окисления могут превращаться в 3-гидрокси-3-фенилпропионовую кислоту и ацетофенон, который может выводиться с мочой. Однако превращение этих промежуточных метаболитов осуществляется второстепенными путями. Наконец, бензоил-КоА конъюгирован с глицин при формировании гиппуровая кислота или гидролизуется с образованием свободных бензойная кислота. Он может выводиться с мочой сразу или после глюкуронизация. Гиппуровая кислота, являющаяся основным метаболитом, также выводится с мочой.[5][21][6]
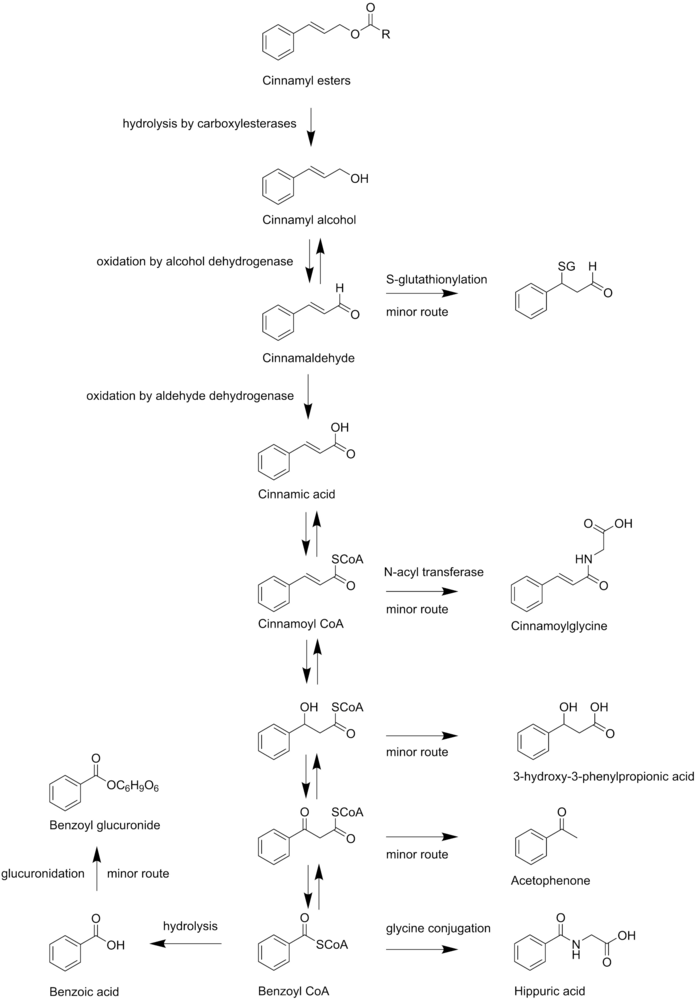 Биотрансформация циннамиловых эфиров.
Биотрансформация циннамиловых эфиров.
Токсичность
Поскольку циннамилацетат используется и как ароматизатор, и как ингредиент пищевого ароматизатора, воздействие на кожу и ротовую полость считается основными путями абсорбции. Систематическое воздействие на кожу циннамилацетата через косметические продукты оценивается в 0,0115 мг / кг массы тела / день.[5]
В прошлом было проведено несколько экспериментов на животных для оценки токсичности циннамилацетата. В одном эксперименте пероральная токсичность была проверена на крысах. Крысы получали перорально дозы циннамилацетата и LD50 оказалось 3,3 г / кг. В ходе эксперимента для высоких доз наблюдались такие симптомы, как замедленное дыхание и грубый тремор.[1] Другие эксперименты показали LD50 значения 4,750 г / кг для перорального введения мышам и морским свинкам. Кроме того, LD50 ценность для внутрибрюшинное введение было исследовано и установлено, что оно составляет 1.200 г / кг.[22]
Кроме того, были проведены исследования кожной токсичности. Эксперименты на кроликах привели к LD50 более 5,0 г / кг, но клинических эффектов не наблюдалось. Кроме того, уровень раздражения кожи у свиней проверяли с помощью 48-часовой патч-тест. В этом исследовании применяли 0,05 г циннамилацетата, и раздражения не наблюдалось. В двух других экспериментах изучали раздражение кожи, вызванное 0,1 мл циннамилацетата на морских свинках и кроликах, путем прямого нанесения на кожу (открытое нанесение). В этих экспериментах наблюдалось раздражение от слабого до умеренного.[1]
А NOAEL для перорального приема 275 мг / кг массы тела / день было определено на основании токсикологических данных EFSA Панель по добавкам и продуктам или веществам, используемым в кормах для животных (FEEDAP).[6]
Помимо этих экспериментов на животных, были выполнены некоторые исследования на людях. 48-часовой закрытый патч-тест на пяти здоровых добровольцах-мужчинах был проведен с использованием 5% циннамилацетата в вазелин. В этом исследовании раздражения не наблюдалось. Слабое раздражение наблюдалось в другом 48-часовом тесте на 50 добровольцев мужского пола с использованием 32% циннамилацетата в ацетон. Наконец, исследование сенсибилизации кожи на людях было выполнено на 25 здоровых добровольцах мужского пола. В этом эксперименте тест максимизации (48-часовой пластырь) проводился с использованием 5% циннамилацетата в петролатуме. Реакции сенсибилизации кожи не наблюдалось.[1]
Более того, стандартные тесты Дрейза были использованы для оценки кожной токсичности у людей, морских свинок и кроликов. Это приводило к легкому раздражению кожи при дозах 16 мг за 48 часов для людей и при дозах 100 мг за 24 часа для морских свинок. У кроликов, подвергшихся воздействию доз 100 мг в сутки, наблюдалось умеренное раздражение кожи.[22]
Наконец, способность циннамилацетата вызывать обмены сестринских хроматид был протестирован с использованием Клетки яичника китайского хомяка. Это было сделано потому, что было обнаружено, что другой компонент растительной эссенции и производного корицы, коричный альдегид, увеличили частоту обменов сестринских хроматид, вызванных митомицин С. Однако результат этого теста доказал, что циннамилацетат не вызывает обмен сестринских хроматид из-за отсутствия альфа-бета ненасыщенного карбонильная группа.[23]
Воздействие на животных
Циннамилацетат содержится в масле листьев Cinnamomum osmophloeum дерево, которое растет в центральном и северном Тайване. Установлено, что эти масла обладают антибактериальным, противоминным, антитермитным, антимитным, противогрибковым и противовоспалительным действием. Кроме того, масла проявляют ларвицидную активность против комаров. Aedes aegypti и Aedes albopictus личинки. Однако циннамилацетат играет незначительную роль в этих действиях.[24][25][26][27]
Кроме того, циннамилацетат обладает репеллентным действием на Anopheles gambiae, и поэтому полезен для защиты от этих насекомых.[28]
Рекомендации
- ^ а б c d е ж грамм Бхатия С.П., Веллингтон Г.А., Коккиара Дж., Лалко Дж., Летиция С.С., Апи А.М. (01.01.2007). «Обзор ароматического материала на циннамилацетате». Пищевая и химическая токсикология. 45 Дополнение 1 (1): S53–7. Дои:10.1016 / j.fct.2007.09.012. PMID 18031892.
- ^ «Уксусная кислота, циннамиловый эфир». webbook.nist.gov. Получено 2018-03-22.
- ^ а б c d ПАСПОРТ БЕЗОПАСНОСТИ МАТЕРИАЛА ELAN CHEMICAL COMPANY, INC - Циннамилацетат. Дата обновления: 30 ноября 2005 г.
- ^ "103-54-8 CAS MSDS (циннамилацетат) Температура плавления Плотность Химические свойства CAS". www.chemicalbook.com. Получено 2018-03-22.
- ^ а б c d е Белсито Д., Бикерс Д., Брюз М., Калоу П., Грейм Х., Ханифин Дж. М., Роджерс А. Э., Сорат Дж. Х., Сайпс И. Г., Тагами Х. (2007). «Токсикологическая и дерматологическая оценка родственных сложных эфиров и спиртов коричной кислоты и циннамилового спирта при использовании в качестве ароматизаторов». Пищевая и химическая токсикология. 45 Дополнение 1: S1–23. Дои:10.1016 / j.fct.2007.09.087. PMID 18035463.
- ^ а б c d е Рихен, Гвидо (2017). «Безопасность и эффективность арилзамещенных первичных спиртов, альдегидов, кислот, сложноэфирных и ацетальных производных, принадлежащих к химической группе 22, при использовании в качестве ароматизаторов для всех видов животных». Журнал EFSA. 15 (2): 4672–4692. Дои:10.2903 / j.efsa.2017.4672. PMID 32625398.
- ^ а б c d е Pubchem. «Циннамилацетат». pubchem.ncbi.nlm.nih.gov. Получено 2018-03-23.
- ^ «Циннамилацетат 166170». Сигма-Олдрич. Получено 2018-03-23.
- ^ а б Любке, Уильям (31.01.2018). "циннамилацетат, 103-54-8". www.thegoodscentscompany.com. Получено 2018-03-23.
- ^ а б Донг Х., Секундо Ф., Сюэ С., Мао Х (март 2017 г.). «Цельноклеточный биокаталитический синтез циннамилацетата с новой эстеразой из библиотеки ДНК Acinetobacter hemolyticus». Журнал сельскохозяйственной и пищевой химии. 65 (10): 2120–2128. Дои:10.1021 / acs.jafc.6b05799. PMID 28220703.
- ^ МакКоннелл, Роб (1986). Отчет об оценке опасности для здоровья. ЮЖНЫЙ БЕНД, ИНДИАНА: ИНТЕРНЭШНЛ БЕЙКЕРС СЕРВИСИС, ИНК.
- ^ а б Гэн Б (август 2012 г.). "Синнамилацетат синтез путем катализируемой липазой переэтерификации в системе без растворителей". Биотехнология и прикладная биохимия. 59 (4): 270–275. Дои:10.1002 / баб.1023. PMID 23586860. S2CID 45334781.
- ^ Холл, Ричард (1965). III. Вещества GRAS. США: The Garrard Press.
- ^ РЕШЕНИЕ КОМИССИИ от 23 февраля 1999 г. об утверждении реестра ароматизирующих веществ, используемых в пищевых продуктах или на них, составленного в соответствии с Регламентом (ЕС) № 2232/96 Европейского парламента и Совета от 28 октября 1996 г.
- ^ РЕШЕНИЕ КОМИССИИ от 8 мая 1996 г. об установлении реестра и общей номенклатуры ингредиентов, используемых в косметических продуктах.
- ^ "CFR - Свод федеральных правил, раздел 21". www.accessdata.fda.gov. Получено 2018-03-21.
- ^ «ЦИННАМИЛОВЫЙ СПИРТ И РОДСТВЕННЫЕ ВЕЩЕСТВА». www.inchem.org. Получено 2018-03-22.
- ^ Цай X, Ван В., Линь Л., Хэ Д., Шен Й, Вэй В., Вей Д. (2017-04-01). «Синтез циннамиловых эфиров путем переэтерификации, катализируемой липазой, в неводной системе». Письма о катализе. 147 (4): 946–952. Дои:10.1007 / s10562-017-1994-8. S2CID 99525798.
- ^ Девулапелли, Вену Гопал; Вэн, Хун-Шань (25.07.2009). «Синтез циннамилацетата твердофазным катализом с переносом фазы: кинетическое исследование с реактором периодического действия». Catalysis Communications. 10 (13): 1638–1642. Дои:10.1016 / j.catcom.2009.04.032.
- ^ Курихара Й, Ямагиши К. (1965-08-01). "Реакция присоединения триоксида диазота к ацетату циннамила 7". Бюллетень химического общества Японии. 38 (8): 1327–1330. Дои:10.1246 / bcsj.38.1327.
- ^ а б Бикерс Д., Калоу П., Грейм Х., Ханифин Дж. М., Роджерс А. Е., Сорат Дж. Х., Сайпс И. Г., Смит Р. Л., Тагами Х (июнь 2005 г.). «Токсикологическая и дерматологическая оценка коричного спирта, коричного альдегида и коричной кислоты при использовании в качестве ароматизаторов». Пищевая и химическая токсикология. 43 (6): 799–836. Дои:10.1016 / j.fct.2004.09.013. PMID 15811570.
- ^ а б «Номер RTECS GE2275000». ccinfoweb2.ccohs.ca. Получено 2018-03-22.
- ^ Сасаки, ЮФ .; Иманиши, Хисако; Охта, Тошихиро; Ширасу, Ясухико (1 июня 1989 г.). «Модифицирующие эффекты компонентов растительной эссенции индукции сестринских хроматидных обменов в культивируемых клетках яичников китайского хомячка». Письма об исследованиях мутаций. 226 (2): 103–110. Дои:10.1016/0165-7992(89)90051-1. PMID 2499782.
- ^ Ченг С.С., Лю Дж.Й., Хуанг К.Г., Хсуи Ю.Р., Чен В.Дж., Чанг С.Т. (январь 2009 г.). «Инсектицидное действие эфирных масел листьев Cinnamomum osmophloeum против трех видов комаров». Биоресурсные технологии. 100 (1): 457–64. Дои:10.1016 / j.biortech.2008.02.030. PMID 18396039.
- ^ Чанг, Шан-Цзэнь; Чен, Pin-Fun; Чанг, Шан-Чвэнь (2001-09-01). «Антибактериальная активность эфирных масел листьев и их компонентов из Cinnamomum osmophloeum». Журнал этнофармакологии. 77 (1): 123–127. Дои:10.1016 / S0378-8741 (01) 00273-2. ISSN 0378-8741. PMID 11483389.
- ^ Чанг С., Ченг С. (2002). «Антитермитическая активность эфирных масел листьев и компонентов из Cinnamomum osmophleum». Журнал сельскохозяйственной и пищевой химии. 50 (6): 1389–1392. Дои:10.1021 / jf010944n.
- ^ Ю-Тан Т (2010). «Противовоспалительное действие эфирных масел и их компонентов из листьев местной корицы (Cinnamomum osmophloeum) различного происхождения». Фармацевтическая биология. 48 (10): 1130–1136. Дои:10.3109/13880200903527728. PMID 20815702.
- ^ Делетр Э., Чандре Ф., Уильямс Л., Дюменил С., Менют С., Мартин Т. (июнь 2015 г.). «Электрофизиологическая и поведенческая характеристика биоактивных соединений эфирных масел Thymus vulgaris, Cymbopogon winterianus, Cesium cyminum и Cinnamomum zeylanicum против Anopheles gambiae и перспективы их использования в качестве лечебных сеток». Паразиты и векторы. 8: 316. Дои:10.1186 / s13071-015-0934-у. ЧВК 4470088. PMID 26063119.







