Демьяновская перестановка - Demjanov rearrangement
В Демьяновская перестановка это химическая реакция первичного амины с азотистая кислота дать переставить спирты.[1][2][3] Это предполагает замену на гидроксил группа с возможным расширение кольца. Назван в честь русского химика. Николай Яковлевич Демьянов (Демьянов, Демьянов) (1861–1938). [4]
Механизм реакции
Процесс реакции начинается с диазотизация амина азотистой кислотой. Группа диазония - хороший уходящая группа, формируя газообразный азот при вытеснении из органической структуры. Это смещение может происходить через перестановку (путь A), в которой один из сигма-облигации соседний с диазогруппой мигрирует. Эта миграция приводит к расширению кольца. Затем образовавшийся карбокатион подвергается атаке молекулы воды. С другой стороны, диазогруппа может быть замещена непосредственно молекулой воды в SN2 реакция (путь B). Оба маршрута приводят к образованию алкоголь.[5]
| А. | 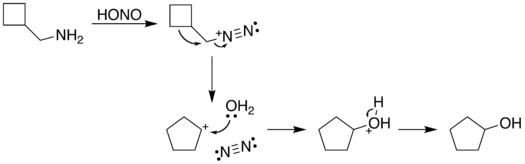 |
| Б. |  |
Использует
Перегруппировка Демьянова представляет собой метод увеличения одноуглеродного цикла в четырех-, пяти- или шестичленные кольца. Полученные пяти-, шести- и семичленные кольца можно затем использовать в дальнейших синтетических реакциях.
Было показано, что реакция Демьянова подвержена региоселективность. Одним из примеров этого является исследование, проведенное Д. Фаттори, изучающее региоселективность перегруппировки Демьянова в увеличении одноуглеродистого голого сахара.[6] Это показало, что когда экзо метиламин подвергся дезаминированию азотистой кислотой Демьянова, укрупнения колец не производилось.
Однако когда эндо метиламин проходил в тех же условиях, была получена смесь перегруппированных спиртов.
Проблемы
Эта перегруппировка также приводит к замещенному, но не расширенному побочному продукту. Таким образом, может оказаться трудным выделить два продукта и получить желаемый выход. Также стереоизомеры получают в зависимости от направления добавления молекулы воды, и другие молекулы могут быть получены в зависимости от перегруппировки.
Будущее использование
Текущие исследования изучают возможности различных управляющих групп влиять на селективность продуктов перегруппировки Демьянова, таких как олово или кремний.[7]Это может привести к большему успеху с Демьяновым, так как это позволит лучше контролировать реакцию и увеличить желаемый выход продукта. Перегруппировка невероятно полезна, но ее использование иногда может оказаться неэффективным из-за сложности создания предпочитаемого продукта. Таким образом, если руководящие группы возможны, это значительно улучшит применимость Демьянова.
Вариации
Перестановка Тиффно-Демьянова
В Перестановка Тиффно-Демьянова (после Марк Тиффно и Николай Демьянов ) является разновидностью перестановки Демьянова, которая включает в себя как расширение кольца и производство кетон используя нитрат натрия и катион водорода. Использование реакции Тиффно-Демьянова часто является выгодным, поскольку, хотя в продуктах возможны перегруппировки, реагент всегда подвергается расширению кольца. Как и в перегруппировке Демьянова, продукты демонстрируют региоселективность реакции. Миграционные способности функциональных групп диктуют продукты перегруппировки.
Использование диазометана
Диазометан также вызывает увеличение кольца, и его реакция механически аналогична реакции Перестановка Тиффно-Демьянова.
Смотрите также
Рекомендации
- ^ Демьянов, Н. Дж .; Лушников, М. (1903). «[Продукты действия азотистой кислоты на тетраметиленилметиламин]». Журнал Русскаго Физико-Химического Общества [Ж. Русь. Phys. Chem.] (на русском). 35: 26–42.
- ^ Демьянов, Н. Дж .; Лушников, М. (1903). Chem. Центр. 1: 828. Отсутствует или пусто
| название =(помощь) - ^ Смит, П. А. С .; Баер, Д. Р. (1960). Орг. Реагировать. 11: 157. Отсутствует или пусто
| название =(помощь) (Рассмотрение) - ^ Джек Ли, Джи (2006). Название Реакции (Третье изд.). Берлин: Springer.
- ^ Чау, L; McClure, M; Уайт, Дж. (2004). «Кремний и олово-направленная реакция Тиффно-Демьянова». Орг. Biomol. Chem. 2 (5): 648–50. Дои:10.1039 / b314923d. PMID 14985802.
- ^ Fattori, D .; Генри, S .; Фогель, П. (1993). "Расширения одноуглеродного кольца Демьянова и Тиффно-Демьянова производных 2-аминометил-7-оксабицикло [2.2.1] гептана. Стерео- и региоселективные добавления 8-оксабицикло [3.2.1] окт-6-ен-2 -один мягким электрофилам ». Тетраэдр. 49 (8): 1649–1664. Дои:10.1016 / S0040-4020 (01) 80352-5.
- ^ McKinney, M.A .; Патель, П. (1973). "Кольцевые расширения. I. Диазометан и кольцевые расширения Тиффно-Демьянова норкамфоры и дегидроноркамфоры". J. Org. Chem. 38 (23): 4059. Дои:10.1021 / jo00987a023.
- ^ Котани, Р. (1965). «Демьяновская перегруппировка 1-метилциклогексанметиламина». J. Org. Chem. 30 (2): 350–354. Дои:10.1021 / jo01013a009.
- ^ Бриллиант, Дж; Bruce, W.F .; Тайсон, Ф. (1965). «Гексагидро-1-метил-4-фенил-4-ацетоксиазепин и Демьяновская перегруппировка 1-метил-4-фенилпиперидин-4-метиламина *». J. Org. Chem. 30 (6): 1840. Дои:10.1021 / jo01017a030.
- ^ Накадзаки, М .; Naemura, K .; Хашимото, М. (1985). «Необычные последовательные перегруппировки в реакции расширения кольца Демьянова 2- (аминометил) -D2d-динорадамантана и 9- (аминометил) норадамантана». J. Org. Chem. 48 (13): 2289. Дои:10.1021 / jo00161a033.
- ^ Jones, J.B .; Прайс, П. (1973). «Стероиды и стероиды-XIX: Сравнение диазометана и тиффено-демьяновых гомологий 5α-3-оксостероидов. Доказательства преобладающего экваториального приближения карбонильной группы C-3 к диазометану». Тетраэдр. 29 (14): 1941–1947. Дои:10.1016/0040-4020(73)80128-0.
- ^ Stern, A.G .; Никон, А. (1992). «Синтез брексан-2-она и конгенеров с расширенным кольцом». J. Org. Chem. 57 (20): 5432. Дои:10.1021 / jo00046a015.



