Диазометан - Diazomethane
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Диазометан | |
| Другие имена Азиметилен, Азометилен, Диазирин | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.005.803 |
| Номер ЕС |
|
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
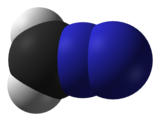
| CH2N2 | |
| Молярная масса | 42,04 г / моль |
| Внешность | Желтый газ |
| Запах | затхлый |
| Плотность | 1,4 (воздух = 1) |
| Температура плавления | -145 ° С (-229 ° F, 128 К) |
| Точка кипения | -23 ° С (-9 ° F, 250 К) |
| гидролиз[1] | |
| Структура | |
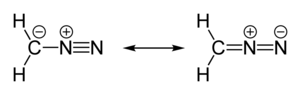
| линейный C = N = N | |
| полярный | |
| Опасности | |
| Основной опасности | токсичный и взрывоопасный |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасность |
| H350 | |
| P201, P202, P281, P308 + 313, P405, P501 | |
| NFPA 704 (огненный алмаз) | |
| Смертельная доза или концентрация (LD, LC): | |
LC50 (средняя концентрация ) | 175 частей на миллион (кошка, 10 мин)[3] |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 0,2 частей на миллион (0,4 мг / м3)[2] |
REL (Рекомендуемые) | TWA 0,2 частей на миллион (0,4 мг / м3)[2] |
IDLH (Непосредственная опасность) | 2 частей на миллион[2] |
| Родственные соединения | |
Связанный функциональные группы; соединения | R-N = N = N (азид ), R-N = N-R (азо); р2CN2 R = Ph, tms, CF3 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Диазометан химическое соединение CH2N2, обнаруженный немецким химиком Ганс фон Пехманн в 1894 году. Это простейший диазосоединение. В чистом виде при комнатной температуре это чрезвычайно чувствительный взрывоопасный желтый цвет. газ; таким образом, он почти повсеместно используется в качестве решения в диэтиловый эфир. Состав является популярным метилирующий агент в лаборатории, но он слишком опасен для использования в промышленных масштабах без специальных мер предосторожности.[4] Использование диазометана было значительно сокращено за счет введения более безопасного и эквивалентного реагента. триметилсилилдиазометан.[5]
Использовать
Для безопасности и удобства диазометан всегда готовят по мере необходимости в виде раствора в эфир и используется как таковой. Он преобразует карбоновые кислоты в их метил сложные эфиры. Считается, что реакция протекает через перенос протона от карбоновой кислоты к диазометану с образованием метилдиазониевого катиона, который немедленно реагирует с карбоксилат-ионом с образованием метилового эфира и газообразного азота. Поскольку требуется перенос протона и ограничение скорости, эта реакция демонстрирует высокую специфичность для карбоновых кислот по сравнению с менее кислыми кислородсодержащими функциональными группами, такими как спирты и фенолы.

В более специализированных областях применения диазометан и гомологи используются в Синтез Арндта-Эйстера и Бюхнер – Куртиус – Шлоттербек реакция на омологацию.[6][7]

Диазометан реагирует с спирты или фенолы в присутствии трифторид бора (BF3) давать метил эфиры.
Диазометан также часто используется в качестве карбен источник. С готовностью принимает участие в 1,3-диполярные циклоприсоединения.
Подготовка

Диазометан получают гидролизом эфирного раствора N-метилнитрозамид с водным основанием. Традиционный предшественник N-нитрозо-N-метилмочевина, но это соединение само по себе несколько нестабильно, и в настоящее время такие соединения, как N-метил-N '-нитро-N-нитрозогуанидин (MNNG) и N-метил-N-нитрозо-п-толуолсульфонамид (Диазальд)[8] являются предпочтительными.[9]
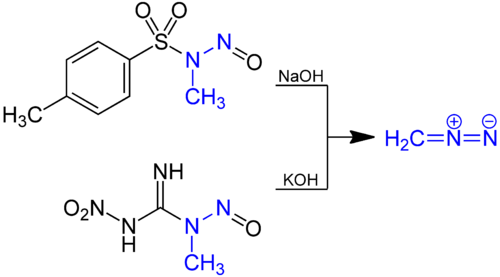 Общие способы получения диазометана.
Общие способы получения диазометана.
CH2N2 реагирует с базовыми растворами D2O, чтобы дать дейтерированную производную CD2N2.[10]
Концентрация CH2N2 можно определить любым из двух удобных способов. Лечится избытком бензойная кислота в холоде Et2О. Не отреагировал бензойная кислота затем титрованный со стандартным NaOH. В качестве альтернативы, концентрация CH2N2 в Et2O можно определить спектрофотометрически на 410 нм, где его коэффициент экстинкции, ε, равно 7,2.[нужна цитата ]Концентрация диазометана в газовой фазе может быть определена с помощью фотоакустическая спектроскопия.[4]
Родственные соединения
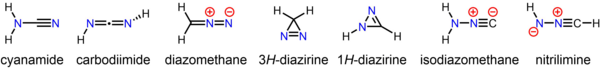
Диазометан одновременно изомерный и изоэлектронный с более стабильным цианамид, но они не могут взаимно превращаться. Было получено много замещенных производных диазометана:
- Очень стабильный (CF3)2CN2 (2-диазо-1,1,1,3,3,3-гексафторпропан; т.кип. 12–13 ° C),[11]
- Ph2CN2 (диазодифенилметан; m.p. 29–30 ° С).[12]
- (CH3)3SiCHN2 (триметилсилилдиазометан ), который коммерчески доступен в виде раствора и так же эффективен, как CH2N2 на метилирование.[13]
- PhC (H) N2, жидкость красного цвета, т.кип. <25 ° C при 0,1 мм рт.[14]
Безопасность
Диазометан токсичен при вдыхании, попадании на кожу или в глаза (TLV 0,2 ppm). Симптомы включают дискомфорт в груди, головную боль, слабость и, в тяжелых случаях, коллапс.[15] Симптомы могут проявиться позже. Сообщалось о случаях смерти от отравления диазометаном. В одном случае лабораторный работник съел гамбургер возле дымового очага, где он производил большое количество диазометана, и умер через четыре дня от молниеносной пневмонии.[16] Как и любой другой алкилирующий агент ожидается, что он будет канцерогенным, но такие опасения затмеваются его серьезной острой токсичностью.
CH2N2 может взорваться при контакте с острыми краями, такими как стыки матового стекла или даже царапины на стеклянной посуде.[17] Стеклянную посуду следует осмотреть перед использованием, а подготовка должна проходить за защитным экраном. В продаже имеются специализированные комплекты для приготовления диазометана с полированными пламенем стыками.
Компаунд взрывается при нагревании выше 100 ° C, под воздействием интенсивного света, щелочных металлов или сульфата кальция. При использовании этого состава настоятельно рекомендуется использовать защиту от взрыва.
Доказательства концепции были выполнены с микрофлюидика, в котором непрерывный синтез в точке использования из N-метил-N-нитрозомочевина и 0,93 M гидроксида калия в воде с последующей конверсией в точке использования с бензойная кислота, что приводит к 65% выходу сложного метилбензоатного эфира в течение нескольких секунд при температурах от 0 до 50 ° C. Выход был лучше, чем в капиллярных условиях; микрофлюидикам приписывают «подавление горячих точек, низкую задержку, изотермические условия и интенсивное перемешивание».[18]
Изомеры
Стабильное соединение цианамид, минорный таутомер которого карбодиимид, представляет собой изомер диазометана. Менее стабильные, но все же выделяемые изомеры диазометана включают циклические 3ЧАС-диазирин и изоцианоамин (изодиазометан ).[19][20] Кроме того, родитель нитрилимин наблюдалась в условиях матричной изоляции.[21]
использованная литература
- ^ ICSC 1256 - ДИАЗОМЕТАН
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0182". Национальный институт охраны труда и здоровья (NIOSH).
- ^ «Диазометан». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б Проктор, Ли Д .; Уорр, Энтони Дж. (Ноябрь 2002 г.). «Разработка непрерывного процесса промышленного производства диазометана». Исследования и разработки в области органических процессов. 6 (6): 884–892. Дои:10.1021 / op020049k.
- ^ Шиоири, Такаюки; Аояма, Тоёхико; Сноуден, Тимоти (2001). «Триметилсилилдиазометан». Энциклопедия реагентов для органического синтеза. Энциклопедия реагентов для органического синтеза e-EROS. Дои:10.1002 / 047084289X.rt298.pub2. ISBN 0471936235.
- ^ Buchner, E .; Курций, Т. (1885). "Synthese von Ketonsäureäthern aus Aldehyden und Diazoessigäther". Berichte der Deutschen Chemischen Gesellschaft. 18 (2): 2371–2377. Дои:10.1002 / cber.188501802118.
- ^ Шлоттербек, Ф. (1907). «Превращение альдегидов и кетонов через диазометан». Berichte der Deutschen Chemischen Gesellschaft. 40: 479–483. Дои:10.1002 / cber.19070400179.
- ^ "Synthese und Stoffwissen". Organic-btc-ilmenaus Webseite! (на немецком). Получено 2020-11-02.
- ^ Рид, Дональд Э .; Джеймс А. Мур (1961). «ДИАЗОМЕТАН». Органический синтез. 41: 16. Дои:10.15227 / orgsyn.041.0016.
- ^ П. Г. Гассман; У. Дж. Гринли (1988). «Дидейтеродиазометан». Органический синтез.; Коллективный объем, 6, п. 432
- ^ У. Дж. Миддлтон; Д. М. Гейл (1988). «Бис (Трифторметил) диазометан». Органический синтез.; Коллективный объем, 6, п. 161
- ^ Л. И. Смит; К. Л. Ховард (1955). "Дифенилдиазометан"". Органический синтез.; Коллективный объем, 3, п. 351
- ^ Т. Шиоири; Т. Аояма; С. Мори. «Триметилсилилдиазометан». Органический синтез.; Коллективный объем, 8, п. 612
- ^ X. Creary (1990). «Пиролиз солей тозилгидразона: фенидиазометаны». Органический синтез.; Коллективный объем, 7, п. 438
- ^ Мьюир, Г. Д. (ред.) 1971, Опасности в химической лаборатории, Королевский институт химии, Лондон.
- ^ Левинн, Э. «Отравление диазометаном: отчет о смертельном случае при вскрытии», Американский журнал медицинских наук, 1949, 218, 556-562.
- ^ de Boer, Th. J .; Бакер, Х. Дж. (1956). «ДИАЗОМЕТАН». Органический синтез. 36: 16. Дои:10.15227 / orgsyn.036.0016.
- ^ Владимир Решетиловский (13.09.2013). Микрореакторы в препаративной химии: практические аспекты биотехнологии, нанотехнологий, катализа и др.. Вайли. п. 6–15. ISBN 9783527652914.
- ^ Ансельм, Ж.-П. (1977-05-01). "Новый взгляд на изодиазометан. N-аминоизонитрилы". Журнал химического образования. 54 (5): 296. Дои:10.1021 / ed054p296. ISSN 0021-9584.
- ^ Ансельм, Дж. П. (1966-11-01). «Химия изодиазометана». Журнал химического образования. 43 (11): 596. Дои:10.1021 / ed043p596. ISSN 0021-9584.
- ^ Комплексные трансформации органических функциональных групп II. Катрицки, Алан Р., Тейлор, Ричард Дж. К. (1-е изд.). Амстердам: Эльзевир. 2005 г. ISBN 9780080523477. OCLC 213375246.CS1 maint: другие (ссылка на сайт)
внешние ссылки
- MSDS диазометан
- CDC - Карманный справочник NIOSH по химической опасности
- Технический бюллетень Sigmaaldrich (PDF)
- Сигма-Олдрич применение диазометана и коммерческая доступность прекурсора (диазальда)
- Реакция Бюхнера – Курциуса – Шлоттербека @ Институт химии, Скопье, Македония
- Идентификация артефактов (побочных продуктов) в реакциях диазометана и триметилсилилдиазометана


