Диаграмма Эллингема - Ellingham diagram
An Диаграмма Эллингема представляет собой график, показывающий температурную зависимость стабильности соединений. Этот анализ обычно используется для оценки легкости восстановления металла. оксиды и сульфиды. Эти диаграммы были впервые построены Гарольд Эллингем в 1944 г.[1] В металлургия, диаграмма Эллингема используется для предсказания равновесной температуры между металл, это окись, и кислород - и, соответственно, реакции металла с сера, азот, и другие неметаллы. Диаграммы полезны для прогнозирования условий, при которых руда сведется к его металлу. Анализ термодинамический в природе и игнорирует кинетика реакции. Таким образом, процессы, которые, согласно диаграмме Эллингема, могут быть благоприятными, могут быть медленными.
Термодинамика
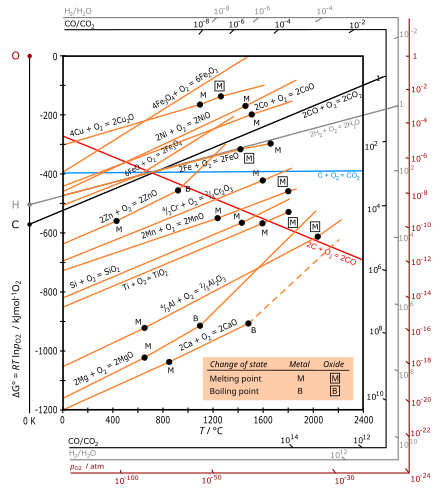
Диаграммы Эллингема представляют собой особую графическую форму принципа, согласно которому термодинамический возможность реакции зависит от знака ΔG, Свободная энергия Гиббса изменение, равное ΔH - TΔS, где ΔH - энтальпия изменение и ΔS - энтропия изменять.
Диаграмма Эллингема показывает Свободная энергия Гиббса изменение (ΔG) для каждой реакции окисления в зависимости от температуры. Для сравнения различных реакций все значения ΔG относятся к реакции одного и того же количества кислорода, выбранного как один моль O (1⁄2 моль О
2) некоторыми авторами[2] и одна родинка О
2 другими.[3] Показанная диаграмма относится к 1 моль О
2, так что, например, линия окисления хрома показывает ΔG для реакции4⁄3 Cr (s) + О
2(г) →2⁄3 Cr
2О
3(s), что является2⁄3 молярной энергии Гиббса образования ΔGж°(Cr
2О
3, с).
В обычно используемых диапазонах температур металл и оксид находятся в конденсированном состоянии (твердом или жидком), а кислород представляет собой газ с гораздо большей молярной энтропией. Для окисления каждого металла преобладающий вклад в изменение энтропии (ΔS) - это удаление1⁄2 моль О
2, так что ΔS отрицательна и примерно одинакова для всех металлов. Наклон участков [2] поэтому положительный для всех металлов, причем ΔG всегда становится более отрицательным с понижением температуры, а линии для всех оксидов металлов приблизительно параллельны. Поскольку эти реакции являются экзотермическими, они всегда возможны при более низких температурах. При достаточно высокой температуре знак ΔG может измениться (стать положительным) и оксид может самопроизвольно восстановиться до металла, как показано для Ag и Cu.
Для окисления углерода красная линия соответствует образованию CO: C (s) +1⁄2 О
2(g) → CO (g) с увеличением количества молей газа, что приводит к положительному ΔS и отрицательному наклону. Синяя линия для образования CO
2 приблизительно горизонтально, так как реакция C (s) + О
2(г) → CO
2(g) оставляет количество молей газа неизменным, так что ΔS мало.
Как и в случае любого предсказания химической реакции, основанного исключительно на термодинамический основания, спонтанная реакция может быть очень медленной, если на одной или нескольких стадиях пути реакции энергии активации EА.
Если присутствуют два металла, необходимо учитывать два состояния равновесия. Оксид с более отрицательным ΔG будет образован, а другой оксид восстановлен.
Особенности схемы
- Кривые на диаграммах Эллингема образования оксидов металлов представляют собой в основном прямые линии с положительным наклоном. Наклон пропорционален ΔS, который практически не зависит от температуры.
- Чем ниже положение линии металла на диаграмме Эллингема, тем выше стабильность его оксида. Например, линия для Al (окисление алюминий ) оказывается ниже, чем для Fe (образование Fe
2О
3). - Стабильность оксидов металлов снижается с повышением температуры. Сильно нестабильные оксиды, такие как Ag
2О и HgO легко подвергаются термическому разложению. - Образование свободной энергии углекислый газ (CO
2) практически не зависит от температуры, а монооксид углерода (CO) имеет отрицательный наклон и пересекает CO
2 линия около 700 ° C. Согласно Реакция Будуара, монооксид углерода является преобладающим оксидом углерода при более высоких температурах (выше примерно 700 ° C), и чем выше температура (выше 700 ° C), тем более эффективным является углерод-восстановитель (восстановитель). - Если сравнить кривые для двух металлов при данной температуре, то металл с более низкой свободной энергией Гиббса окисления на диаграмме будет восстанавливать оксид с более высокой свободной энергией Гиббса образования. Например, металлический алюминий может восстанавливать оксид железа до металлического железа, причем сам алюминий окисляется до оксида алюминия. (Эта реакция используется в термит.)
- Чем больше зазор между любыми двумя линиями, тем выше эффективность восстановителя, соответствующего нижней линии.
- Пересечение двух линий подразумевает окислительно-восстановительное равновесие. Восстановление с использованием данного восстановителя возможно при температурах выше точки пересечения, где линия ΔG этого восстановителя ниже на диаграмме, чем линия восстанавливаемого оксида металла. В точке пересечения изменение свободной энергии реакции равно нулю, ниже этой температуры оно положительно, и оксид металла стабилен в присутствии восстановителя, а выше точки пересечения энергия Гиббса отрицательна, и оксид может быть уменьшенный.
Восстановители
В промышленных процессах восстановление оксидов металлов часто осуществляется путем карботермическая реакция с использованием угля в качестве восстановителя. Углерод доступен дешево как каменный уголь, который может быть преобразован в кокс. Когда углерод вступает в реакцию с кислородом, он образует газообразные оксиды. монооксид углерода и углекислый газ, поэтому термодинамика его окисления отличается от таковой для металлов: его окисление имеет более отрицательную ΔG при более высоких температурах (выше 700 ° C). Таким образом, углерод может служить Восстановитель. Используя это свойство, восстановление металлов можно проводить как двойное редокс реакция при относительно низкой температуре.
Использование диаграмм Эллингема
Основное применение диаграмм Эллингема находится в добывающая металлургия промышленность, где он помогает выбрать лучший восстановитель для различных руд в процессе добычи, очистки и настройки сорта при производстве стали. Он также помогает направлять очистку металлов, особенно удаление микроэлементов. Процесс прямого восстановления для получения железа твердо основан на диаграммах Эллингема, которые показывают, что водород сам по себе может восстанавливать оксиды железа до металла.
Восстановитель гематита
В плавка железной руды, гематит снижается в верхней части печи, где температура находится в диапазоне 600-700 ° C. Диаграмма Эллингема показывает, что в этом диапазоне оксид углерода действует как более сильный восстановитель, чем углерод, поскольку процесс
- 2 СО + О
2 → 2 CO
2
имеет более отрицательное изменение свободной энергии, чем процесс:
- 2 С + О
2 → 2 КО.
В верхней части доменной печи гематит восстанавливается за счет CO (образуется путем окисления кокса ниже, при более высоких температурах) даже в присутствии углерода - хотя это в основном связано с тем, что кинетика реакции газообразного CO с рудой лучше. .
Восстановитель для оксида хрома-углерода использовать нельзя.
Кривая Эллингема для реакции 2C (s) + О
2(g) → 2CO (g) наклоняется вниз и опускается ниже кривых для всех металлов. Следовательно, углерод обычно может действовать как восстановитель для всех оксидов металлов при очень высоких температурах. Но хром, образующийся при таких температурах, реагирует с углеродом с образованием его карбида, который придает нежелательные свойства полученному металлическому хрому. Следовательно, при высоких температурах снижение оксид хрома, углерод использовать нельзя.
Алюмино термический процесс

Кривая Эллингема для алюминий лежит ниже кривых большинства металлов, таких как хром, утюг и др. Этот факт указывает на то, что алюминий может быть использован в качестве восстановителя оксидов всех этих металлов. Этот результат иллюстрируется следующим образом:
Свободные энергии образования оксид хрома (III) и оксид алюминия на моль потребленного кислорода составляют -541 кДж и -827 кДж соответственно. Это следующие процессы:
(1)
(2)
Второе уравнение минус первое уравнение дает:
(3)
Таким образом, оксид алюминия более стабилен, чем оксид хрома (по крайней мере, при нормальных температурах, и фактически вплоть до температур разложения оксидов). Поскольку изменение свободной энергии Гиббса отрицательно, алюминий может восстанавливать оксид хрома.
В пирометаллургия, алюминий используется в качестве восстановителя в алюмотермическом процессе или термит процесс извлечения хрома и марганца путем восстановления их оксидов.
Расширения к другим газофазным реакциям
Концепция построения графиков свободных энергий реакции различных элементов с данным газофазным реагентом может быть расширена за пределы реакций окисления. Оригинальная статья Эллингема, в которой прямо говорится о восстановлении как кислорода, так и серы в металлургических процессах,[1] и предполагал использование таких диаграмм для других соединений, включая хлориды, карбиды и сульфаты. Эта концепция обычно полезна для изучения сравнительной стабильности соединений в диапазоне парциальных давлений и температур. Построение диаграммы Эллингема особенно полезно при изучении стабильности соединений в присутствии восстановителя. Диаграммы Эллингема теперь доступны для бромидов, хлоридов, фторидов, гидридов, йодидов, нитридов, оксидов, сульфидов, селенидов и теллуридов.
Рекомендации
- ^ а б Эллингем, Х. Дж. Т. (1944), «Восстанавливаемость оксидов и сульфидов в металлургических процессах», J. Soc. Chem. Ind. (Лондон), 63 (5): 125, Дои:10.1002 / jctb.5000630501.
- ^ а б Аткинс, Питер; де Паула, Хулио (2006), Физическая химия: термодинамика и кинетика (8-е изд.), W.H. Фримен, стр. 215, ISBN 0716785676. Эта ссылка показывает диаграмму в перевернутом виде с уменьшением ΔG ° вверх.
- ^ Схема эллингема и интерактивная диаграмма (Кембриджский университет )
внешняя ссылка
- Интерактивные диаграммы Эллингема в Государственный университет Сан-Хосе
- Схема эллингема и интерактивная диаграмма (Кембриджский университет )





