Палладий на угле - Palladium on carbon
| Имена | |
|---|---|
| Название ИЮПАК Палладий | |
| Другие имена Палладий на угле, Pd / C, Pd-C | |
| Идентификаторы | |
3D модель (JSmol ) | |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| Pd | |
| Молярная масса | 106.42 |
| Внешность | Черный порошок |
| Растворимость | Царская водка |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Палладий на угле, часто называемый Pd / C, это форма палладий используется как катализатор.[1] Металл поддержанный на Активированный уголь чтобы максимально площадь поверхности и Мероприятия.
Использует
Гидрирование
Палладий на угле используется для каталитических гидрогенизация в органический синтез. Примеры включают восстановительное аминирование,[2] восстановление карбонила, восстановление нитросоединений, то редукция иминов и базисов Шиффа[1] и реакции дебензилирования.
Гидрогенолиз
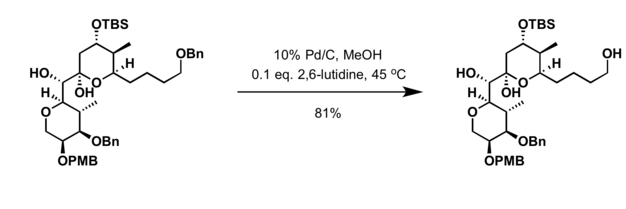
Палладий на угле является обычным катализатором гидрогенолиз. Такие реакции полезны в стратегиях снятия защиты. Особенно распространенными субстратами для гидрогенолиза являются бензиловые эфиры:[3]
Другие лабильные заместители также подвержены расщеплению этим реагентом. [4]
Реакции сцепления
Палладий на угле также используется для реакции сочетания. Примеры включают Сузуки реакция и Стилле реакция.[5]
Подготовка
Решение хлорид палладия и соляная кислота сочетается с водный приостановка Активированный уголь. Затем палладий (II) восстанавливают добавлением формальдегида.[6] Содержание палладия обычно составляет от 5% до 10%. Часто смесь катализаторов хранят влажной.
Смотрите также
- Палладий черный
- Платина на угле
- Диоксид платины
- Оксид родия-платины
- Катализатор Линдлара
- Никель Ренея
- Урушибара никель
Рекомендации
- ^ а б Нисимура, Шигео (2001). Справочник по гетерогенному каталитическому гидрированию для органического синтеза (1-е изд.). Нью-Йорк: Wiley-Interscience. С. 34–38. ISBN 9780471396987.
- ^ Романелли, Майкл Г .; Беккер, Эрнест I. (1967). «Этилп-диметиламинофенилацетат». Органический синтез. 47: 69. Дои:10.15227 / orgsyn.047.0069.
- ^ Smith, Amos B .; Чжу, Вэньюй; Шираками, Шохей; Сфуггатакис, Крис; Даути, Виктория А .; Bennett, Clay S .; Сакамото, Ясухару (01.03.2003). «Полный синтез (+) - Спонгистатина 1. Эффективная конструкция второго поколения усовершенствованной соли EF Виттига, объединения фрагментов и окончательной разработки». Органические буквы. 5 (5): 761–764. Дои:10.1021 / ol034037a. ISSN 1523-7060. PMID 12605509.
- ^ Musliner, Уолтер Дж .; Гейтс младший, Джон У. (1971). «Дегидроксилирование фенолов; гидрогенолиз фенольных эфиров: бифенил». Органический синтез. 51: 82. Дои:10.15227 / orgsyn.051.0082.
- ^ Liebeskind, Lanny S .; Пенья-Кабрера, Эдуардо (2000). «Стилловые взаимодействия, катализируемые палладием на угле с CuI в качестве сокатализатора: синтез 2- (4'-ацетилфенил) тиофена». Органический синтез. 77: 138. Дои:10.15227 / orgsyn.077.0135.
- ^ Мозинго, Ральф (1946). «Палладиевые катализаторы». Органический синтез. 26: 77–82. Дои:10.15227 / orgsyn.026.0077. PMID 20280763.