Гидрирование - Hydrogenation

(1) Реагенты: адсорбированный на поверхности катализатора и H2 диссоциирует.
(2) Атом H связан с одним атомом C. Другой атом C все еще прикреплен к поверхности.
(3) Второй атом C связывается с атомом H. Молекула покидает поверхность.
| Тип процесса | Химическая |
|---|---|
| Промышленный сектор (ы) | Пищевая промышленность, нефтехимическая промышленность, фармацевтический промышленность, сельское хозяйство |
| Основные технологии или подпроцессы | Различные катализаторы на основе переходных металлов, технология высокого давления |
| Сырье | Ненасыщенный субстраты и водород или доноры водорода |
| Товары) | Насыщенные углеводороды и производные |
| Изобретатель | Поль Сабатье |
| Год изобретения | 1897 |
Гидрирование это химическая реакция между молекулярными водород (ЧАС2) и другое соединение или элемент, обычно в присутствии катализатор Такие как никель, палладий или же платина. Этот процесс обычно используется для уменьшать или же насыщать органические соединения. Гидрирование обычно представляет собой добавление пар водород атомы молекуле, часто алкен. Катализаторы необходимы для использования реакции; некаталитическое гидрирование происходит только при очень высоких температурах. Гидрирование снижает двойной и тройной облигации в углеводороды.[1]
Процесс
Гидрирование состоит из трех компонентов: ненасыщенный субстрат, водород (или источник водорода) и, обязательно, катализатор. В снижение реакция проводится при различных температурах и давлениях в зависимости от субстрата и активности катализатора.
Связанные или конкурирующие реакции
Те же катализаторы и условия, которые используются для реакций гидрирования, также могут привести к изомеризация из алкены из снг[требуется разъяснение ] к перев. Этот процесс представляет большой интерес, поскольку технология гидрогенизации генерирует большую часть транс-жиры в продуктах питания (см. § Пищевая промышленность ниже). Реакция, при которой связи разрываются при добавлении водорода, называется гидрогенолиз, реакция, которая может происходить с углерод-углеродным и углерод-гетероатомом (кислород, азот или же галоген ) облигации. Некоторые гидрогенизации полярных связей сопровождаются гидрогенолизом.
Источники водорода
Для гидрирования очевидным источником водорода является H2 сам газ, который обычно коммерчески доступен в среде хранения баллона под давлением. В процессе гидрогенизации часто используется более 1 атмосферы H.2, как правило, подается из цилиндров и иногда дополняется «подкачивающими насосами». Газообразный водород промышленно производят из углеводородов с помощью процесса, известного как паровой риформинг.[2] Для многих приложений водород переносится от молекул-доноров, таких как муравьиная кислота, изопропанол и дигидроантрацен.[3] Эти доноры водорода подвергаются дегидрирование до соответственно диоксида углерода, ацетона и антрацена. Эти процессы называются перенос гидрирования.
Субстраты
Важной характеристикой гидрирования алкенов и алкинов, как гомогенно, так и гетерогенно катализированных версий, является то, что присоединение водорода происходит с "синхронное дополнение ", причем водород поступает с наименее затрудненной стороны.[4] Эта реакция может быть проведена на множестве различных функциональные группы.
| Субстрат | Товар | Комментарии | Теплота гидрирования (кДж / моль)[5] |
|---|---|---|---|
| р2C = CR '2 (алкен ) | р2ЧКПЧ2 (алкан) | большое применение - производство маргарин | От −90 до −130 |
| RC≡CR ' (алкин ) | RCH2CH2Р' (алкан) | полугидрирование дает СНГ-RHC = CHR ' | −300 (для полного гидрирования) |
| RCHO (альдегид ) | RCH2ОЙ (первичный спирт) | часто нанимает перенос гидрирования | От −60 до −65 |
| р2CO (кетон ) | р2CHOH (вторичный спирт) | часто нанимает перенос гидрирования | От −60 до −65 |
| RCO2Р' (сложный эфир ) | RCH2OH + R'OH (два спирта) | часто применяется к производству жирные спирты | От −25 до −105 |
| RCO2ЧАС (карбоновая кислота ) | RCH2ОЙ (первичный спирт) | применимо к жирным спиртам | От −25 до −75 |
| РНО2 (нитро ) | RNH2 (амин) | основное приложение анилин[6][7] | −550 |
Катализаторы
За редкими исключениями H2 не реагирует с органическими соединениями в отсутствие металлических катализаторов. Ненасыщенный субстрат хемосорбированный на катализатор, причем большинство участков покрыто подложкой. В гетерогенных катализаторах водород образует поверхностные гидриды (M-H), из которых водород может переноситься на хемосорбированный субстрат. Платина, палладий, родий, и рутений образуют высокоактивные катализаторы, которые работают при более низких температурах и более низких давлениях H2. Катализаторы из неблагородных металлов, особенно на основе никель (Такие как Никель Ренея и Урушибара никель ) также были разработаны как экономичные альтернативы, но они часто работают медленнее или требуют более высоких температур. Компромисс между активностью (скоростью реакции) и стоимостью катализатора и стоимостью устройства, необходимого для использования высоких давлений. Обратите внимание, что гидрирование, катализируемое никелем Ренея, требует высоких давлений:[8][9]
Катализаторы обычно делятся на два широких класса: гомогенные катализаторы и гетерогенные катализаторы. Гомогенные катализаторы растворяются в растворителе, содержащем ненасыщенный субстрат. Гетерогенные катализаторы - это твердые вещества, которые суспендированы в одном растворителе с субстратом или обработаны газообразным субстратом.
Гомогенные катализаторы
Некоторые хорошо известные гомогенные катализаторы указаны ниже. Это координационные комплексы которые активируют как ненасыщенный субстрат, так и H2. Чаще всего эти комплексы содержат металлы платиновой группы, особенно Rh и Ir.
- Гомогенные катализаторы гидрирования и их прекурсоры

Дихлортрис (трифенилфосфин) рутений (II) предкатализатор на основе рутения.

Катализатор Крэбтри представляет собой высокоактивный катализатор, содержащий иридий.

Rh2Cl2(треска)2 является предшественником многих гомогенных катализаторов.

(S) -iPr-PHOX представляет собой типичный хелатирующий фосфиновый лиганд, используемый при асимметричном гидрировании.

Гомогенные катализаторы также используются в асимметричном синтезе путем гидрирования прохиральных субстратов. Ранней демонстрацией этого подхода было катализируемое Rh гидрирование енамидов как предшественников препарата L-DOPA.[10] Для достижения асимметричного восстановления эти катализаторы делают хиральными за счет использования хиральных дифосфиновых лигандов.[11] Катализируемое родием гидрирование также использовалось в производстве гербицидов S-метолахлора, в котором используется лиганд типа Josiphos (называемый Xyliphos).[12] В принципе асимметричное гидрирование может катализироваться хиральными гетерогенными катализаторами,[13] но этот подход остается больше любопытством, чем полезной технологией.
Гетерогенные катализаторы
Гетерогенные катализаторы гидрирования более распространены в промышленности. В промышленности катализаторы гидрирования драгоценных металлов осаждают из раствора в виде тонкого порошка на носитель, который представляет собой дешевый, объемный, пористый, обычно гранулированный материал, такой как Активированный уголь, глинозем, карбонат кальция или же сульфат бария.[14] Например, платину на угле получают восстановлением платинохлористоводородная кислота на месте в углероде. Примеры этих катализаторов 5% рутений на Активированный уголь, или 1% платина на глинозем. Катализаторы из неблагородных металлов, такие как Никель Ренея, обычно намного дешевле и не нуждаются в поддержке. Кроме того, в лаборатории без подложки (массивные) катализаторы из драгоценных металлов, такие как платиновый черный до сих пор используются, несмотря на стоимость.
Как и в случае с гомогенными катализаторами, активность регулируется путем изменения окружающей среды вокруг металла, т.е. сфера координации. Разные лица кристаллического гетерогенного катализатора проявляют различные активности, например. Это можно изменить путем смешивания металлов или использования различных методов приготовления. Аналогичным образом на гетерогенные катализаторы влияют их носители.
Во многих случаях весьма эмпирические модификации включают выборочные «яды». Таким образом, тщательно подобранный катализатор можно использовать для гидрирования некоторых функциональных групп, не затрагивая другие, например, для гидрирования алкенов без контакта с ароматическими кольцами или для селективного гидрирования алкины в алкены с помощью Катализатор Линдлара. Например, когда катализатор палладий размещен на сульфат бария а затем обработали хинолин, полученный катализатор восстанавливает алкины только до алкенов. Катализатор Линдлара применялся для превращения фенилацетилен к стирол.[15]
- Иллюстративные гидрирования
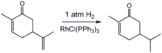
Селективное гидрирование менее затрудненной алкеновой группы в Carvone с использованием гомогенного катализатора (Катализатор Уилкинсона ).[16]

Частичное гидрирование фенилацетилен с использованием Катализатор Линдлара.
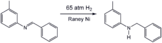
Гидрирование имина с использованием Никель Ренея катализатор, популярный гетерогенный катализатор.

Частичное гидрирование резорцин производное с использованием катализатора Ренея-Никеля.

Гидрирование малеиновая кислота к Янтарная кислота.[17]
Передача гидрогенизации
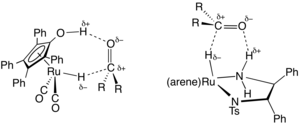
Передача гидрогенизации использует другие молекулы донора водорода вместо H2 сам. Эти реагенты, которые также могут служить растворители для реакции включают гидразин, дигидронафталин, дигидроантрацен, изопропанол, и муравьиная кислота.[18] Реакция включает внешнесферный механизм.
В органический синтез, перенос гидрирования полезен для асимметричного восстановления полярных ненасыщенных субстратов, таких как кетоны, альдегиды, и имины. Гидрирование полярных субстратов, таких как кетоны и альдегиды, обычно требует гидрогенизации с переносом, по крайней мере, для реакций, в которых используются гомогенные катализаторы. Эти катализаторы легко образуются в хиральных формах, что является основой асимметричного гидрирования кетонов.
Электролитическое гидрирование
Полярный субстраты, такие как нитрилы можно гидрогенизировать электрохимически, с помощью протонные растворители и восстанавливающие эквиваленты в качестве источника водорода.[19]
Термодинамика и механизм
Присоединение водорода к двойным или тройным связям в углеводороды это тип редокс реакция, которая может быть термодинамически выгодной. Например, добавление водорода к этену имеет Свободная энергия Гиббса изменение -101 кДж · моль−1, что очень экзотермический.[11] Например, при гидрировании растительных масел и жирных кислот выделяемого тепла, составляющего около 25 ккал на моль (105 кДж / моль), достаточно для повышения температуры масла на 1,6–1,7 ° C на 1 моль. йодное число уронить.
Однако скорость реакции для большинства реакций гидрирования незначительна в отсутствие катализаторов. В механизм гидрирования алкенов и алкинов, катализируемого металлами, широко изучены.[20] Прежде всего маркировка изотопов с помощью дейтерий подтверждает региохимия дополнения:
- RCH = CH2 + D2 → RCHDCH2D
Гетерогенный катализ
На твердых телах принятый механизм - Horiuti-Поланьи механизм:[21][22]
- Связывание ненасыщенной связи и диссоциация водорода на атомарный водород на катализаторе
- Добавление одного атома водорода; этот шаг обратимый
- Добавление второго атома; эффективно необратимо в условиях гидрогенизации.
На второй стадии образующийся металло-промежуточный продукт представляет собой насыщенное соединение, которое может вращаться и затем разрушаться, снова отделяя алкен от катализатора. Следовательно, контакт с катализатором гидрирования обязательно вызывает цис-транс-изомеризация, поскольку изомеризация является термодинамически выгодной. Это проблема при частичном гидрировании, в то время как при полном гидрировании образуются транс-алкен со временем гидрируется.
Для ароматических субстратов первую связь труднее всего гидрогенизировать из-за потери свободной энергии за разрыв ароматической системы. Продуктом этого является циклогексадиен, который чрезвычайно активен и не может быть выделен; в условиях снижения, достаточного для прекращения ароматизации, он немедленно восстанавливается до циклогексена. В циклогексен обычно немедленно восстанавливается до полностью насыщенного циклогексана, но специальные модификации катализаторов (такие как использование воды, препятствующей растворителю, на рутении) могут сохранить часть циклогексена, если это желаемый продукт.
Гомогенный катализ
Во многих процессах гомогенного гидрирования[23] металл связывается с обоими компонентами с образованием промежуточного алкен-металла (H)2 сложный. Предполагается, что общая последовательность реакций представляет собой следующую или связанную последовательность шагов:
- связывание водорода с образованием дигидридного комплекса через окислительная добавка (перед окислительным добавлением H2 это формирование дигидрогенный комплекс ):
- LпM + H2 → LпMH2
- связывание алкена:
- LпM (η2ЧАС2) + CH2= CHR → Lп-1MH2(CH2= CHR) + L
- перенос одного атома водорода от металла к углероду (миграционная вставка)
- Lп-1MH2(CH2= CHR) → Lп-1M (H) (CH2-CH2Р)
- перенос второго атома водорода от металла к алкильной группе с одновременной диссоциацией алкана («восстановительное отщепление»)
- Lп-1M (H) (CH2-CH2R) → Lп-1M + CH3-CH2р
Неорганические субстраты
Гидрогенизация азота с получением аммиака широко проводится Габер – Бош процесс, потребляющий примерно 1% мировое энергоснабжение.
Кислород можно частично гидрогенизировать, чтобы получить пероксид водорода, хотя этот процесс не получил коммерческого применения. Одна из трудностей заключается в том, чтобы не дать катализаторам вызвать разложение перекиси водорода с образованием воды.[24][25]
Промышленное применение
Каталитическое гидрирование находит широкое применение в промышленности. Чаще всего для промышленного гидрирования используют гетерогенные катализаторы.[2]
Пищевая промышленность
Наиболее масштабным применением гидрогенизации является обработка растительные масла.[2] Типичные растительные масла получают из полиненасыщенные жирные кислоты (содержащие более одного углерод-углерод двойная связь ). Гидрирование уменьшает или устраняет эти двойные связи. Цель состоит в том, чтобы превратить жидкие масла в твердые или полутвердые жиры, которые могут заменить масло сливочное и сокращение в пастах, конфетах, выпечке и других продуктах.[26]
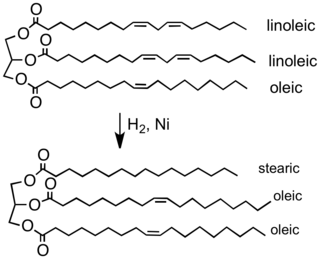 Частичное гидрирование типичного растительного масла до типичного компонента маргарина. В этом процессе удаляется большая часть двойных связей C = C, что повышает температуру плавления продукта.
Частичное гидрирование типичного растительного масла до типичного компонента маргарина. В этом процессе удаляется большая часть двойных связей C = C, что повышает температуру плавления продукта.
Нефтехимическая промышленность
В нефтехимических процессах гидрирование используется для превращения алкенов и ароматических углеводородов в насыщенные алканы (парафины) и циклоалканы (нафтены), которые менее токсичны и обладают меньшей реакционной способностью. Что касается жидкого топлива, которое иногда хранится в течение длительного времени на воздухе, насыщенные углеводороды обладают превосходными свойствами хранения. С другой стороны, алкены имеют тенденцию образовывать гидропероксиды, которые могут образовывать смолы, мешающие работе оборудования для работы с топливом. Например, минеральный скипидар обычно гидрогенизируется. Гидрокрекинг тяжелых остатков в дизельное топливо - еще одно применение. В изомеризация и каталитический риформинг процессы, некоторое давление водорода поддерживается до гидрогенолиз кокс образуются на катализаторе и предотвращают его накопление.
Органическая химия
Гидрирование - полезный способ превращения ненасыщенных соединений в насыщенные производные. Субстраты включают не только алкены и алкины, но также альдегиды, имины и нитрилы,[27] которые превращаются в соответствующие насыщенные соединения, то есть спирты и амины. Таким образом, алкилальдегиды, которые могут быть синтезированы с оксо процесс из монооксид углерода и алкен могут быть превращены в спирты. Например. 1-пропанол производится из пропиональдегида, получаемого из этилена и окиси углерода. Ксилит, а полиол, получается путем гидрогенизации сахара ксилоза, альдегид. Первичные амины могут быть синтезированы гидрирование нитрилов, в то время как нитрилы легко синтезируются из цианида и подходящего электрофила. Например, изофорондиамин, предшественник полиуретан мономер изофорондиизоцианат, получают из изофороннитрила тандемным гидрированием нитрила / восстановительным аминированием аммиаком, при котором гидрогенизация превращает как нитрил в амин, так и имин, образованный из альдегида и аммиака, в другой амин.
Гидрирование угля
История
Гетерогенно-каталитическое гидрирование
Самое раннее гидрирование - гидрирование платина катализированный добавление водорода к кислороду в Лампа доберейнера, устройство поступило в продажу еще в 1823 году. Французский химик Поль Сабатье считается отцом процесса гидрирования. В 1897 году, основываясь на более ранней работе Джеймс Бойс, американский химик, занимающийся производством мыла, он обнаружил, что следы никеля катализируют присоединение водорода к молекулам газообразных углеводородов в том, что сейчас известно как Сабатье процесс. Для этой работы Сабатье поделился 1912 г. Нобелевская премия по химии. Вильгельм Норманн был награжден патентом в Германии в 1902 году и в Великобритании в 1903 году на гидрирование жидких масел, что положило начало тому, что сейчас стало всемирной промышленностью. Коммерчески важный Процесс Габера – Боша, впервые описанный в 1905 году, включает гидрирование азота. в Процесс Фишера-Тропша, как сообщалось в 1922 году, окись углерода, которую легко получить из угля, гидрогенизируется до жидкого топлива.
В 1922 году Вурхиз и Адамс описали устройство для проведения гидрирования при давлении выше одной атмосферы.[28] Шейкер Парра, первый продукт, позволяющий проводить гидрирование с использованием повышенных давлений и температур, был коммерциализирован в 1926 году на основе исследований Вурхиса и Адамса и до сих пор широко используется. В 1924 г. Мюррей Рэйни разработали тонкоизмельченную форму никеля, который широко используется для катализа реакций гидрирования, таких как превращение нитрилов в амины или производство маргарина.
Гомогенно-каталитическое гидрирование
В 1930-х годах Кальвин обнаружил, что комплексы меди (II) окисляют H2. 1960-е годы стали свидетелями развития четко определенных гомогенные катализаторы с использованием комплексов переходных металлов, например, Катализатор Уилкинсона (RhCl (PPh3)3). Вскоре было обнаружено, что катионные Rh и Ir катализируют гидрирование алкенов и карбонилов.[29] В 1970-х годах асимметричное гидрирование было продемонстрировано в синтезе L-ДОПА, а в 1990-е годы были изобретены Асимметричное гидрирование Нойори.[30] На развитие гомогенного гидрирования повлияла работа, начатая в 1930-х и 1940-х годах над оксо процесс и Полимеризация Циглера-Натта.
Безметалловое гидрирование
Для большинства практических целей для гидрирования требуется металлический катализатор. Однако гидрирование может происходить от некоторых доноров водорода без катализаторов, иллюстративными донорами водорода являются диимид и изопропоксид алюминия, последнее проиллюстрировано Редукция Меервейна – Понндорфа – Верлея. Некоторые безметалловые каталитические системы были исследованы в академических исследованиях. Одна такая система для уменьшения кетоны состоит из терт-бутанол и трет-бутоксид калия и очень высокие температуры.[31] Изображенная ниже реакция описывает гидрирование бензофенон:
А химическая кинетика изучать[32] обнаружил, что эта реакция первый заказ во всех трех реагентах, предполагая циклический 6-членный переходное состояние.
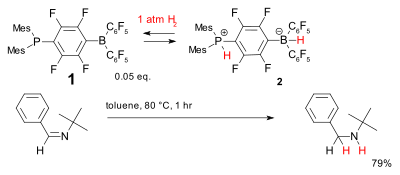
Другая система безметаллового гидрирования основана на фосфин -боран, сложный 1, который был назван разочарованная пара Льюиса. Он обратимо принимает дигидроген при относительно низких температурах с образованием фосфоний борат 2 что может уменьшить простое затрудненное имины.[33]
Уменьшение нитробензол к анилин как сообщается, катализируется фуллерен, его моноанион, атмосферный водород и ультрафиолетовый свет.[34]
Оборудование, используемое для гидрирования
У современного лабораторного химика есть три основных варианта оборудования для гидрогенизации:
- Периодическое гидрирование в атмосферных условиях
- Периодическое гидрирование при повышенной температуре и / или давлении[35]
- Проточное гидрирование
Периодическое гидрирование в атмосферных условиях
Первоначальная и до сих пор широко применяемая форма гидрирования в учебных лабораториях, этот процесс обычно осуществляется путем добавления твердого катализатора в раствор. круглодонная колба растворенного реагента, который был удален с использованием азот или же аргон газ и герметизация смеси резиновым проницаемым уплотнением. Затем газообразный водород подается из H2-заполненный воздушный шар. Полученную трехфазную смесь перемешивают, чтобы способствовать перемешиванию. Можно контролировать поглощение водорода, что может быть полезно для мониторинга процесса гидрирования. Это достигается либо с помощью градуированной трубки, содержащей окрашенную жидкость, обычно водную. сульфат меди или с датчики для каждого реакционного сосуда.
Периодическое гидрирование при повышенной температуре и / или давлении
Поскольку многие реакции гидрирования, такие как гидрогенолиз из защитные группы и сокращение ароматный системы работают крайне медленно при атмосферной температуре и давлении, популярны системы под давлением. В этих случаях катализатор добавляют к раствору реагента в инертной атмосфере в сосуд под давлением. Водород добавляется непосредственно из баллона или встроенного лабораторного источника водорода, и суспензия под давлением механически встряхивается для перемешивания, или используется прядильная корзина.[35] Последние достижения в электролиз технологии привели к развитию генераторы водорода высокого давления, которые производят водород из воды под давлением до 100 бар (1400 фунтов на квадратный дюйм). Также можно использовать тепло, поскольку давление компенсирует связанное с этим снижение растворимости газа.
Проточное гидрирование
Проточное гидрирование стало популярным методом на стенде и все в большей степени масштабируется. Этот метод включает непрерывный поток разбавленного потока растворенного реагента над неподвижным слоем катализатора в присутствии водорода. Используя установленные ВЭЖХ Технология позволяет применять давление от атмосферного до 1450 фунтов на квадратный дюйм (100 бар). Также могут использоваться повышенные температуры. В лабораторных условиях системы используют ряд предварительно упакованных катализаторов, что исключает необходимость взвешивания и фильтрации. пирофорный катализаторы.
Промышленные реакторы
Каталитическое гидрирование проводится в трубчатый поршневой реактор (PFR) набита катализатором на носителе. Давление и температура обычно высокие, хотя это зависит от катализатора. Загрузка катализатора обычно намного ниже, чем при лабораторном периодическом гидрировании, и к металлу добавляют различные промоторы или используются смешанные металлы для повышения активности, селективности и стабильности катализатора. Никель широко используется, несмотря на его низкую активность из-за его низкой стоимости по сравнению с драгоценными металлами.
Газожидкостные индукционные реакторы (гидрогенизатор) также используются для каталитического гидрирования.[36]
Смотрите также
Рекомендации
- ^ Худлицкий, Милош (1996). Уменьшение в органической химии. Вашингтон, округ Колумбия.: Американское химическое общество. п. 429. ISBN 978-0-8412-3344-7.
- ^ а б c Пол Н. Райландер, «Гидрирование и дегидрирование» в Энциклопедия промышленной химии Ульмана, Wiley-VCH, Weinheim, 2005. Дои:10.1002 / 14356007.a13_487
- ^ Бек, Шэй. Металлоорганическая химия. Великобритания, EDTECH, 2019.
- ^ Продвинутая органическая химия Джерри Марч 2-е издание
- ^ Скотт Д. Барницки «Синтетические органические химические вещества» в Справочнике по промышленной химии и биотехнологии под редакцией Джеймса А. Кента, Нью-Йорк: Springer, 2012. 12-е изд. ISBN 978-1-4614-4259-2.
- ^ «Гидрирование нитробензола с использованием полимерных комплексов Ru (III) в качестве катализатора». Ind. Jr. Of Chem. Технология. 7: 280. 2000.
- ^ Патель, Д. Р. (1998). «Гидрирование нитробензола с использованием полимерных закрепленных комплексов Pd (II) в качестве катализатора». Журнал молекулярного катализа. 130 (1–2): 57. Дои:10.1016 / с 1381-1169 (97) 00197-0.
- ^ С.Ф.Х. Аллен и Джеймс Ваналлан (1955). «м-Тойлибензиламин». Органический синтез.; Коллективный объем, 3, п. 827
- ^ А. Б. Меклер, С. Рамачандран, С. Сваминатан и Мелвин С. Ньюман (1973). «2-Метил-1,3-Циклогександион». Органический синтез.CS1 maint: несколько имен: список авторов (связь); Коллективный объем, 5, п. 743
- ^ Ноулз, В. С. (март 1986 г.). «Применение металлоорганического катализа для промышленного производства L-DOPA». Журнал химического образования. 63 (3): 222. Bibcode:1986JChEd..63..222K. Дои:10.1021 / ed063p222.
- ^ а б Аткинс, Питер У. (2010). Неорганическая химия Шрайвера и Аткинса (5-е изд.). Нью-Йорк: W.H. Freeman and Co., стр. 696. ISBN 978-1-4292-1820-7.
- ^ Блазер, Ганс-Ульрих; Пугин, Бенуа; Шпиндлер, Феликс; Томмен, Марк (декабрь 2007 г.). «От хирального переключателя к портфелю лигандов для асимметричного катализа». Отчеты о химических исследованиях. 40 (12): 1240–1250. Дои:10.1021 / ar7001057. PMID 17715990.
- ^ Маллат, Т .; Orglmeister, E .; Байкер, А. (2007). «Асимметричный катализ на хиральных металлических поверхностях». Химические обзоры. 107 (11): 4863–90. Дои:10.1021 / cr0683663. PMID 17927256.
- ^ «Платиновые гетерогенные катализаторы - Альфа Эзар». www.alfa.com. В архиве из оригинала 18 января 2018 г.. Получено 28 апреля 2018.
- ^ Х. Линдлар и Р. Дюбуи (1973). «Палладиевый катализатор частичного восстановления ацетиленов». Органический синтез.; Коллективный объем, 5, п. 880
- ^ С. Роберт Э. Айрлэнд и П. Бей (1988). «Гомогенное каталитическое гидрирование: дигидрокарвон». Органический синтез.; Коллективный объем, 6, п. 459
- ^ Амоа, Квеси (2007). «Каталитическое гидрирование малеиновой кислоты при умеренных давлениях, лабораторная демонстрация». Журнал химического образования. 84 (12): 1948. Дои:10.1021 / ed084p1948.
- ^ van Es, T .; Стаскун, Б. "Альдегиды из ароматических нитрилов: 4-Формилбензолсульфонамид" Орг. Synth., Сб. Vol. 6, стр. 631 (1988). (Статья В архиве 2007-09-27 на Wayback Machine )
- ^ Наварро, Даниэла Мария ду Амарал Феррас; Наварро, Марсело (2004). «Каталитическое гидрирование органических соединений без подачи H2: электрохимическая система». Журнал химического образования. 81 (9): 1350. Дои:10.1021 / ed081p1350.
- ^ Кубас, Г. Дж., "Металл дигидроген и комплексы σ-связей", Kluwer Academic / Plenum Publishers: Нью-Йорк, 2001
- ^ Галлезо, Пьер. «Гидрирование - гетерогенное» в Энциклопедии катализа, том 4, изд. Хорват, И.Т., John Wiley & Sons, 2003.
- ^ Хориути, Юро; Поланьи, М. (1934). «Обменные реакции водорода на металлических катализаторах». Труды общества Фарадея. 30: 1164. Дои:10.1039 / TF9343001164.
- ^ Johannes G. de Vries, Cornelis J. Elsevier, ред. Справочник по гомогенному гидрированию Wiley-VCH, Weinheim, 2007. ISBN 978-3-527-31161-3
- ^ Норитака Мизуно Габриэле Ченти, Сиглинда Ператонер, Сальваторе Абате «Прямой синтез пероксида водорода: последние достижения» в Современный гетерогенный окислительный катализ: конструкция, реакции и характеристика 2009, Вайли-ВЧ. Дои:10.1002 / 9783527627547.ch8
- ^ Эдвардс, Дженнифер К .; Сольсона, Бенджамин; N, Эдвин Нтайнджуа; Карли, Альберт Ф .; Герцинг, Эндрю А .; Кили, Кристофер Дж .; Хатчингс, Грэм Дж. (20 февраля 2009 г.). «Отключение гидрирования пероксида водорода в процессе прямого синтеза». Наука. 323 (5917): 1037–1041. Bibcode:2009Научный ... 323.1037E. Дои:10.1126 / science.1168980. PMID 19229032.
- ^ Иэн П. Фриман «Маргарины и шортенинг» в Энциклопедия промышленной химии Ульмана, 2005, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a16_145
- ^ Werkmeister, Svenja; Юнге, Катрин; Беллер, Матиас (2 февраля 2014 г.). «Каталитическое гидрирование сложных эфиров, амидов и нитрилов карбоновых кислот с гомогенными катализаторами». Исследования и разработки в области органических процессов. 18 (2): 289–302. Дои:10.1021 / op4003278.

- ^ «Архивная копия» (PDF). В архиве (PDF) из оригинала от 10.09.2008. Получено 2008-08-05.CS1 maint: заархивированная копия как заголовок (связь)
- ^ Schrock, Ричард Р .; Осборн, Джон А. (апрель 1976 г.). «Каталитическое гидрирование с использованием катионных комплексов родия. I. Эволюция каталитической системы и гидрирование олефинов». Журнал Американского химического общества. 98 (8): 2134–2143. Дои:10.1021 / ja00424a020.
- ^ К. Петтинари, Ф. Маркетти, Д. Мартини «Металлические комплексы как катализаторы гидрирования» Комплексная координационная химия II, 2004, том 9. С. 75–139. Дои:10.1016 / B0-08-043748-6 / 09125-8
- ^ Walling, Cheves .; Боллыки, Ласло. (1964). «Гомогенное гидрирование в отсутствие катализаторов переходных металлов». Журнал Американского химического общества. 86 (18): 3750. Дои:10.1021 / ja01072a028.
- ^ Беркессель, Альбрехт; Schubert, Thomas J. S .; Мюллер, Томас Н. (2002). "Гидрирование без катализатора переходного металла: О механизме катализируемого основанием гидрирования кетонов". Журнал Американского химического общества. 124 (29): 8693–8. Дои:10.1021 / ja016152r. PMID 12121113.
- ^ Чейз, Престон А .; Уэлч, Грегори С.; Юрка, Тител; Стефан, Дуглас В. (2007). «Безметалловое каталитическое гидрирование». Angewandte Chemie International Edition. 46 (42): 8050–3. Дои:10.1002 / anie.200702908. PMID 17696181.
- ^ Ли, Баоцзюнь; Сюй, Чжэн (2009). «Неметаллический катализатор для активации молекулярного водорода с сопоставимой способностью к каталитическому гидрированию с катализатором из благородных металлов». Журнал Американского химического общества. 131 (45): 16380–2. Дои:10.1021 / ja9061097. PMID 19845383.
- ^ а б Адамс, Роджер; Вурхиз В. (1928). «Аппарат каталитического восстановления». Органический синтез. 8: 10. Дои:10.15227 / orgsyn.008.0010.
- ^ Joshi, J.B .; Pandit, A.B .; Шарма, М. (1982). «Газожидкостные реакторы с механическим перемешиванием». Химическая инженерия. 37 (6): 813. Дои:10.1016/0009-2509(82)80171-1.
дальнейшее чтение
- Джанг ES, Юнг М.Ю., Мин ДБ (2005). «Гидрирование жирных кислот с низким содержанием транс и высоким содержанием конъюгированных жирных кислот» (PDF). Комплексные обзоры в области пищевой науки и безопасности пищевых продуктов. 1. Архивировано из оригинал (PDF) 17 декабря 2008 г.
- примеры гидрирования из органических синтезов:
- ранние работы по переносу гидрирования:
- Davies, R. R .; Ходжсон, Х. Х. (1943). «76. Каталитическое восстановление муравьиной кислотой под давлением. Часть II. Сравнение меди и никеля как катализаторов». J. Chem. Soc.: 281. Дои:10.1039 / jr9430000281.
- Легкая, Б. Е .; Браун, Р. К. (1960). «Восстановление моногалогенированных нитробензолов гидразином и никелем Ренея. Удобное получение галогенированных анилинов». Может. J. Chem. 38 (12): 2363. Дои:10.1139 / v60-320.
- Кун, Л. П. (1951). «Каталитическое восстановление гидразином». Варенье. Chem. Soc. 73 (4): 1510. Дои:10.1021 / ja01148a029.
- Куммеров, Фред Август; Куммеров, Жан М. (2008). Холестерин не убьет вас, но трансжиры могут. Траффорд. ISBN 978-1-4251-3808-0.
внешняя ссылка
- "Магия гидро", Популярная механика, Июнь 1931 г., стр. 107–109 - первая статья для широкой публики о гидрогенизации нефти, добытой в 1930-х гг.





![Гидрирование азота { Displaystyle { ce {{ underset {азот} {N { Equiv} N}} + { underset {водород наверху (200 атм)} {3H2}} -> [{ ce {Fe катализатор}} ] [350-550 ^ { circ} { ce {C}}] { underset {аммиак} {2NH3}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2dd5645111a3ad991987a7b9e10599029c287e98)