Растворитель - Solvent

А растворитель (от латинский solvō, "ослабить, развязать, решить") - это вещество, которое растворяет растворенное вещество, в результате чего решение. Растворителем обычно является жидкость, но также может быть твердое вещество, газ или сверхкритическая жидкость. Количество растворенного вещества, которое может раствориться в определенном объеме растворителя, зависит от температура. В основном растворители используются в красках, средствах для снятия краски, чернилах и в химической чистке.[1] Конкретное использование для органический растворители в сухая чистка (например. тетрахлорэтилен ), в качестве разбавители для краски (например. толуол, скипидар ), как жидкости для снятия лака и растворители клея (ацетон, метилацетат, ацетат этила ), в средствах для удаления пятен (например, гексан, петролейный эфир), в моющих средствах (цитрусовые терпены ) И в духи (этиловый спирт ). Вода - растворитель для полярные молекулы и наиболее распространенный растворитель, используемый живыми существами; все ионы и белки в клетке растворены в воде внутри клетки. Растворители находят различное применение в химической, фармацевтический, нефтяной и газовой промышленности, в том числе в химический синтез и процессы очистки.
Решения и сольватация
Когда одно вещество растворенный в другой, решение сформирован.[2] Это противоположно ситуации, когда соединения нерастворимый как песок в воде. В растворе все ингредиенты равномерно распределены на молекулярном уровне и не остается остатков. Смесь растворителя и растворенного вещества состоит из одного фаза со всеми молекулами растворенного вещества, встречающимися как сольваты (растворитель-растворенный комплексы ), в отличие от отдельных непрерывных фаз, как в суспензиях, эмульсиях и других типах смесей, не являющихся растворами. Способность одного соединения растворяться в другом известна как растворимость; если это происходит во всех пропорциях, это называется смешивающийся.
Помимо перемешивания, вещества в растворе взаимодействуют друг с другом на молекулярном уровне. Когда что-то растворяется, молекулы растворителя располагаются вокруг молекулы растворенного вещества. Теплопередача участвует и энтропия увеличивается, делая решение более термодинамически стабильнее, чем растворенное вещество и растворитель по отдельности. Такое расположение опосредуется соответствующими химическими свойствами растворителя и растворенного вещества, такими как водородная связь, дипольный момент и поляризуемость.[3] Сольватация не вызывает химической реакции или изменений химической конфигурации растворенного вещества. Однако сольватация напоминает координационный комплекс реакция образования, часто со значительной энергетикой (теплота сольватации и энтропия сольватации) и, таким образом, далека от нейтрального процесса.
Когда одно вещество растворяется в другом, образуется раствор. Раствор представляет собой гомогенную смесь, состоящую из растворенного вещества, растворенного в растворителе. Растворенное вещество - это вещество, которое растворяется, а растворитель - растворяющая среда. Растворы могут быть образованы с использованием многих различных типов и форм растворенных веществ и растворителей.
Классификация растворителей
Растворители можно условно разделить на две категории: полярный и неполярный. Особый случай Меркурий, решения которой известны как амальгамы; также другие металлические решения существуют жидкие при комнатной температуре. Как правило, диэлектрическая постоянная Количество растворителя позволяет приблизительно определить полярность растворителя. На сильную полярность воды указывает ее высокая диэлектрическая проницаемость 88 (при 0 ° C).[4] Растворители с диэлектрической проницаемостью менее 15 обычно считаются неполярными.[5] Диэлектрическая проницаемость измеряет тенденцию растворителя частично компенсировать напряженность электрического поля заряженная частица погрузился в него. Это сокращение затем сравнивается с напряженность поля заряженной частицы в вакууме.[5] Эвристически диэлектрическую проницаемость растворителя можно рассматривать как его способность снижать эффективность растворенного вещества. внутренний заряд. Как правило, диэлектрическая проницаемость растворителя является приемлемым показателем способности растворителя растворять обычные ионные соединения, например соли.
Другие шкалы полярности
Диэлектрическая проницаемость - не единственная мера полярности. Поскольку растворители используются химиками для проведения химических реакций или наблюдения за химическими и биологическими явлениями, требуются более конкретные меры полярности. Большинство этих мер чувствительны к химической структуре.
В Грюнвальд – Винштейн мY шкала измеряет полярность с точки зрения влияния растворителя на накопление положительного заряда растворенного вещества во время химической реакции.
Kosower с Z шкала измеряет полярность с точки зрения влияния растворителя на УФ -максимумы поглощения соли, обычно пиридиний йодид или пиридиний цвиттерион.[6]
Номер донора и шкала акцептора донора измеряет полярность с точки зрения того, как растворитель взаимодействует с определенными веществами, например, сильным Кислота Льюиса или сильная база Льюиса.[7]
В Параметр Хильдебранда квадратный корень из плотность когезионной энергии. Его можно использовать с неполярными соединениями, но он не подходит для сложных химических процессов.
Краситель Рейхардта, а сольватохромный краситель, меняющий цвет в зависимости от полярности, дает шкалу EТ(30) значения. EТ - энергия перехода между основным состоянием и нижним возбужденным состоянием в ккал / моль, а (30) идентифицирует краситель. Другая, примерно коррелированная шкала (EТ(33)) можно определить как Нильский красный.
Полярность, дипольный момент, поляризуемость и водородная связь растворителя определяет, какой тип соединения он способен растворяться и с какими другими растворителями или жидкими соединениями он смешивающийся. Обычно полярные растворители лучше всего растворяют полярные соединения, а неполярные растворители лучше всего растворяют неполярные соединения: «подобное растворяется в подобном». Сильно полярные соединения, такие как сахара (например, сахароза) или ионные соединения, такие как неорганический соли (например. столовая соль ) растворяются только в очень полярных растворителях, таких как вода, в то время как сильно неполярные соединения, такие как масла или же воск растворяются только в очень неполярных органических растворителях, таких как гексан. Точно так же вода и гексан (или же уксус и растительное масло) не смешивающийся друг с другом и быстро разделятся на два слоя даже после хорошего встряхивания.
Полярность может быть разделена на разные вклады. Например, Параметры Камлета-Тафта диполярность / поляризуемость (π *), водородно-связывающая кислотность (α) и основность водородных связей (β). Их можно рассчитать по сдвигу длин волн 3–6 различных сольватохромных красителей в растворителе, обычно включая Краситель Рейхардта, нитроанилин и диэтилнитроанилин. Другой вариант, параметры Хансена, разделяют плотность энергии когезии на вклады дисперсии, полярности и водородных связей.
Полярный протон и полярный апротический
Растворители с диэлектрической проницаемостью (точнее, относительная статическая диэлектрическая проницаемость ) более 15 (т.е. полярные или поляризуемые) можно разделить на протический и апротический. Сольват протонных растворителей анионы (отрицательно заряженные растворенные вещества) сильно через водородная связь. Вода - протонный растворитель. Апротонные растворители, такие как ацетон или же дихлорметан имеют тенденцию иметь большие дипольные моменты (разделение частичных положительных и частичных отрицательных зарядов в одной и той же молекуле) и сольватировать положительно заряженные частицы через их отрицательный диполь.[8] В химические реакции использование полярных протонных растворителей способствует SN1 механизм реакции, в то время как полярные апротонные растворители способствуют SN2 механизм реакции. Эти полярные растворители способны образовывать водородные связи с водой для растворения в воде, тогда как неполярные растворители не способны к прочным водородным связям.
Многокомпонентный
Многокомпонентные растворители появились после Второй мировой войны в СССР и продолжают использоваться и производиться в постсоветских странах.
Растворители
| Имя | Сочинение |
|---|---|
| Растворитель 645 | толуол 50%, бутилацетат 18%, этилацетат 12%, бутанол 10%, этанол 10%. |
| Растворитель 646 | толуол 50%, этиловый спирт 15%, бутанол 10%, бутил- или амилацетат 10%, этилцеллозольв 8%, ацетон 7%[9] |
| Растворитель 647 | бутилацетат или амилацетат 29,8%, ацетат этила 21,2%, бутанол 7,7%, толуол или пиробензол 41.3%[10] |
| Растворитель 648 | бутил ацетат 50%, этанол 10%, бутанол 20%, толуол 20%[11] |
| Растворитель 649 | этилцеллозольв 30%, бутанол 20%, ксилол 50% |
| Растворитель 650 | этилцеллозольв 20%, бутанол 30%, ксилол 50%[12] |
| Растворитель 651 | белый дух 90%, бутанол 10% |
| Растворитель КР-36 | бутилацетат 20%, бутанол 80% |
| Растворитель П-4 | толуол 62%, ацетон 26%, бутилацетат 12%. |
| Растворитель П-10 | ксилол 85%, ацетон 15%. |
| Растворитель П-12 | толуол 60%, бутилацетат 30%, ксилол 10%. |
| Растворитель П-14 | циклогексанон 50%, толуол 50%. |
| Растворитель П-24 | растворитель 50%, ксилол 35%, ацетон 15%. |
| Растворитель П-40 | толуол 50%, этилцеллозольв 30%, ацетон 20%. |
| Растворитель П-219 | толуол 34%, циклогексанон 33%, ацетон 33%. |
| Растворитель Р-3160 | бутанол 60%, этанол 40%. |
| Растворитель RCC | ксилол 90%, бутилацетат 10%. |
| Растворитель РМЛ | этанол 64%, этилцеллозольв 16%, толуол 10%, бутанол 10%. |
| Растворитель ПМЛ-315 | толуол 25%, ксилол 25%, бутилацетат 18%, этилцеллозольв 17%, бутанол 15%. |
| Растворитель ПК-1 | толуол 60%, бутилацетат 30%, ксилол 10%. |
| Растворитель ПК-2 | уайт-спирит 70%, ксилол 30%. |
| Растворитель RFG | этанол 75%, бутанол 25%. |
| Растворитель РЭ-1 | ксилол 50%, ацетон 20%, бутанол 15%, этанол 15%. |
| Растворитель РЕ-2 | Растворитель 70%, этанол 20%, ацетон 10%. |
| Растворитель РЭ-3 | растворитель 50%, этанол 20%, ацетон 20%, этилцеллозольв 10%. |
| Растворитель РЭ-4 | растворитель 50%, ацетон 30%, этанол 20%. |
| Растворитель ФК-1 (?) | абсолютный спирт (99,8%) 95%, этилацетат 5% |
Разбавители
| Имя | Сочинение |
|---|---|
| Разбавитель РКБ-1 | бутанол 50%, ксилол 50% |
| Разбавитель РКБ-2 | бутанол 95%, ксилол 5% |
| Разбавитель РКБ-3 | ксилол 90%, бутанол 10% |
| Разбавитель М | этанол 65%, бутилацетат 30%, этилацетат 5%. |
| Разбавитель П-7 | циклогексанон 50%, этанол 50%. |
| Разбавитель Р-197 | ксилол 60%, бутилацетат 20%, этилцеллозольв 20%. |
| Разбавитель WFD | толуол 50%, бутилацетат (или амилацетат) 18%, бутанол 10%, этанол 10%, этилацетат 9%, ацетон 3%. |
Физические свойства
Таблица свойств распространенных растворителей
Растворители сгруппированы в неполярный, полярный апротический, и полярный протический растворители, причем каждая группа упорядочена по возрастанию полярности. В характеристики растворители, превышающие водные, выделены жирным шрифтом.
| Растворитель | Химическая формула | Точка кипения[13] (° C) | Диэлектрическая постоянная[14] | Плотность (г / мл) | Дипольный момент (D ) |
|---|---|---|---|---|---|
Неполярный растворители | |||||
| Пентан |  CH3CH2CH2CH2CH3 | 36.1 | 1.84 | 0.626 | 0.00 |
| Циклопентан | 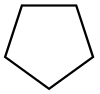 C5ЧАС10 | 49.2 | 1.97 | 0.751 | 0.00 |
| Гексан | 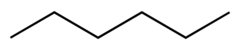 CH3CH2CH2CH2CH2CH3 | 69 | 1.88 | 0.655 | 0.00 |
| Циклогексан |  C6ЧАС12 | 80.7 | 2.02 | 0.779 | 0.00 |
| Бензол | 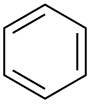 C6ЧАС6 | 80.1 | 2.3 | 0.879 | 0.00 |
| Тетрахлорметан | CCl4 | 76.7 | 2.3 | 1.5867 | 0.00 |
| Толуол | C6ЧАС5-CH3 | 111 | 2.38 | 0.867 | 0.36 |
| 1,4-диоксан |  C4ЧАС8О2 | 101.1 | 2.3 | 1.033 | 0.45 |
| Диэтиловый эфир |  CH3CH2-O-CH2CH3 | 34.6 | 4.3 | 0.713 | 1.15 |
| Хлороформ |  CHCl3 | 61.2 | 4.81 | 1.498 | 1.04 |
Полярный апротический растворители | |||||
| Дихлорметан (DCM) | 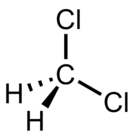 CH2Cl2 | 39.6 | 9.1 | 1.3266 | 1.60 |
| Тетрагидрофуран (THF) | 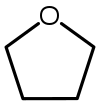 C4ЧАС8О | 66 | 7.5 | 0.886 | 1.75 |
| Ацетат этила |  CH3-C (= O) -O-CH2-CH3 | 77.1 | 6.02 | 0.894 | 1.78 |
| Ацетон |  CH3-C (= O) -CH3 | 56.1 | 21 | 0.786 | 2.88 |
| Диметилформамид (DMF) | 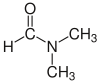 H-C (= O) N (CH3)2 | 153 | 38 | 0.944 | 3.82 |
| Ацетонитрил (MeCN) | CH3-C≡N | 82 | 37.5 | 0.786 | 3.92 |
| Диметилсульфоксид (ДМСО) |  CH3-S (= O) -CH3 | 189 | 46.7 | 1.092 | 3.96 |
| Нитрометан |  CH3-НЕТ2 | 100–103 | 35.87 | 1.1371 | 3.56 |
| Пропиленкарбонат |  C4ЧАС6О3 | 240 | 64.0 | 1.205 | 4.9 |
Полярный протический растворители | |||||
| Аммиак | 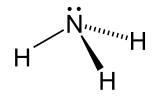 NH3 | -33.3 | 17 | 0.674 (при -33,3 ° C) | 1.42 |
| Муравьиная кислота | 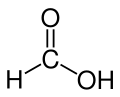 Н-С (= O) ОН | 100.8 | 58 | 1.21 | 1.41 |
| п-Бутанол | CH3CH2CH2CH2ОЙ | 117.7 | 18 | 0.810 | 1.63 |
| Изопропиловый спирт (IPA) | 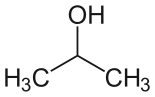 CH3-СН (-ОН) -СН3 | 82.6 | 18 | 0.785 | 1.66 |
| п-Пропанол |  CH3CH2CH2ОЙ | 97 | 20 | 0.803 | 1.68 |
| Этиловый спирт | CH3CH2ОЙ | 78.2 | 24.55 | 0.789 | 1.69 |
| Метанол | 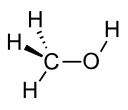 CH3ОЙ | 64.7 | 33 | 0.791 | 1.70 |
| Уксусная кислота |  CH3-С (= О) ОН | 118 | 6.2 | 1.049 | 1.74 |
| Вода |  H-O-H | 100 | 80 | 1.000 | 1.85 |
В ACS Green Chemistry Institute поддерживает инструмент для выбора растворителей на основе Анализ главных компонентов свойств растворителя.[15]
Значения параметра растворимости Хансена
Значения параметра растворимости Хансена[16][17] основаны на дисперсионные облигации (δD), полярные связи (δP) и водородные связи (δH). Они содержат информацию о межмолекулярных взаимодействиях с другими растворителями, а также с полимерами, пигментами, наночастицами и т. Д. Это позволяет создавать рациональные рецептуры, зная, например, что существует хорошее соответствие HSP между растворителем и полимером. Рациональные замены также могут быть сделаны для «хороших» растворителей (эффективных для растворения растворенного вещества), которые являются «плохими» (дорогими или опасными для здоровья или окружающей среды). В следующей таблице показано, что интуиция от «неполярного», «полярного апротонного» и «полярного протонного» выражается численно - «полярные» молекулы имеют более высокие уровни δP, а протонные растворители имеют более высокие уровни δH. Поскольку используются числовые значения, сравнения можно проводить рационально, сравнивая числа. Например, ацетонитрил гораздо более полярен, чем ацетон, но имеет немного меньшую водородную связь.
| Растворитель | Химическая формула | δD Дисперсия | δP Полярный | δH Водородная связь |
|---|---|---|---|---|
Неполярные растворители | ||||
| н-гексан | CH3CH2CH2CH2CH2CH3 | 14.9 | 0.0 | 0.0 |
| Бензол | C6ЧАС6 | 18.4 | 0.0 | 2.0 |
| Толуол | C6ЧАС5-CH3 | 18.0 | 1.4 | 2.0 |
| Диэтиловый эфир | CH3CH2-O-CH2CH3 | 14.5 | 2.9 | 4.6 |
| Хлороформ | CHCl3 | 17.8 | 3.1 | 5.7 |
| 1,4-диоксан | / -CH2-CH2-O-CH2-CH2-O- | 17.5 | 1.8 | 9.0 |
Полярные апротонные растворители | ||||
| Ацетат этила | CH3-C (= O) -O-CH2-CH3 | 15.8 | 5.3 | 7.2 |
| Тетрагидрофуран (THF) | / -CH2-CH2-O-CH2-CH2-\ | 16.8 | 5.7 | 8.0 |
| Дихлорметан | CH2Cl2 | 17.0 | 7.3 | 7.1 |
| Ацетон | CH3-C (= O) -CH3 | 15.5 | 10.4 | 7.0 |
| Ацетонитрил (MeCN) | CH3-C≡N | 15.3 | 18.0 | 6.1 |
| Диметилформамид (DMF) | H-C (= O) N (CH3)2 | 17.4 | 13.7 | 11.3 |
| Диметилсульфоксид (ДМСО) | CH3-S (= O) -CH3 | 18.4 | 16.4 | 10.2 |
Полярные протонные растворители | ||||
| Уксусная кислота | CH3-С (= О) ОН | 14.5 | 8.0 | 13.5 |
| п-Бутанол | CH3CH2CH2CH2ОЙ | 16.0 | 5.7 | 15.8 |
| Изопропанол | CH3-СН (-ОН) -СН3 | 15.8 | 6.1 | 16.4 |
| п-Пропанол | CH3CH2CH2ОЙ | 16.0 | 6.8 | 17.4 |
| Этиловый спирт | CH3CH2ОЙ | 15.8 | 8.8 | 19.4 |
| Метанол | CH3ОЙ | 14.7 | 12.3 | 22.3 |
| Муравьиная кислота | Н-С (= O) ОН | 14.6 | 10.0 | 14.0 |
| Вода | H-O-H | 15.5 | 16.0 | 42.3 |
Если по экологическим или другим причинам требуется растворитель или смесь растворителей для замены другого растворителя с эквивалентной растворимостью, замена может быть произведена на основе Параметры растворимости Хансена каждого. Значения для смесей приняты как средневзвешенные значений для чистых растворителей. Это можно рассчитать как методом проб и ошибок, таблица значений или программное обеспечение HSP.[16][17] Смесь 1: 1 толуол и 1,4 диоксан имеет значения δD, δP и δH 17,8, 1,6 и 5,5, сопоставимые со значениями хлороформ на уровне 17,8, 3,1 и 5,7 соответственно. Из-за опасности для здоровья, связанной с самим толуолом, можно найти другие смеси растворителей с использованием полного HSP набор данных.
Точка кипения
| Растворитель | Точка кипения (° C)[13] |
|---|---|
| этилендихлорид | 83.48 |
| пиридин | 115.25 |
| метилизобутилкетон | 116.5 |
| метиленхлорид | 39.75 |
| изооктан | 99.24 |
| сероуглерод | 46.3 |
| четыреххлористый углерод | 76.75 |
| о-ксилол | 144.42 |
Температура кипения является важным свойством, поскольку от нее зависит скорость испарения. Небольшие количества растворителей с низкой температурой кипения, например диэтиловый эфир, дихлорметан, или ацетон испарится за секунды при комнатной температуре, в то время как растворители с высокой точкой кипения, такие как вода или диметилсульфоксид нужны более высокие температуры, воздушный поток или нанесение вакуум для быстрого испарения.
- Низкокипящие: температура кипения ниже 100 ° C (температура кипения воды)
- Средние котлы: от 100 ° C до 150 ° C
- Высококипящие: выше 150 ° C
Плотность
Большинство органических растворителей имеют более низкую плотность чем вода, что означает, что они легче, чем вода, и образуют слой поверх нее. Важными исключениями являются большинство галогенированный растворители, такие как дихлорметан или же хлороформ опустится на дно емкости, оставив воду в качестве верхнего слоя. Это очень важно помнить, когда разделение соединения между растворителями и водой в разделительная воронка во время химического синтеза.
Часто, удельный вес цитируется вместо плотности. Удельный вес определяется как отношение плотности растворителя к плотности воды при той же температуре. Таким образом, удельный вес является безразмерным значением. Он легко сообщает, будет ли нерастворимый в воде растворитель плавать (SG <1,0) или тонуть (SG> 1,0) при смешивании с водой.
| Растворитель | Удельный вес[18] |
|---|---|
| Пентан | 0.626 |
| Петролейный эфир | 0.656 |
| Гексан | 0.659 |
| Гептан | 0.684 |
| Диэтиламин | 0.707 |
| Диэтиловый эфир | 0.713 |
| Триэтиламин | 0.728 |
| Трет-бутилметиловый эфир | 0.741 |
| Циклогексан | 0.779 |
| Трет-бутиловый спирт | 0.781 |
| Изопропанол | 0.785 |
| Ацетонитрил | 0.786 |
| Этиловый спирт | 0.789 |
| Ацетон | 0.790 |
| Метанол | 0.791 |
| Метилизобутилкетон | 0.798 |
| Изобутиловый спирт | 0.802 |
| 1-пропанол | 0.803 |
| Метилэтилкетон | 0.805 |
| 2-бутанол | 0.808 |
| Изоамиловый спирт | 0.809 |
| 1-бутанол | 0.810 |
| Диэтилкетон | 0.814 |
| 1-октанол | 0.826 |
| п-ксилол | 0.861 |
| м-ксилол | 0.864 |
| Толуол | 0.867 |
| Диметоксиэтан | 0.868 |
| Бензол | 0.879 |
| Бутил ацетат | 0.882 |
| 1-хлорбутан | 0.886 |
| Тетрагидрофуран | 0.889 |
| Ацетат этила | 0.895 |
| о-ксилол | 0.897 |
| Триамид гексаметилфосфора | 0.898 |
| 2-этоксиэтиловый эфир | 0.909 |
| N, N-диметилацетамид | 0.937 |
| Диметиловый эфир диэтиленгликоля | 0.943 |
| N, N-диметилформамид | 0.944 |
| 2-метоксиэтанол | 0.965 |
| Пиридин | 0.982 |
| Пропановая кислота | 0.993 |
| Вода | 1.000 |
| 2-метоксиэтилацетат | 1.009 |
| Бензонитрил | 1.01 |
| 1-метил-2-пирролидинон | 1.028 |
| Гексаметилфосфорамид | 1.03 |
| 1,4-диоксан | 1.033 |
| Уксусная кислота | 1.049 |
| Уксусный ангидрид | 1.08 |
| Диметилсульфоксид | 1.092 |
| Хлорбензол | 1.1066 |
| Оксид дейтерия | 1.107 |
| Этиленгликоль | 1.115 |
| Диэтиленгликоль гликоль | 1.118 |
| Пропиленкарбонат | 1.21 |
| Муравьиная кислота | 1.22 |
| 1,2-дихлорэтан | 1.245 |
| Глицерин | 1.261 |
| Сероуглерод | 1.263 |
| 1,2-дихлорбензол | 1.306 |
| Метиленхлорид | 1.325 |
| Нитрометан | 1.382 |
| 2,2,2-Трифторэтанол | 1.393 |
| Хлороформ | 1.498 |
| 1,1,2-трихлортрифторэтан | 1.575 |
| Тетрахлорметан | 1.594 |
| Тетрахлорэтилен | 1.623 |
Безопасность
Огонь
Большинство органических растворителей легко или легко воспламеняются в зависимости от их летучести. Исключение составляют некоторые хлорированные растворители, например дихлорметан и хлороформ. Смеси паров растворителей и воздуха могут взорваться. Пары растворителя тяжелее воздуха; они опускаются на дно и могут преодолевать большие расстояния почти в неразбавленном виде. Пары растворителя также можно найти в предположительно пустых бочках и банках, что создает вспышка огня опасность; следовательно, пустые емкости с летучими растворителями следует хранить открытыми и перевернутыми.
Обе диэтиловый эфир и сероуглерод имеют исключительно низкий температуры самовоспламенения которые значительно увеличивают риск возгорания, связанный с этими растворителями. Температура самовоспламенения сероуглерода ниже 100 ° C (212 ° F), поэтому такие предметы, как пар трубы лампочки, конфорки, и недавно погашенный горелки Бунзена способны воспламенить его пары.
Кроме того, некоторые растворители, такие как метанол, могут гореть очень горячим пламенем, которое может быть почти невидимым при некоторых условиях освещения.[19][20] Это может задержать или предотвратить своевременное распознавание опасного пожара до тех пор, пока пламя не перейдет на другие материалы.
Взрывоопасное образование перекиси
Эфиры подобно диэтиловый эфир и тетрагидрофуран (THF) может образовывать взрывоопасные органические пероксиды при воздействии кислорода и света. THF обычно более склонен к образованию таких пероксидов, чем диэтиловый эфир. Один из самых чувствительных растворителей - это диизопропиловый эфир, но все эфиры считаются потенциальными источниками перекиси.
Гетероатом (кислород ) стабилизирует образование свободный радикал который образован абстракцией водород атом другим свободным радикалом.[требуется разъяснение ] Образованный таким образом углерод-центрированный свободный радикал способен реагировать с молекулой кислорода с образованием пероксидного соединения. Процесс образования перекиси значительно ускоряется даже при слабом освещении, но может протекать медленно даже в темноте.
Если только осушитель используется, который может разрушить пероксиды, они будут концентрироваться во время дистилляция, из-за их более высоких точка кипения. Когда образуется достаточное количество пероксидов, они могут образовывать кристаллический, чувствительное к ударам твердое тело осадок у горлышка контейнера или бутылки. Незначительные механические нарушения, такие как царапание внутренней части сосуда или удаление отложений, простое закручивание крышки может обеспечить достаточную энергию для взрыва перекиси или взорвать. При быстром расходе свежих растворителей образование перекиси не представляет серьезной проблемы; они представляют собой большую проблему в лабораториях, которым могут потребоваться годы, чтобы закончить одну бутылку. Пользователи небольших объемов должны приобретать только небольшое количество пероксидных растворителей и регулярно утилизировать старые растворители.
Чтобы избежать взрывоопасного образования пероксида, эфиры следует хранить в герметичном контейнере, вдали от света, потому что и свет, и воздух могут способствовать образованию пероксида.[21]
Для обнаружения пероксида в эфире можно использовать ряд тестов; один - использовать комбинацию сульфат железа (II) и тиоцианат калия. Перекись способна окислять Fe2+ ион к Fe3+ ион, который затем образует темно-красный координационный комплекс с тиоцианат.
Пероксиды можно удалить промыванием кислым сульфатом железа (II), фильтрованием через глинозем, или же дистилляция из натрий /бензофенон. Оксид алюминия не разрушает пероксиды, а просто улавливает их, и от него необходимо утилизировать надлежащим образом. Преимущество использования натрия / бензофенона заключается в том, что влага и кислород также удаляются.[нужна цитата ]
Влияние на здоровье
Общие опасности для здоровья, связанные с воздействием растворителей, включают токсичность для нервной системы, повреждение репродуктивной системы, повреждение печени и почек, нарушение дыхания, рак и дерматит.[22]
Острое воздействие
Многие растворители могут привести к внезапной потере сознания, если вдохнул в больших количествах. Растворители, подобные диэтиловый эфир и хлороформ использовались в медицине как анестетики, успокаивающие, и снотворные длительное время. Этиловый спирт (зерновой спирт) широко используется и злоупотребляет психоактивный препарат. Диэтиловый эфир, хлороформ и многие другие растворители, например из бензин или клеем злоупотребляют в рекреационных целях нюхание клея, часто с вредными долгосрочными последствиями для здоровья, такими как нейротоксичность или же рак. Мошенническая подмена 1,5-пентандиол психоактивными 1,4-бутандиол субподрядчиком вызвало Bindeez отозвать продукт.[23] При попадании внутрь так называемые токсичные спирты (кроме этанола), такие как метанол, пропанол, и этиленгликоль метаболизируются в токсичные альдегиды и кислоты, вызывающие потенциально смертельный исход Метаболический ацидоз.[24] Обычно доступный спиртовой растворитель метанол может вызвать необратимую слепоту или смерть при проглатывании. Растворитель 2-бутоксиэтанол, используется в жидкости для гидроразрыва, может вызвать гипотония и метаболический ацидоз.[25]
Хроническое воздействие
Некоторые растворители, включая хлороформ и бензол общий ингредиент в бензин известны как канцерогенный, в то время как многие другие рассматриваются Всемирная организация здоровья вероятно, канцерогены. Растворители могут повредить внутренние органы, например печень, то почки, то нервная система, или мозг. Кумулятивные эффекты длительного или многократного воздействия растворителей называются хроническая энцефалопатия, вызванная растворителями (CSE).
Хроническое воздействие органических растворителей в рабочей среде может вызвать ряд неблагоприятных психоневрологических эффектов. Например, профессиональное воздействие органических растворителей было связано с увеличением числа художников, страдающих от алкоголизм.[26] Этанол имеет синергетический эффект при приеме в сочетании со многими растворителями; например, сочетание толуол /бензол а этанол вызывает большее тошнота /рвота чем любое вещество в отдельности.
Известно или предполагается, что многие растворители обладают катарактогенными свойствами, что значительно увеличивает риск развития катаракта в хрусталике глаза.[27] Воздействие растворителей также было связано с нейротоксическим повреждением, вызывающим потеря слуха[28][29] и цветовое зрение убытки.[30]
Загрязнение окружающей среды
Основной путь воздействия на здоровье - это разливы или утечки растворителей, которые достигают подстилающей почвы. Поскольку растворители легко мигрируют на значительные расстояния, создание широко распространенных Загрязнение почвы не редкость; это особенно опасно для здоровья, если водоносные горизонты под действием. Вторжение пара может произойти на объектах с обширным подземным загрязнением растворителями.[31][нужна цитата ]
Смотрите также
- Свободная энергия сольватации
- Растворители часто кипятят с обратным холодильником с подходящим осушитель перед перегонкой для удаления воды. Это может быть выполнено до химического синтеза, когда вода может помешать намеченной реакции.
- Список смешивающихся с водой растворителей
- Лиолюминесценция
- Гигиена труда
- Коэффициент распределения (бревно п) представляет собой меру дифференциальной растворимости соединения в двух растворителях.
- Решение
- Решение
- Системы растворителей существуют за пределами обычных органических растворителей: Сверхкритические жидкости, ионные жидкости и глубокие эвтектические растворители
- Водная модель
- Загрязнение воды
Рекомендации
- ^ Стоу, Дитер (2000). «Растворители». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a24_437.
- ^ Тиноко I, Зауэр К., Ван Дж.С. (2002). Физическая химия. Прентис Холл. п.134. ISBN 978-0-13-026607-1.
- ^ Лоури и Ричардсон, стр. 181–183.
- ^ Мальмберг CG, Мэриотт AA (январь 1956 г.). «Диэлектрическая проницаемость воды от 0 ° до 100 ° C». Журнал исследований Национального бюро стандартов. 56 (1): 1. Дои:10.6028 / jres.056.001.
- ^ а б Лоури и Ричардсон, стр. 177.
- ^ Kosower, E.M. (1969) "Введение в физико-органическую химию" Wiley: New York, p. 293
- ^ Гутманн V (1976). «Влияние растворителей на химическую активность металлоорганических соединений». Coord. Chem. Rev. 18 (2): 225. Дои:10.1016 / S0010-8545 (00) 82045-7.
- ^ Лоури и Ричардсон, стр. 183.
- ^ dcpt.ru Характеристики растворителя 646 (ru)
- ^ dcpt.ru Характеристики растворителя 647 (ru)
- ^ dcpt.ru Характеристики Растворителя 648 (ru)
- ^ dcpt.ru Характеристики Растворителя 650 (ru)
- ^ а б Свойства растворителя - точка кипения В архиве 14 июня 2011 г. Wayback Machine. Xydatasource.com. Проверено 26 января 2013 г.
- ^ Диэлектрическая постоянная В архиве 4 июля 2010 г. Wayback Machine. Macro.lsu.edu. Проверено 26 января 2013 г.
- ^ Diorazio, Louis J .; Хосе, Дэвид Р. Дж .; Адлингтон, Нил К. (2016). «На пути к более целостной структуре выбора растворителя». Исследования и разработки в области органических процессов. 20 (4): 760–773. Дои:10.1021 / acs.oprd.6b00015.
- ^ а б Эбботт С., Хансен К.М. (2008). Параметры растворимости Хансена на практике. Хансен-Растворимость. ISBN 978-0-9551220-2-6.
- ^ а б Хансен CM (январь 2002 г.). Параметры растворимости Хансена: руководство пользователя. CRC Press. ISBN 978-0-8493-7248-3.
- ^ Выбранные свойства растворителя - Удельный вес В архиве 14 июня 2011 г. Wayback Machine. Xydatasource.com. Проверено 26 января 2013 г.
- ^ Фаник Э. Р., Смит Л. Р., Бейнс ТМ (1 октября 1984 г.). «Добавки, связанные с безопасностью для метанольного топлива». Серия технических документов SAE. 1. Варрендейл, Пенсильвания. Дои:10.4271/841378. В архиве с оригинала от 12 августа 2017 года.
- ^ Андерсон Дж. Э., Мадьярл М. В., Зигл В. О. (1 июля 1985 г.). «О светимости пламени диффузии метанола и углеводородов». Наука и технология горения. 43 (3–4): 115–125. Дои:10.1080/00102208508947000. ISSN 0010-2202.
- ^ «Пероксиды и простые эфиры | Охрана окружающей среды, безопасность и управление рисками». www.uaf.edu. Получено 25 января 2018.
- ^ «Растворители». Управление по охране труда и технике безопасности. Министерство труда США. В архиве из оригинала 15 марта 2016 г.
- ^ Руд, Дэвид (7 ноября 2007 г.). «Национал: отзыв заказан на игрушку, которая превращается в наркотик». www.theage.com.au.
- ^ Краут Дж. А., Маллинз М. Е. (январь 2018 г.). «Токсичные спирты». Медицинский журнал Новой Англии. 378 (3): 270–280. Дои:10.1056 / NEJMra1615295. PMID 29342392. S2CID 36652482.
- ^ Хунг Т., Девитт CR, Мартц В., Шрайбер В., Холмс Д. Т. (июль 2010 г.). «Фомепизол не может предотвратить прогрессирование ацидоза при совместном употреблении 2-бутоксиэтанола и этанола». Клиническая токсикология. 48 (6): 569–71. Дои:10.3109/15563650.2010.492350. PMID 20560787. S2CID 23257894.
- ^ Lundberg I, Gustavsson A, Högberg M, Nise G (июнь 1992 г.). «Диагностика злоупотребления алкоголем и других психоневрологических расстройств среди маляров по сравнению с плотниками». Британский журнал промышленной медицины. 49 (6): 409–15. Дои:10.1136 / oem.49.6.409. ЧВК 1012122. PMID 1606027.
- ^ Райтта К., Хусман К., Тоссавайнен А. (август 1976 г.). «Смена линз у маляров, подвергшихся воздействию смеси органических растворителей». Albrecht von Graefes Archiv für Klinische und Experimentelle Ophthalmologie. Архив клинической и экспериментальной офтальмологии Альбрехта фон Грефе. 200 (2): 149–56. Дои:10.1007 / bf00414364. PMID 1086605. S2CID 31344706.
- ^ Кампо П., Мората ТК, Хонг О (апрель 2013 г.). «Химическое воздействие и потеря слуха». Болезнь-месяц. 59 (4): 119–38. Дои:10.1016 / j.disamonth.2013.01.003. ЧВК 4693596. PMID 23507352.
- ^ Джонсон AC, Мората TC (2010). «Воздействие химических веществ на рабочем месте и нарушение слуха. Северная группа экспертов по критериям документирования рисков для здоровья, связанных с химическими веществами» (PDF). Арбете оч Хэлса. 44: 177. В архиве (PDF) из оригинала от 4 июня 2016 г.
- ^ Мерглер Д., Блейн Л., Лагасе Дж. П. (1987). «Потеря цветового зрения, связанная с растворителем: индикатор повреждения нервной системы?». Международный архив гигиены труда и окружающей среды. 59 (4): 313–21. Дои:10.1007 / bf00405275. PMID 3497110. S2CID 33855389.
- ^ Форанд С.П., Льюис-Михл Е.Л., Гомес М.И. (апрель 2012 г.). «Неблагоприятные исходы родов и воздействие трихлорэтилена и тетрахлорэтилена на матери в результате проникновения паров почвы в штате Нью-Йорк». Перспективы гигиены окружающей среды. 120 (4): 616–21. Дои:10.1289 / ehp.1103884. ЧВК 3339451. PMID 22142966.
Библиография
- Лоури TH, Ричардсон KS (1987). Механизм и теория органической химии (3-е изд.). Издательство Harper Collins. ISBN 978-0-06-364044-3.
внешняя ссылка
- Инструмент выбора растворителя ACS Green Chemistry Institute
- «Европейская группа производителей растворителей - ESIG - Европейская группа производителей растворителей ESIG» Растворители в Европе.
- Таблица и текст Лекция по O-Chem
- Столы Свойства и токсичность органических растворителей
- CDC - Органические растворители - Тема безопасности и здоровья NIOSH
- EPA - Салфетки, загрязненные растворителями
