Твердый раствор - Solid solution
Эта статья нужны дополнительные цитаты для проверка. (Ноябрь 2007 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |

Примечание 1: Определение «кристалл, содержащий второй компонент, который вписывается в
распределяется в решетке основного кристалла », приведенного в работах,[1][2] не является общим
и, таким образом, не рекомендуется.
Заметка 2: Выражение должно использоваться для описания твердой фазы, содержащей
более одного вещества, когда для удобства одно (или несколько) веществ,
называется растворителем, обрабатывается иначе, чем другие вещества, называемые растворенными веществами.
Заметка 3: Один или несколько компонентов могут быть макромолекулы. Некоторые из
другие компоненты могут затем действовать как пластификаторы, т.е. как молекулярно-диспергированные
вещества, понижающие температуру стеклования, при которых аморфный
фаза полимер преобразуется между стекловидным и эластичным состояниями.
Примечание 4: В фармацевтических препаратах понятие твердого раствора часто
применяется к смесям препарат, средство, медикамент и полимер.
полимеров мало.[3]
А Твердый раствор[4] это твердый -государственный решение одного или нескольких растворенные вещества в растворитель. Такая многокомпонентная система считается скорее решением, чем сложный когда Кристальная структура растворителя остается неизменным при добавлении растворенных веществ и когда химические компоненты остаются в единой гомогенной фазе. Это часто случается, когда два элемента (обычно металлы ) вовлечены близко друг к другу на периодическая таблица; И наоборот, химическое соединение обычно возникает, когда два вовлеченных металла не находятся рядом друг с другом в периодической таблице.[5]
Твердый раствор нужно отличать от механические смеси порошкообразных твердых веществ, таких как две соли, сахар и соль и т. д. Механические смеси имеют полное или частичное разрыв в смешиваемости в твердом состоянии. Примеры твердых растворов включают кристаллизованные соли из их жидкой смеси, металлов сплавы и влажный твердые тела. В случае металлических сплавов интерметаллид соединения встречаются часто.
Подробности
Растворенное вещество может включаться в растворитель. кристаллическая решетка замещающий, заменяя частицу растворителя в решетке, или межстраничный, помещаясь в пространство между частицами растворителя. Оба этих типа твердых растворов влияют на свойства материала, искажая кристаллическую решетку и нарушая физическую и электрическую однородность материала растворителя.[6]
Некоторые смеси легко образуют твердые растворы в широком диапазоне концентраций, тогда как другие смеси вообще не образуют твердых растворов. Склонность любых двух веществ к образованию твердого раствора - сложный вопрос, связанный с химический, кристаллографический, и квант свойства рассматриваемых веществ. Твердые растворы замещения, в соответствии с Правила Юма-Розери, может образоваться, если растворенное вещество и растворитель имеют:
- Похожий атомные радиусы (Разница 15% или меньше)
- Та же кристаллическая структура
- Похожий электроотрицательность
- Похожий валентность
твердый раствор смешивается с другими, образуя новый раствор
В фазовая диаграмма в рисунок 1 отображает сплав двух металлов, который образует твердый раствор относительно концентрации двух видов. В этом случае чистая фаза каждого элемента имеет одну и ту же кристаллическую структуру, и аналогичные свойства двух элементов допускают несмещенное замещение во всем диапазоне относительных концентраций.
Твердые растворы имеют важное коммерческое и промышленное применение, поскольку такие смеси часто обладают превосходными свойствами по сравнению с чистыми материалами. Многие металлические сплавы представляют собой твердые растворы. Даже небольшое количество растворенного вещества может повлиять на электрические и физические свойства растворителя.
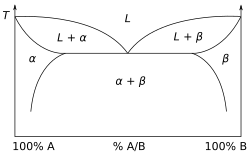
Бинарная фазовая диаграмма в Рис. 2 показывает фазы смеси двух веществ в различных концентрациях, и . Регион с пометкой ""твердый раствор, с действуя как растворенное вещество в матрице . На другом конце шкалы концентраций область помечена ""тоже твердый раствор, с действуя как растворенное вещество в матрице . Большая сплошная область между и твердые растворы, помеченные " + ", является нет твердый раствор. Вместо этого изучение микроструктура смеси в этом диапазоне обнаружит две фазы - твердый раствор -в- и твердый раствор -в- образуют отдельные фазы, возможно ламели или же зерна.
Заявление
На фазовой диаграмме при трех различных концентрациях материал будет твердым, пока не нагреется до температура плавления, а затем (после добавления теплота плавления ) становятся жидкими при той же температуре:
- беспримесные крайние левые
- беспримесные крайне правые
- провал в центре ( эвтектика сочинение).
При других пропорциях материал перейдет в кашеобразную или пастообразную фазу, пока не нагреется до полного расплавления.
Смесь в точке падения диаграммы называется эвтектика сплав. Смеси свинца и олова, приготовленные на этом этапе (смесь 37/63), полезны при пайке электронных компонентов, особенно если это делается вручную, поскольку твердая фаза быстро входит в состав при охлаждении припоя. Напротив, когда смеси свинца и олова использовались для пайки швов в кузовах автомобилей, пастообразное состояние позволяло формировать форму с помощью деревянной лопатки или инструмента, поэтому использовалось соотношение свинца и олова 70-30. (Свинец удаляется из таких приложений из-за его токсичность и, как следствие, трудности с переработкой устройств и компонентов, содержащих свинец.)
Exsolution
Когда твердый раствор становится нестабильным - например, из-за более низкой температуры - происходит распад, и две фазы разделяются на отдельные микроскопические и сверхмассивные ламели. В основном это вызвано разницей в размере катионов. Катионы с большим различием радиусов вряд ли легко заменятся.[7]
Возьми щелочь полевой шпат минералы например, чей конечные члены находятся альбит, NaAlSi3О8 и микроклин, КАЛСИ3О8. При высоких температурах Na+ и K+ легко замещают друг друга, и поэтому минералы образуют твердый раствор, но при низких температурах альбит может заменять лишь небольшое количество K+ и то же самое относится к Na+ в микроклине. Это приводит к распаду, где они разделятся на две отдельные фазы. В случае минералов щелочного полевого шпата тонкие белые слои альбита будут чередоваться между типично розовым микроклином,[7] в результате пертит текстура.
Смотрите также
Рекомендации
- ^ Алан Д. Макнот; Эндрю Р. Уилкинсон, ред. (1997). Сборник химической терминологии: Рекомендации ИЮПАК (2-е изд.). Blackwell Science. ISBN 0865426848.
- ^ Сборник аналитической номенклатуры («Оранжевая книга»). Оксфорд: Blackwell Science. 1998 г. ISBN 0865426155.
- ^ Верт, Мишель; Дои, Йошихару; Хеллвич, Карл-Хайнц; Гесс, Майкл; Ходж, Филипп; Кубиса, Пшемыслав; Ринаудо, Маргарита; Шуэ, Франсуа (2012). «Терминология для биорелированных полимеров и приложений (Рекомендации IUPAC 2012 г.)» (PDF). Чистая и прикладная химия. 84 (2): 377–410. Дои:10.1351 / PAC-REC-10-12-04. S2CID 98107080.
- ^ «Твердый раствор - химия».
- ^ Коттрелл, Алан Ховард (1967). Введение в металлургию. Институт материалов. ISBN 0-8448-0767-2.
- ^ Каллистер-младший, Уильям Д. (2006). Материаловедение и инженерия: введение (7-е изд.). Джон Вили и сыновья. ISBN 0-471-35446-5.
- ^ а б Нессе, Уильям Д. (2000). Введение в минералогию. Нью-Йорк: Издательство Оксфордского университета. p91-92. ISBN 978-0-19-510691-6
- Чен, Цзин; Сюй, Чжи-цинь; Чен, Z-Z .; Ли, Т-Ф. И Чен, Ф-Й. (Декабрь 2005 г.). «Текстура распада паргасита и ильменита в клинопироксене из Hujialing Garnet-Pyroxenite, Su-lu U.H.P. террейна, Центральный Китай: геодинамическое значение» (PDF). Европейский журнал минералогии. 17 (6): 895–903. Bibcode:2005EJMin..17..895C. Дои:10.1127/0935-1221/2005/0017-0895. Архивировано из оригинал (PDF) 9 мая 2006 г.
- Петерсен, У. "Введение в рудную микроскопию II; минеральный парагенезис" (PDF). Архивировано из оригинал (PDF) 11 апреля 2006 г.




