Диметилформамид - Dimethylformamide - Wikipedia
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC N,N-Диметилформамид[2] | |||
| Другие имена | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 3DMet | |||
| 605365 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.617 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
| MeSH | Диметилформамид | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 2265 | ||
| |||
| |||
| Характеристики | |||
| C3ЧАС7NО | |||
| Молярная масса | 73.095 г · моль−1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | рыбный, аммиачный | ||
| Плотность | 0,948 г / мл | ||
| Температура плавления | -78 ° С (-108 ° F, 195 К) | ||
| Точка кипения | 153 ° С (307 ° F, 426 К) | ||
| Смешиваемый | |||
| бревно п | −0.829 | ||
| Давление газа | 516 Па | ||
| Кислотность (пKа) | -0,3 (для конъюгированной кислоты) (H2O)[3] | ||
| УФ-видимый (λМаксимум) | 270 нм | ||
| Абсорбция | 1.00 | ||
| 1,4305 (при 20 ° C) | |||
| Вязкость | 0,92 мПа с (при 20 ° C) | ||
| Структура | |||
| 3.86 D | |||
| Термохимия | |||
Теплоемкость (C) | 146,05 Дж / (К · моль) | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -239,4 ± 1,2 кДж / моль | ||
Станд. Энтальпия горение (ΔcЧАС⦵298) | -1,9416 ± 0,0012 МДж / моль | ||
| Опасности | |||
| Паспорт безопасности | Видеть: страница данных | ||
| Пиктограммы GHS |    | ||
| Сигнальное слово GHS | Опасность | ||
| H226, H312, H319, H332, H360 | |||
| P280, P305 + 351 + 338, P308 + 313 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 58 ° С (136 ° F, 331 К) | ||
| 445 ° С (833 ° F, 718 К) | |||
| Пределы взрываемости | 2.2–15.2% | ||
| 30 мг / м (TWA) | |||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза ) |
| ||
LC50 (средняя концентрация ) | 3092 частей на миллион (мышь, 2час )[5] | ||
LCLo (самый низкий опубликованный ) | 5000 ppm (крыса, 6 ч)[5] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 10 частей на миллион (30 мг / м3) [кожа][4] | ||
REL (Рекомендуемые) | TWA 10 частей на миллион (30 мг / м3) [кожа][4] | ||
IDLH (Непосредственная опасность) | 500 частей на миллион[4] | ||
| Родственные соединения | |||
Родственные алканамиды | |||
Родственные соединения | |||
| Страница дополнительных данных | |||
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |||
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ | ||
| УФ, ИК, ЯМР, РС | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
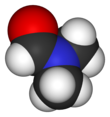
Диметилформамид является органическое соединение с формула (CH3 )2NC (O) H. Обычно сокращенно DMF (хотя этот инициализм иногда используется для диметилфуран, или же диметилфумарат ) эта бесцветная жидкость смешивается с воды и большинство органических жидкостей. ДМФ является обычным растворитель за химические реакции. Диметилформамид не имеет запаха, но технический или деградированные образцы часто имеют рыбный запах из-за примесей диметиламин. Примеси разложения диметиламина могут быть удалены путем барботирования разложившихся образцов инертным газом, таким как аргон или путем обработки образцов ультразвуком при пониженном давлении. Как видно из названия, это производное от формамид, то амид из муравьиная кислота. ДМФ - это полярный (гидрофильный ) апротонный растворитель с высоким точка кипения. Он способствует реакциям, которые следуют полярным механизмам, таким как SN2 реакции.
Структура и свойства
Что касается большинства амиды спектроскопические данные указывают на частичный характер двойной связи для связей C-N и C-O. Таким образом инфракрасный спектр показывает частоту растяжения C = O всего на 1675 см−1, тогда как кетон поглотит около 1700 см−1.[6]
DMF - классический пример флюсионная молекула.[7]

Температура окружающей среды 1H ЯМР спектр показывает два сигнала метила, указывающие на затрудненное вращение вокруг связи (O) C-N.[6] При температурах около 100 ° C спектр ЯМР 500 МГц этого соединения показывает только один сигнал для метильных групп.
ДМФ смешивается с водой.[8] Давление пара при 20 ° C составляет 3,5 гПа.[9] А Закон Генри постоянная 7,47 × 10−5 гПа м3 моль−1 можно вывести из экспериментально определенной константы равновесия при 25 ° C.[10] В Коэффициент распределения бревнопOW измеряется до -0,85.[11] Поскольку плотность ДМФА (0,95 г см−3 при 20 ° C[8]) аналогична воде, значительной флотации или расслоения в поверхностных водах в случае аварийных потерь не ожидается.

Реакции
ДМФ гидролизуется сильными кислотами и основаниями, особенно при повышенных температурах. С едкий натр, ДМФ превращается в формиат и диметиламин. ДМФ проходит декарбонилирование около точки кипения с образованием диметиламина. Поэтому дистилляцию проводят при пониженном давлении и более низких температурах.[12]
В одном из его основных применений в органический синтез, ДМФ был реагентом в Реакция Вильсмайера – Хаака, который используется для формилирования ароматических соединений.[13][14] Процесс включает начальное превращение ДМФ в ион хлориминия, [(CH3)2N = CH (Cl)]+, известный как реагент Вильсмайера,[15] который атакует арены.
Литийорганические соединения и Реактивы Гриньяра реагировать с DMF, чтобы дать альдегиды после гидролиза в реакции имени Буво.[16]
Диметилформамид образует 1: 1 аддукты с различными кислотами Льюиса, такими как мягкая кислота я2, и твердая кислота фенол. Классифицируется как жесткая база Льюиса и это Модель ECW базовые параметры - EB= 2,19 и CB= 1.31.[17] Его относительную донорную силу по отношению к ряду кислот по сравнению с другими основаниями Льюиса можно проиллюстрировать с помощью Графики C-B.[18][19]
Производство
ДМФ впервые был получен в 1893 году французским химиком Альбертом Верли (8 января 1867 - 27 ноября 1959) путем перегонки смеси гидрохлорида диметиламина и формиата калия.[20]
ДМФ получают путем объединения метилформиат и диметиламин или реакцией диметиламина с монооксид углерода.[21]
Хотя в настоящее время это непрактично, ДМФ может быть получен из сверхкритический углекислый газ с помощью рутений катализаторы на основе.[22]
Приложения
В основном ДМФ используется в качестве растворителя с низкой скоростью испарения. ДМФ используется в производстве акриловые волокна и пластмассы. Он также используется в качестве растворителя в пептидное связывание для фармацевтики, при разработке и производстве пестициды, и при изготовлении клеи синтетический кожи, волокна, пленки и поверхностные покрытия.[8]
- Используется как реагент в Синтез альдегида Буво[23][24][25] и в реакции Вильсмайера-Хаака[13][14] еще один полезный метод формирования альдегиды.
- Это обычный растворитель в Чертовски реакция.[26]
- Это также обычный катализатор, используемый в синтезе ацилгалогениды, в частности синтез ацилхлориды из карбоновые кислоты с помощью оксалил или же тионилхлорид. Каталитический механизм влечет за собой обратимое образование имидоилхлорида:[27][28]
- Мне2NC (O) H + (COCl)2 → CO + CO2 + [Я2N = CHCl] Cl
Иминиевый промежуточный продукт реагирует с карбоновой кислотой, выделяя оксид и регенерируя катализатор ДМФ.[27]
- ДМФ проникает больше всего пластмассы и заставляет их набухать. Благодаря этому свойству DMF подходит для твердофазный пептидный синтез и как компонент инструменты для снятия краски.
- ДМФ используется в качестве растворителя для восстановления олефины Такие как 1,3-бутадиен через экстрактивная перегонка.
- Он также используется в производстве сольвентных красителей в качестве важного сырья. Он расходуется во время реакции.
- Чистый ацетилен газ нельзя сжимать и хранить без опасности взрыва. Промышленный ацетилен безопасно сжимается в присутствии диметилформамида, который образует безопасный концентрированный раствор. Корпус также заполнен агамассан, что делает его безопасным для транспортировки и использования.
Правильное использование
Как дешевый и распространенный реагент, ДМФА широко используется в исследовательских лабораториях.
- ДМФ эффективен для разделения и суспендирования углеродные нанотрубки, и рекомендуется NIST для использования в ближняя инфракрасная спектроскопия таких.[29]
- ДМФ можно использовать в качестве стандарта в протонной ЯМР-спектроскопии, позволяя количественно определять неизвестное соединение.
- При синтезе металлоорганических соединений используется как источник монооксид углерода лиганды.
- ДМФ - распространенный растворитель, используемый в электроспиннинг.
- ДМФ обычно используется в сольвотермическом синтезе Металлоорганические каркасы.
- DMF-d7 в присутствии каталитического количества КОт-Bu при микроволновом нагреве является реагентом для дейтерирования полиароматических углеводородов.
Безопасность
Реакции, включая использование гидрид натрия в ДМФА в качестве растворителя несколько опасны; сообщалось о экзотермическом разложении при температурах до 26 ° C. В лабораторных условиях любое превышение температуры (обычно) быстро обнаруживается и контролируется с помощью ледяной ванны, и это остается популярной комбинацией реагентов. На пилотный проект масштаба, с другой стороны, сообщалось о нескольких несчастных случаях.[30]
20 июня 2018 г. Датское агентство по охране окружающей среды опубликовал статью об использовании ДМФ в хлюпик. Плотность смеси в игрушке привела к тому, что все хлюпки были удалены с датского рынка. Все сквиши рекомендовалось выбрасывать как бытовые отходы.[31]
Токсичность
Острый LD50 (перорально, крысы и мыши) 2,2–7,55 г / кг.[8] Опасности DMF были изучены.[32]
Рекомендации
- ^ N,N-Диметилметанамид, Термостолы NIST Web
- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. С. 841, 844. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
Традиционное название «формамид» сохраняется для HCO-NH.2 и является предпочтительным названием ИЮПАК. Замена разрешена на –NH2 группа.
- ^ «Банк данных по опасным веществам (HSDB) - N, N-ДИМЕТИЛФОРМАМИД».
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0226". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б «Диметилформамид». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б «Диметилформамид». Спектральная база данных органических соединений. Япония: AIST. Получено 2012-06-28.[постоянная мертвая ссылка ]
- ^ Х. С. Гутовский; К. Х. Холм (1956). «Скоростные процессы и спектры ядерного магнитного резонанса. II. Затрудненное внутреннее вращение амидов». J. Chem. Phys. 25 (6): 1228–1234. Bibcode:1956ЖЧФ..25.1228Г. Дои:10.1063/1.1743184.
- ^ а б c d Bipp, H .; Кечка, Х. «Формамиды». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a12_001.pub2.
- ^ IPCS (Международная программа по химической безопасности) (1991). Критерии гигиены окружающей среды 114 «Диметилформамид» Программа Организации Объединенных Наций по окружающей среде, Международная организация труда, Всемирная организация здравоохранения; 1–124.
- ^ Taft, R.W .; Abraham, M.H .; Doherty, R.M .; Камлет, М. Дж. (1985). «Молекулярные свойства, определяющие растворимость органических неэлектролитов в воде». Природа. 313 (6001): 384–386. Bibcode:1985Натура.313..384Т. Дои:10.1038 / 313384a0.
- ^ (BASF AG, отдел аналитических, неопубликованных данных, J-No. 124659/08, 27.11.1987)
- ^ Comins, Daniel L .; Джозеф, Саян П. (2001). «N, N-диметилформамид». N,N-Диметилформамид. Энциклопедия реагентов для органического синтеза. Джон Уайли и сыновья. Дои:10.1002 / 047084289x.rd335. ISBN 9780470842898.
- ^ а б Вильсмайер, Антон; Хаак, Альбрехт (1927). "Über die Einwirkung von Halogenphosphor auf Alkyl-formanilide. Eine neue Methode zur Darstellung sekundärer und tertiärer п-Алкиламино-бензальдегид »[О реакции галогенидов фосфора с алкилформанилидами. Новый метод получения вторичных и третичных п-алкиламино-бензальдегид]. Бер. Dtsch. Chem. Ges. А / Б (на немецком). 60 (1): 119–122. Дои:10.1002 / cber.19270600118.
- ^ а б Мет-Кон, Отто; Стэнфорт, Стивен П. (1993). «Реакция Вильсмайера-Хаака». В Трост, Барри М.; Хиткок, Клейтон Х. (ред.). Дополнения к π-облигациям CX, часть 2. Комплексный органический синтез: селективность, стратегия и эффективность в современной органической химии. 2. Эльзевир. С. 777–794. Дои:10.1016 / B978-0-08-052349-1.00049-4. ISBN 9780080405933.
- ^ Джонс, Гурнос; Стэнфорт, Стивен П. (2000). "Реакция Вильсмайера неароматических соединений". Орг. Реагировать. 56 (2): 355–686. Дои:10.1002 / 0471264180.or056.02.
- ^ Ван, Зеронг (2009). Исчерпывающие органические названия реакций и реагентов. Хобокен, штат Нью-Джерси: Джон Вили. С. 490–492. ISBN 9780471704508.
- ^ Vogel G.C .; Драго, Р. С. (1996). «Модель ECW». Журнал химического образования. 73: 701–707. Bibcode:1996JChEd..73..701V. Дои:10.1021 / ed073p701.
- ^ Лоуренс, К. и Гал, Дж.Ф. Шкалы основности и сродства Льюиса, данные и измерения, (Wiley 2010), стр. 50-51, IBSN 978-0-470-74957-9
- ^ Cramer, R.E .; Бопп, Т. Т. (1977). «Графическое отображение энтальпий образования аддуктов для кислот и оснований Льюиса». Журнал химического образования. 54: 612–613. Дои:10.1021 / ed054p612. На графиках, представленных в этом документе, используются более старые параметры. Улучшенные параметры E&C перечислены в Модель ECW.
- ^ Верлей, А. (1893). "Sur la preparation des amides en général" [О получении амидов в целом]. Bulletin de la Société Chimique de Paris. 3-я серия (на французском языке). 9: 690–692. На стр. 692, Верли заявляет, что ДМФ получают по методике, аналогичной процедуре получения диметилацетамида (см. Стр. 691), которая может происходить путем отгонки гидрохлорида диметиламина и формиат калия.
- ^ Weissermel, K .; Арпе, Х.-Дж. (2003). Промышленная органическая химия: важное сырье и промежуточные продукты. Wiley-VCH. С. 45–46. ISBN 3-527-30578-5.
- ^ Вальтер Лейтнер; Филип Дж. Джессоп (1999). Химический синтез с использованием сверхкритических жидкостей. Wiley-VCH. С. 408–. ISBN 978-3-527-29605-7. Получено 27 июн 2011.
- ^ Буво, Луи (1904). "Режимы образования и подготовки альдегидов сатурации в серии Грасс" [Способы получения предельных альдегидов алифатического ряда]. Bulletin de la Société Chimique de Paris. 3-я серия (на французском языке). 31: 1306–1322.
- ^ Буво, Луи (1904). "Nouvelle méthode générale synthétique de preparation des aldéhydes" [Новый общий синтетический метод получения альдегидов]. Bulletin de la Société Chimique de Paris. 3-я серия (на французском языке). 31: 1322–1327.
- ^ Ли, Джи Джек (2014). «Синтез альдегида Буво». Именные реакции: сборник подробных механизмов и синтетических приложений (5-е изд.). Springer Science & Business Media. С. 72–73. ISBN 978-3-319-03979-4.
- ^ Острейх, Мартин, изд. (2009). Реакция Мизороки – Хека.. Джон Уайли и сыновья. ISBN 9780470716069.
- ^ а б Клейден, Дж. (2001). Органическая химия. Оксфорд: Издательство Оксфордского университета. стр.276–296. ISBN 0-19-850346-6.
- ^ Анселл, М.Ф. в «Химии ацилгалогенидов»; С. Патай, Ред .; Джон Уайли и сыновья: Лондон, 1972; С. 35–68.
- ^ Haddon, R .; Иткис, М. (март 2008 г.). «3. Спектроскопия в ближней инфракрасной области (БИК)» (pdf). In Freiman, S .; Hooker, S .; Миглер; К .; Арепалли, С. (ред.). Публикация 960-19 Проблемы измерения одностенных углеродных нанотрубок. NIST. п. 20. Получено 2012-06-28.
- ^ Форум опасностей химических реакций Великобритании В архиве 2011-10-06 на Wayback Machine и цитируемые там ссылки
- ^ Магнус Лёфстедт. "Skumlegetøj afgiver farlige kemikalier (на английском языке - Squishies, дающие опасные химические вещества)".
- ^ Redlich, C .; Beckett, W. S .; Sparer, J .; Barwick, K.W .; Riely, C.A .; Miller, H .; Sigal, S.L .; Shalat, S.L .; Каллен М. Р. (1988). «Заболевание печени, связанное с профессиональным воздействием растворителя диметилформамида». Анналы внутренней медицины. 108 (5): 680–686. Дои:10.7326/0003-4819-108-5-680. PMID 3358569.
внешняя ссылка
- Международная карта химической безопасности 0457
- Карманный справочник NIOSH по химической опасности. "#0226". Национальный институт охраны труда и здоровья (NIOSH).
- Краткий международный документ по химической оценке 31: N, N-диметилформамид