Водная модель - Water model

В вычислительная химия, а водная модель используется для моделирования и термодинамического расчета кластеры воды, жидкость воды, и водные растворы с явным растворителем. Модели определены из квантовая механика, молекулярная механика, экспериментальные результаты и эти комбинации. Чтобы имитировать определенную природу молекул, было разработано много типов моделей. В целом их можно классифицировать по следующим трем пунктам; (i) количество точек взаимодействия, называемых сайт, (ii) является ли модель жесткой или гибкой, (iii) включает ли модель поляризация последствия.
Альтернативой явным моделям воды является использование неявная сольватация модель, также называемая континуальной моделью, примером которой может быть Модель сольватации COSMO или модель поляризуемого континуума (PCM) или гибридная сольватационная модель.[1]
Простые водные модели
Жесткие модели считаются простейшими моделями воды и основаны на несвязанные взаимодействия. В этих моделях связывающие взаимодействия неявно рассматриваются как голономные ограничения. Электростатическое взаимодействие моделируется с помощью Закон Кулона, а силы рассеяния и отталкивания с использованием Потенциал Леннарда-Джонса.[2][3] Потенциал таких моделей, как TIP3P (переносимый межмолекулярный потенциал с 3 точками) и TIP4P представлен как
куда kC, то электростатическая постоянная, имеет значение 332,1 Å · ккал / (моль ·е ²) в единицах, обычно используемых в молекулярном моделировании.[нужна цитата ];[4][5][6] qя и qj являются частичные сборы относительно заряда электрона; рij расстояние между двумя атомами или заряженными узлами; и А и B являются Параметры Леннарда-Джонса. Заряженные сайты могут находиться на атомах или на фиктивных сайтах (например, неподеленных парах). В большинстве моделей воды термин Леннарда-Джонса применяется только к взаимодействию между атомами кислорода.
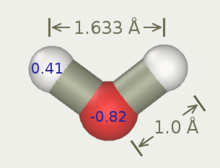
На рисунке ниже показана общая форма моделей воды с 3–6 участками. Точные геометрические параметры (расстояние OH и угол HOH) варьируются в зависимости от модели.

2-местный
Было показано, что двухсайтовая модель воды, основанная на знакомой трехузловой модели SPC (см. Ниже), предсказывает диэлектрические свойства воды с использованием теории молекулярной жидкости с перенормировкой узлов.[7]
3-местный
Трехузельные модели имеют три точки взаимодействия, соответствующие трем атомам молекулы воды. Каждый узел имеет точечный заряд, и узел, соответствующий атому кислорода, также имеет параметры Леннарда-Джонса. Поскольку трехсайтовые модели обеспечивают высокую вычислительную эффективность, они широко используются во многих приложениях молекулярная динамика симуляции. Большинство моделей используют жесткую геометрию, соответствующую геометрии реальных молекул воды. Исключением является модель SPC, которая предполагает идеальную тетраэдрическую форму (угол HOH 109,47 °) вместо наблюдаемого угла 104,5 °.
В таблице ниже перечислены параметры для некоторых моделей с 3 участками.
| ЧАЕВЫЕ[8] | SPC[9] | TIP3P[10] | SPC / E[11] | |
|---|---|---|---|---|
| р(ОН), Å | 0.9572 | 1.0 | 0.9572 | 1.0 |
| HOH, град | 104.52 | 109.47 | 104.52 | 109.47 |
| А, 103 ккал Å12/ моль | 580.0 | 629.4 | 582.0 | 629.4 |
| B, ккал Å6/ моль | 525.0 | 625.5 | 595.0 | 625.5 |
| q(O) | −0.80 | −0.82 | −0.834 | −0.8476 |
| q(ЧАС) | +0.40 | +0.41 | +0.417 | +0.4238 |
Модель SPC / E добавляет поправку к средней поляризации к функции потенциальной энергии:
где μ - электрический дипольный момент эффективно поляризованной молекулы воды (2.35 D для модели SPC / E), μ0 - дипольный момент изолированной молекулы воды (1,85 Д из эксперимента), а αя изотропный поляризуемость постоянная, со значением 1.608×10−40 F · М2. Поскольку заряды в модели постоянны, эта поправка просто приводит к добавлению 1,25 ккал / моль (5,22 кДж / моль) к полной энергии. Модель SPC / E дает лучшие плотность и константу диффузии, чем модель SPC.
Модель TIP3P, реализованная в Очарование силовое поле - это немного измененная версия оригинала. Разница заключается в параметрах Леннарда-Джонса: в отличие от TIP3P, версия модели CHARMM помещает параметры Леннарда-Джонса также и для атомов водорода, в дополнение к параметру для кислорода. Стоимость не изменяется.[12] Трехузловая модель (TIP3P) лучше справляется с расчетом удельной плавки.[13]
Гибкая водная модель SPC
Гибкая простая модель воды с точечным зарядом (или гибкая модель воды SPC) является перепараметризацией модели воды SPC с тремя участками.[14][15] В SPC модель жесткая, в то время как гибкий SPC модель гибкая. В модели Тукана и Рахмана растяжение O – H делается ангармоническим, и, таким образом, динамическое поведение хорошо описано. Это одна из самых точных трехцентровых моделей воды без учета поляризация. В молекулярная динамика моделирование дает правильные плотность и диэлектрическая проницаемость воды.[16]
В программах реализован гибкий SPC. MDynaMix и Морское ушко.
Другие модели
- Фергюсон (гибкий SPC)
- CVFF (гибкий)
- MG (гибкий и диссоциативный)[17]
- KKY потенциал (гибкая модель).[18]
- BLXL (размытие заряженного потенциала).[19]
4-местный
Четырехузельные модели имеют четыре точки взаимодействия путем добавления одного фиктивного атома рядом с кислородом вдоль биссектриса угла HOH трехпозиционных моделей (обозначенных M на рисунке). У фиктивного атома только отрицательный заряд. Эта модель улучшает электростатическое распределение вокруг молекулы воды. Первой моделью, использующей этот подход, была модель Бернала – Фаулера, опубликованная в 1933 г.[20] которая также может быть самой ранней водной моделью. Однако модель BF плохо воспроизводит объемные свойства воды, такие как плотность и теплота испарения, и поэтому представляет только исторический интерес. Это следствие метода параметризации; новые модели, разработанные после того, как стали доступны современные компьютеры, параметризовались путем запуска Метрополис Монте-Карло или моделирование молекулярной динамики и корректировка параметров до тех пор, пока объемные свойства не будут воспроизведены достаточно хорошо.
Модель TIP4P, впервые опубликованная в 1983 году, широко применяется в программных пакетах вычислительной химии и часто используется для моделирования биомолекулярных систем. Были последующие изменения параметров модели TIP4P для конкретных целей: модель TIP4P-Ew для использования с методами суммирования Эвальда; TIP4P / Ice для моделирования твердого водяного льда; и TIP4P / 2005, общая параметризация для моделирования всего фазовая диаграмма конденсированной воды.
Большинство моделей воды с четырьмя узлами используют расстояние ОН и угол НОН, соответствующие таковому у свободной молекулы воды. Исключением является модель OPC, на которую не накладываются никакие геометрические ограничения, кроме фундаментальных C2v молекулярная симметрия молекулы воды. Вместо этого точечные заряды и их положения оптимизированы для наилучшего описания электростатики молекулы воды. OPC воспроизводит полный набор объемных свойств более точно, чем обычно используемый жесткий п-сайтовые водные модели. Модель OPC реализована в ЯНТАРЬ силовое поле.
| BF[20] | СОВЕТЫ2[21] | TIP4P[10] | TIP4P-Ew[22] | TIP4P / Ice[23] | TIP4P / 2005[24] | OPC[25] | TIP4P-D[26] | |
|---|---|---|---|---|---|---|---|---|
| р(ОН), Å | 0.96 | 0.9572 | 0.9572 | 0.9572 | 0.9572 | 0.9572 | 0.8724 | 0.9572 |
| HOH, град | 105.7 | 104.52 | 104.52 | 104.52 | 104.52 | 104.52 | 103.6 | 104.52 |
| р(ОМ), Å | 0.15 | 0.15 | 0.15 | 0.125 | 0.1577 | 0.1546 | 0.1594 | 0.1546 |
| А, 103 ккал Å12/ моль | 560.4 | 695.0 | 600.0 | 656.1 | 857.9 | 731.3 | 865.1 | 904.7 |
| B, ккал Å6/ моль | 837.0 | 600.0 | 610.0 | 653.5 | 850.5 | 736.0 | 858.1 | 900.0 |
| q(М) | −0.98 | −1.07 | −1.04 | −1.04844 | −1.1794 | −1.1128 | −1.3582 | −1.16 |
| q(ЧАС) | +0.49 | +0.535 | +0.52 | +0.52422 | +0.5897 | +0.5564 | +0.6791 | +0.58 |
Другие:
- q-TIP4P / F (гибкий)
5-местный
5-позиционные модели помещают отрицательный заряд на фиктивные атомы (помечены L) представляющий одинокие пары атома кислорода с тетраэдрической геометрией. Ранней моделью этих типов была модель BNS Бен-Наима и Стиллингера, предложенная в 1971 г.[нужна цитата ] Вскоре на смену модели ST2 Стиллинджера и Рахмана в 1974 году.[27] В основном из-за более высокой вычислительной стоимости пятиузловые модели не особо разрабатывались до 2000 года, когда была опубликована модель Махони и Йоргенсена TIP5P.[28] По сравнению с более ранними моделями, модель TIP5P приводит к улучшению геометрии для димер воды, более «тетраэдрическая» структура воды, лучше воспроизводящая экспериментальную функции радиального распределения из нейтронография, и температура максимальной плотности воды. Модель TIP5P-E представляет собой реконструкцию TIP5P для использования с Суммы Эвальда.
| BNS[27] | ST2[27] | TIP5P[28] | TIP5P-E[29] | |
|---|---|---|---|---|
| р(ОН), Å | 1.0 | 1.0 | 0.9572 | 0.9572 |
| HOH, град | 109.47 | 109.47 | 104.52 | 104.52 |
| р(OL), Å | 1.0 | 0.8 | 0.70 | 0.70 |
| LOL, град. | 109.47 | 109.47 | 109.47 | 109.47 |
| А, 103 ккал Å12/ моль | 77.4 | 238.7 | 544.5 | 554.3 |
| B, ккал Å6/ моль | 153.8 | 268.9 | 590.3 | 628.2 |
| q(L) | −0.19562 | −0.2357 | −0.241 | −0.241 |
| q(ЧАС) | +0.19562 | +0.2357 | +0.241 | +0.241 |
| рL, Å | 2.0379 | 2.0160 | ||
| рU, Å | 3.1877 | 3.1287 |
Обратите внимание, однако, что модели BNS и ST2 не используют закон Кулона непосредственно для электростатических членов, а модифицированную версию, которая уменьшается в масштабе на коротких расстояниях путем умножения ее на функцию переключения. S(р):
Таким образом рL и рU параметры применяются только к BNS и ST2.
6-сайт
Первоначально разработанная для изучения систем вода / лед, модель с 6 участками, объединяющая все участки моделей с 4 и 5 участками, была разработана Нада и ван дер Эрденом.[30] Поскольку у него была очень высокая температура плавления[31] при использовании в периодических электростатических условиях (суммирование Эвальда) модифицированная версия была опубликована позже[32] оптимизирован с использованием метода Эвальда для оценки кулоновского взаимодействия.
Другой
- Влияние явной модели растворенного вещества на поведение растворенного вещества в моделировании биомолекул также широко изучалось. Было показано, что явные водные модели влияют на специфическую сольватацию и динамику развернутых пептидов, в то время как конформационное поведение и гибкость свернутых пептидов остаются неизменными.[33]
- Модель МБ. Более абстрактная модель, напоминающая Мерседес Бенц логотип, воспроизводящий некоторые черты воды в двухмерных системах. Он не используется как таковой для моделирования «реальных» (т.е. трехмерных) систем, но полезен для качественных исследований и в образовательных целях.[34]
- Крупнозернистые модели. Также были разработаны одно- и двухпозиционные модели воды.[35] В крупнозернистых моделях каждое место может представлять несколько молекул воды.
- Многотельные модели. Модели воды, построенные с использованием конфигураций обучающих наборов, решаемых квантово-механически, которые затем используют протоколы машинного обучения для извлечения поверхностей потенциальной энергии. Эти поверхности потенциальной энергии вводятся в моделирование МД для беспрецедентной степени точности при вычислении физических свойств систем конденсированной фазы.[36]
Вычислительная стоимость
Вычислительные затраты на моделирование воды возрастают с увеличением количества точек взаимодействия в модели воды. Время ЦП примерно пропорционально количеству межатомных расстояний, которые необходимо вычислить. Для 3-позиционной модели требуется 9 расстояний для каждой пары молекул воды (каждый атом одной молекулы против каждого атома другой молекулы, или 3 × 3). Для модели с 4 сайтами требуется 10 расстояний (каждый заряженный сайт с каждым заряженным сайтом, плюс взаимодействие O – O, или 3 × 3 + 1). Для 5-позиционной модели требуется 17 расстояний (4 × 4 + 1). Наконец, для 6-позиционной модели требуется 26 расстояний (5 × 5 + 1).
При использовании моделей жесткой воды в молекулярной динамике существуют дополнительные затраты, связанные с удержанием конструкции в ограниченном состоянии с использованием алгоритмы ограничения (хотя при ограничении длины связи часто можно увеличить временной шаг).
Смотрите также
- Вода (свойства)
- Вода (страница данных)
- Димер воды
- Силовое поле (химия)
- Сравнение реализаций силового поля
- Молекулярная механика
- Молекулярное моделирование
- Сравнение программного обеспечения для моделирования молекулярной механики
- Модели на растворителях
Рекомендации
- ^ Скайнер Р. Э., МакДонах Дж. Л., Грум К. Р., ван Моурик Т., Митчелл Дж. Б. (март 2015 г.). «Обзор методов расчета свободной энергии раствора и моделирования систем в растворе» (PDF). Физическая химия Химическая физика. 17 (9): 6174–91. Bibcode:2015PCCP ... 17.6174S. Дои:10.1039 / C5CP00288E. PMID 25660403.
- ^ Аллен MP, Тилдесли DJ (1989). Компьютерное моделирование жидкостей. Кларендон Пресс. ISBN 978-0-19-855645-9.
- ^ Кирби Би Джей. Микро- и наномасштабная механика жидкости: перенос в микрофлюидных устройствах.
- ^ Swails JM, Roitberg AE (2013). "файл prmtop {A} mber" (PDF).
- ^ Swails JM (2013). Моделирование свободной энергии сложных биологических систем при постоянном pH (PDF). Университет Флориды.
- ^ Case DA, Walker RC, Cheatham III TE, Simmerling CL, Roitberg A, Merz KM и др. (Апрель 2019). «Справочное руководство Amber 2019 (охватывает Amber18 и AmberTools19)» (PDF).
- ^ Дайер К.М., Perkyns JS, Stell G, Pettitt BM (2009). "Сайт-перенормированная теория молекулярной жидкости: о полезности двухузельной модели воды". Молекулярная физика. 107 (4–6): 423–431. Bibcode:2009МолФ.107..423Д. Дои:10.1080/00268970902845313. ЧВК 2777734. PMID 19920881.
- ^ Йоргенсен, Уильям Л. (1981). «Квантовые и статистические механические исследования жидкостей. 10. Переносимые межмолекулярные потенциальные функции для воды, спиртов и эфиров. Применение к жидкой воде». Журнал Американского химического общества. Американское химическое общество (ACS). 103 (2): 335–340. Дои:10.1021 / ja00392a016. ISSN 0002-7863.
- ^ Х. Дж. К. Берендсен, Дж. П. М. Постма, В. Ф. ван Гунстерен и Дж. Херманс, In Межмолекулярные силыпод редакцией Б. Пуллмана (Reidel, Dordrecht, 1981), п. 331.
- ^ а б Йоргенсен В.Л., Чандрасекхар Дж., Мадура Д.Д., Импей Р.В., Кляйн М.Л. (1983). «Сравнение простых потенциальных функций для моделирования жидкой воды». Журнал химической физики. 79 (2): 926–935. Bibcode:1983JChPh..79..926J. Дои:10.1063/1.445869.
- ^ Берендсен HJ, Grigera JR, Straatsma TP (1987). «Недостающий член в эффективных парных потенциалах». Журнал физической химии. 91 (24): 6269–6271. Дои:10.1021 / j100308a038.
- ^ Маккерелл А.Д., Башфорд Д., Беллотт М., Данбрак Р.Л., Эвансек Д.Д., Филд М.Дж. и др. (Апрель 1998 г.). «Всеатомный эмпирический потенциал для молекулярного моделирования и изучения динамики белков». Журнал физической химии B. 102 (18): 3586–616. Дои:10.1021 / jp973084f. PMID 24889800.
- ^ Мао И, Чжан И (2012). «Теплопроводность, сдвиговая вязкость и удельная теплоемкость моделей жесткой воды». Письма по химической физике. 542: 37–41. Bibcode:2012CPL ... 542 ... 37 млн. Дои:10.1016 / j.cplett.2012.05.044.
- ^ Тукан К., Рахман А. (март 1985 г.). «Молекулярно-динамическое исследование движений атомов в воде». Физический обзор B. 31 (5): 2643–2648. Bibcode:1985ПхРвБ..31.2643Т. Дои:10.1103 / PhysRevB.31.2643. PMID 9936106.
- ^ Берендсен HJ, Grigera JR, Straatsma TP (1987). «Недостающий член в эффективных парных потенциалах». Журнал физической химии. 91 (24): 6269–6271. Дои:10.1021 / j100308a038.
- ^ Praprotnik M, Janezic D, Mavri J (2004). "Температурная зависимость колебательного спектра воды: исследование с помощью моделирования молекулярной динамики". Журнал физической химии А. 108 (50): 11056–11062. Bibcode:2004JPCA..10811056P. Дои:10.1021 / jp046158d.
- ^ Модель MG.
- ^ Кумагаи Н., Кавамура К., Йококава Т. (1994). «Модель межатомного потенциала для H2O: приложения к полиморфам воды и льда». Молекулярное моделирование. Informa UK Limited. 12 (3–6): 177–186. Дои:10.1080/08927029408023028. ISSN 0892-7022.
- ^ Бернхэм С.Дж., Ли Дж., Ксантеас СС, Лесли М. (1999). «Параметризация модели полностью атомной поляризуемой воды типа Толола из первых принципов и ее применение к изучению кластеров воды (n = 2–21) и фононного спектра льда Ih». Журнал химической физики. 110 (9): 4566–4581. Bibcode:1999ЖЧФ.110.4566Б. Дои:10.1063/1.478797.
- ^ а б Бернал Дж. Д., Фаулер Р. Х. (1933). «Теория воды и ионного раствора, с особым упором на водород и гидроксильные ионы». Журнал химической физики. 1 (8): 515. Bibcode:1933ЖЧФ ... 1..515Б. Дои:10.1063/1.1749327.
- ^ Йоргенсен (1982). «Пересмотренные TIPS для моделирования жидкой воды и водных растворов». Журнал химической физики. 77 (8): 4156–4163. Bibcode:1982ЖЧФ..77.4156Ж. Дои:10.1063/1.444325.
- ^ Horn HW, Swope WC, Pitera JW, Madura JD, Dick TJ, Hura GL, Head-Gordon T (май 2004 г.). «Разработка улучшенной модели воды с четырьмя узлами для моделирования биомолекул: TIP4P-Ew». Журнал химической физики. 120 (20): 9665–78. Bibcode:2004ЖЧФ.120.9665Н. Дои:10.1063/1.1683075. PMID 15267980.
- ^ Abascal JL, Sanz E, García Fernández R, Vega C (июнь 2005 г.). «Возможная модель для изучения льда и аморфной воды: TIP4P / Ice». Журнал химической физики. 122 (23): 234511. Bibcode:2005ЖЧФ.122в4511А. Дои:10.1063/1.1931662. PMID 16008466.
- ^ Abascal JL, Vega C (декабрь 2005 г.). «Универсальная модель конденсированных фаз воды: TIP4P / 2005». Журнал химической физики. 123 (23): 234505. Bibcode:2005ЖЧФ.123w4505A. Дои:10.1063/1.2121687. PMID 16392929.
- ^ Изади С., Анандакришнан Р., Онуфриев А.В. (ноябрь 2014 г.). «Построение водных моделей: другой подход». Письма в Журнал физической химии. 5 (21): 3863–3871. arXiv:1408.1679. Bibcode:2014arXiv1408.1679I. Дои:10.1021 / jz501780a. ЧВК 4226301. PMID 25400877.
- ^ Пиана С., Дончев А.Г., Робустелли П., Шоу Д.Е. (апрель 2015 г.). «Взаимодействие с водной дисперсией сильно влияет на смоделированные структурные свойства неупорядоченных состояний белка». Журнал физической химии B. 119 (16): 5113–23. Дои:10.1021 / jp508971m. PMID 25764013.
- ^ а б c Стиллинджер Ф.Х., Рахман А (1974). «Улучшенное моделирование жидкой воды с помощью молекулярной динамики». Журнал химической физики. 60 (4): 1545–1557. Bibcode:1974ЖЧФ..60.1545С. Дои:10.1063/1.1681229.
- ^ а б Махони MW, Йоргенсен WL (2000). «Пятиузельная модель жидкой воды и воспроизведение аномалии плотности жесткими неполяризуемыми потенциальными функциями». Журнал химической физики. 112 (20): 8910–8922. Bibcode:2000ЖЧФ.112.8910М. Дои:10.1063/1.481505.
- ^ Рик SW (апрель 2004 г.). «Повторная оптимизация водного потенциала пяти участков (TIP5P) для использования с суммами Эвальда». Журнал химической физики. 120 (13): 6085–93. Bibcode:2004ЖЧФ.120.6085Р. Дои:10.1063/1.1652434. PMID 15267492.
- ^ Нада, Х. (2003). "Модель межмолекулярного потенциала для моделирования льда и воды вблизи точки плавления: шестиузельная модель H2О ". Журнал химической физики. 118 (16): 7401. Bibcode:2003ЖЧФ.118.7401Н. Дои:10.1063/1.1562610.
- ^ Abascal JL, Fernández RG, Vega C, Carignano MA (октябрь 2006 г.). «Температура плавления шестиузловой потенциальной модели воды». Журнал химической физики. 125 (16): 166101. Bibcode:2006ЖЧФ.125п6101А. Дои:10.1063/1.2360276. PMID 17092145.
- ^ Нада Х (декабрь 2016 г.). «2O и моделирование молекулярной динамики». Журнал химической физики. 145 (24): 244706. Bibcode:2016ЖЧФ.145х4706Н. Дои:10.1063/1.4973000. PMID 28049310.
- ^ Флорова П., Скленовский П., Банаш П., Отепка М. (ноябрь 2010 г.). «Явные водные модели влияют на специфическую сольватацию и динамику развернутых пептидов, в то время как конформационное поведение и гибкость свернутых пептидов остаются неизменными». Журнал химической теории и вычислений. 6 (11): 3569–79. Дои:10.1021 / ct1003687. PMID 26617103.
- ^ Сильверштейн К.А., Хаймет А.Д., Дилл К.А. (1998). «Простая модель воды и гидрофобный эффект». Журнал Американского химического общества. 120 (13): 3166–3175. Дои:10.1021 / ja973029k.
- ^ Извеков С., Вот Г.А. (октябрь 2005 г.). «Мультимасштабная крупнозернистая структура жидких систем». Журнал химической физики. Издательство AIP. 123 (13): 134105. Bibcode:2005ЖЧФ.123м4105И. Дои:10.1063/1.2038787. PMID 16223273.
- ^ Меддерс Г.Р., Паесани Ф. (март 2015 г.). "Инфракрасная и рамановская спектроскопия жидкой воды на основе" первых принципов "молекулярной динамики многих тел". Журнал химической теории и вычислений. 11 (3): 1145–54. Дои:10.1021 / ct501131j. PMID 26579763.
- ^ Cisneros GA, Wikfeldt KT, Ojamäe L, Lu J, Xu Y, Torabifard H, et al. (Июль 2016 г.). «Моделирование молекулярных взаимодействий в воде: от парных к функциям потенциальной энергии многих тел». Химические обзоры. 116 (13): 7501–28. Дои:10.1021 / acs.chemrev.5b00644. ЧВК 5450669. PMID 27186804.
- ^ Wikfeldt KT, Batista ER, Vila FD, Jónsson H (октябрь 2013 г.). «Переносимый потенциал взаимодействия H2O на основе одноцентрового мультипольного расширения: SCME». Физическая химия Химическая физика. 15 (39): 16542–56. arXiv:1306.0327. Дои:10.1039 / c3cp52097h. PMID 23949215.



