Платинохлористоводородная кислота - Chloroplatinic acid
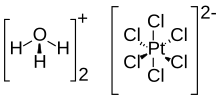 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Гексахлороплатинат дигидрония (2–) | |
| Другие имена Гексахлорплатиновая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.037.267 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 2507 |
| |
| |
| Характеристики | |
| ЧАС6Cl6О2Pt | |
| Молярная масса | 409,81 г / моль |
| Внешность | Красновато-коричневое твердое вещество |
| Плотность | 2,431 г / см3 |
| Температура плавления | 60 ° С (140 ° F, 333 К) |
| Точка кипения | разлагается |
| хорошо растворим | |
| Структура | |
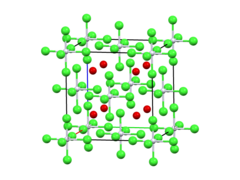
| Антифлюорит. | |
| восьмигранный | |
| 0 D | |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материала |
| Пиктограммы GHS |     |
| Сигнальное слово GHS | Опасность |
| H301, H314, H317, H334 | |
| P260, P261, P264, P270, P272, P280, P285, P301 + 310, P301 + 330 + 331, P302 + 352, P303 + 361 + 353, P304 + 340, P304 + 341, P305 + 351 + 338, P310, P321, P330, P333 + 313, P342 + 311, P363, P405, P501 | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Другой анионы | Гексахлорпалладовая кислота |
Другой катионы | Гексахлороплатинат калия, Гексахлороплатинат аммония, Гексахлороплатинат рубидия, Гексахлороплатинат цезия |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Платинохлористоводородная кислота (также известен как платинохлористоводородная кислота) является неорганическое соединение с формулой [H3O]2[PtCl6](ЧАС2O)Икс (0 ≤ Икс ≤ 6). Красное твердое вещество, это важный коммерческий источник платина, обычно в виде водного раствора. Хотя часто сокращенно пишется как H2PtCl6, это гидроксоний (ЧАС3О+) соль аниона гексахлороплатината (PtCl2−
6).[1][2][3] Гексахлорплатиновая кислота очень гигроскопичный.
Производство

Гексахлорплатиновая кислота может производиться различными способами. Наиболее распространенный из этих методов включает растворение платины в царская водка. Другие методы включают воздействие на водную суспензию частиц платины газообразным хлором или электролиз.
Полагают, что при производстве царской водкой гексахлорплатиновая кислота возникает по следующему уравнению: [4][5]
- Pt + 4 HNO3 + 6 HCl → H2PtCl6 + 4 НЕТ2 + 4 часа2О
Полученный оранжево-красный раствор можно упарить, получив коричневато-красные кристаллы. Некоторые авторы предполагают, что гексахлорплатиновая кислота, полученная этим методом, загрязнена гексахлороплатинатом нитрозония. В новой литературе указано, что это не так, и что после удаления азотной кислоты образцы, полученные этим методом, не содержат обнаруживаемого азота.
Были исследованы и описаны альтернативные методы, часто мотивированные недопущением загрязнения азотом.[6]
Реакции
При нагревании платинохлористоводородная кислота разлагается до хлорид платины (IV).[1]
- (ЧАС3O)2PtCl6·пЧАС2O → PtCl4 + 2 HCl + (п + 2) H2О
Приложения
Определение калия
Хлороплатиновая кислота была популяризирована для количественный анализ калия. Калий селективно осаждается из решение как гексахлороплатинат калия. Определения проводили в 85% (об. / Об.) Спиртовых растворах с избытком ионов платината, и осажденный продукт взвешивали. Калий можно обнаружить в растворах с разбавлением от 0,02 до 0,2% (м / об).[7]
Этот метод определения калия был выгоден по сравнению с кобальтинитрит натрия использованный ранее метод, так как он требовал одного осадки реакция.[7] Гравиметрический анализ выпавших продуктов был вытеснен современным инструментальный анализ такие методы как ионоселективные электроды, фотометрия пламени, ICP-AES или же ИСП-МС.
Очистка платины
После обработки солью аммония, такой как хлорид аммония, платинохлористоводородная кислота превращается в гексахлороплатинат аммония, который осаждается в виде твердого вещества.[4] При нагревании в атмосфере водород, соль аммония превращается в элементарную платину. Платину часто выделяют из руды или таким образом повторно используют из остатков.[8]
Катализ
Как и многие соединения платины, платинохлористоводородная кислота является катализатором (или предварительным катализатором) для гидрирование и родственные реакции. Как впервые сообщили Джон Спейер и его коллеги из Dow Corning, он катализирует присоединение гидросиланов к олефинам, т.е. гидросилилирование. В первых демонстрационных реакциях использовались изопропанольные растворы трихлорсилан (SiHCl3) с пентены. Предыдущие работы по добавлению силанов к алкенам требовали радикальных реакций, которые были неэффективными.[9][10] Как и с Катализатор Карстедта Катализатор Шпейера широко используется для гидросилилирования, основным недостатком этого катализатора являются свойства плавучести.[11]
Обычно считается, что платинохлористоводородная кислота является предшественником реального катализатора. Возможная роль коллоидной платины или нулевой валентный комплексы также были рассмотрены.[12]
Родственные соединения
Хлороплатиновая кислота, полученная из царская водка предлагается содержать гексахлороплатинат нитрозония, (NO)2PtCl6. Гексахлороплатинат нитрозония получают по реакции нитрозилхлорид (NOCl) и металлическая платина.[13] Было обнаружено, что гексахлороплатинат нитрозония активно реагирует с водой и соляной кислотой, что делает маловероятным загрязнение платинохлористоводородной кислоты, полученной с использованием царской водки, гексахлороплатинатом нитрозония.
Рекомендации
- ^ а б Schweizer, A.E .; Керр, Г. Т. (1978). «Термическое разложение платинохлористоводородной кислоты». Неорг. Chem. 17 (8): 2326–2327. Дои:10.1021 / ic50186a067.
- ^ Холлеман; Виберг (2001). Неорганическая химия (Первое изд.). Нью-Йорк: Academic Press. ISBN 0-12-352651-5.
- ^ Greenwood, N. N .; Эрншоу, А. (1997). Химия элементов (Второе изд.). Нью-Йорк: Эльзевьер Баттерворт-Хайнеманн. ISBN 978-0-7506-3365-9.
- ^ а б Кауфман, Джордж Б. (1967). «Гексахлороплатинат аммония (IV)». Неорганические синтезы. 9: 182–185. Дои:10.1002 / 9780470132401.ch51. ISBN 9780470132401.
- ^ Грубе, Х. (1963). «Гексахлорплатиновая (IV) кислота». В Брауэре, Г. (ред.). Справочник по препаративной неорганической химии. 2 (2-е изд.). Нью-Йорк: Academic Press. п. 1569.
- ^ Рудник, Пол; Кук, Р. Д. (1917). «Получение платинохлористоводородной кислоты с помощью перекиси водорода». Варенье. Chem. Soc. 39 (4): 633–635. Дои:10.1021 / ja02249a011.
- ^ а б Смит, Г. Фредерик; Гринг, Дж. Л. (1933). «Разделение и определение щелочных металлов с использованием хлорной кислоты. V. Хлорная кислота и хлороплатиновая кислота в определении малых количеств калия в присутствии больших количеств натрия». Варенье. Chem. Soc. 55 (10): 3957–3961. Дои:10.1021 / ja01337a007.
- ^ Коттон, С. А. (1997). Химия драгоценных металлов. Лондон: Чепмен и Холл. ISBN 0-7514-0413-6.
- ^ Speier, J. L .; Webster, J. A .; Барнс, Г. Х. (1957). «Добавление гидридов кремния к олефиновым двойным связям. Часть II. Использование металлических катализаторов VIII группы». Варенье. Chem. Soc. 79 (4): 974–979. Дои:10.1021 / ja01561a054.
- ^ Саам, Джон С .; Спейер, Джон Л. (1958). «Добавление гидридов кремния к олефиновым двойным связям. Часть III. Добавление к нетерминальным олефинам в присутствии платинохлористоводородной кислоты». Варенье. Chem. Soc. 80 (15): 4104–4106. Дои:10.1021 / ja01548a073.
- ^ Сиби, Мукунд П. (2001). «Гексахлороплатинат (IV) водорода». Энциклопедия реагентов для органического синтеза, 8 томов. Энциклопедия реагентов для органического синтеза. Джон Вили и сыновья. Дои:10.1002 / 047084289X.rh038. ISBN 0471936235.
- ^ Lewis, L.N .; Sy, K. G .; Bryant, G.L .; Донахью, П. Э. (1991). «Гидросилилирование алкинов, катализируемое платиной». Металлоорганические соединения. 10 (10): 3750–3759. Дои:10.1021 / om00056a055.
- ^ Moravek, R.T .; Кауфман, Г. Б .; Махмуд, Т. (1967). «Нитрозилгексахлороплатинат (IV)». Неорганические синтезы. 9: 217–220. Дои:10.1002 / 9780470132555.ch63. ISBN 9780470132555.

