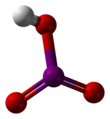
Йодная кислота - Iodic acid
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Другие имена Йодная (V) кислота | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.056 | ||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| HIO3 | |||
| Молярная масса | 175,91 г / моль | ||
| Внешность | Белое твердое вещество | ||
| Плотность | 4,62 г / см3, твердый | ||
| Температура плавления | 110 ° С (230 ° F, 383 К) | ||
| 269 г / 100 мл (20 ° С) | |||
| Кислотность (пKа) | 0.75 | ||
| Основание конъюгата | Йодат | ||
| −48.0·10−6 см3/ моль | |||
| Опасности | |||
| Главный опасности | кислота, коррозионный, окислитель | ||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | Негорючий | ||
| Родственные соединения | |||
Другой катионы | Литий йодат Йодат калия | ||
Связанный галоген оксокислоты | Хлорная кислота Бромная кислота | ||
Родственные соединения | Йодистоводородная кислота Пятиокись йода Периодическая кислота | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
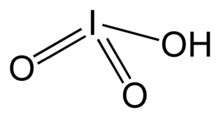
Йодная кислота, HIO3. Это белое водорастворимое твердое вещество. Его надежность контрастирует с нестабильностью хлорная кислота и бромная кислота. Йодная кислота содержит йод со степенью окисления +5 и является одной из самых стабильных оксокислот галогенов. При нагревании образцы обезвоживаются, давая пятиокись йода. При дальнейшем нагревании пятиокись йода разлагается, давая смесь йода, кислорода и низших оксидов йода.
Подготовка
Йодная кислота может производиться окисляющий йод я2 с сильными окислителями, такими как азотная кислота HNO
3, хлор Cl
2, хлорная кислота HClO
3 или же пероксид водорода ЧАС
2О
2,[1] Например:
Характеристики
Йодная кислота - относительно сильная кислота с пKа 0,75. Это сильно окисляющий в кислом растворе, реже в щелочном растворе. Когда йодная кислота действует как окислитель, продуктом реакции является либо йод, либо иодид-ион. В некоторых особых условиях (очень низкий pH и высокая концентрация хлорид-ионов, например, в концентрированной соляной кислоте) йодная кислота восстанавливается до трихлорид йода, соединение золотисто-желтого цвета в растворе, и дальнейшего восстановления не происходит. В отсутствие хлорид-ионов, когда есть избыточное количество восстановителя, все йодат превращается в иодид-ион. Когда имеется избыточное количество йодата, тогда часть йодата превращается в йод. Его можно использовать при подготовке к ионизации с образованием алкилгалогенидов.
Использует
Йодная кислота используется как сильная кислота в аналитическая химия. Его можно использовать для стандартизации решений обоих слабый и сильные основы, с помощью метиловый красный или же метиловый апельсин как индикатор.
Использование в солевой промышленности
Йодную кислоту можно использовать для синтеза натрий или же йодат калия для увеличения йод содержание соли.[нужна цитата ]
Другие оксикислоты
Йодат является частью серии оксикислоты в котором йод может принимать состояния окисления из −1, +1, +3, +5 или +7. Ряд нейтральных оксиды йода также известны.
| Степень окисления йода | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Имя | Йодистый водород | Гипоиодистая кислота | Йодистая кислота | Йодная кислота | Периодическая кислота |
| Формула | ЗДРАВСТВУЙ | HIO | HIO2 | HIO3 | HIO4 или H5IO6 |
Рекомендации
Эта статья нужны дополнительные цитаты для проверка. (Май 2013) (Узнайте, как и когда удалить этот шаблон сообщения) |
- ^ Холлеман, Арнольд Ф .; Виберг, Нильс (2007). Lehrbuch der Anorganischen Chemie (на немецком языке) (102-е изд.). Берлин. ISBN 978-3-11-017770-1.