Органоплатина - Organoplatinum - Wikipedia
Органоплатиновая химия это химия из металлоорганические соединения содержащий углерод к платина химическая связь, а изучение платины как катализатор в органические реакции.[1][2][3] Платинорганические соединения существуют в степень окисления От 0 до IV, причем степень окисления II наиболее распространена. Общий порядок прочности связи: Pt-C (sp)> Pt-O> Pt-N> Pt-C (sp3). Органоплатина и органопалладий химические соединения аналогичны, но платиновые органические соединения более стабильны и поэтому менее полезны в качестве катализаторов.
Органоплатина (0)
Большинство платинорганических (0) соединений содержат алкеновые и алкиновые лиганды. Карбонильные комплексы встречаются редко, аналог Ni (CO)4 неуловимо. Алкеновые и алкиновые лиганды служат двухэлектронными донорами, например, в комплексах (PPh3)2Pt (C2ЧАС4) и (PPh3)2Pt (C2Ph2 ). Этиленовый лиганд в (PPh3)2Pt (C2ЧАС4) является лабильным и обменивается с алкинами и электрофильными алкенами, даже с C60 а фуллерен.
Общий синтетический путь к (PPh3)2Pt (un) (un = алкен, алкин) - восстановление тетрахлороплатинат калия с этанолом гидроксид калия или же гидразин в присутствии фосфинового лиганда, такого как трифенилфосфин и алкен или алкин. Такие реакции протекают через посредство СНГ-дихлорбис (трифенилфосфин) платина (II). Лиганды на основе азота не часто способствуют образованию платиновых комплексов алкенов и алкинов.
Комплексы платины с нулевой валентностью, не содержащие фосфиновых лигандов, часто получают через PtCl.2(ХПК).
- Ли2C8ЧАС8 + PtCl2(ХПК) + 3 ° C7ЧАС10 → [Pt (C7ЧАС10)3] + 2 LiCl + C8ЧАС8 + C8ЧАС12
- Pt (C7ЧАС10)3 + 2 COD → Pt (COD)2 + 3 С7ЧАС10
где C7ЧАС10 является норборнен.
Органоплатина (I)
Соединения платины (I) встречаются нечасто, но обычно являются диамагнитными, поскольку имеют связи Pt-Pt. Примером может служить дикция [Pt2(CO)6]2+.
Органоплатина (II)
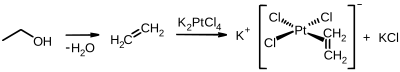
Исторически значимое соединение платины (II) - это Соль Цейзе, который получается из этилен и тетрахлороплатинат калия:
Бесцветный диолефиновый комплекс дихлор (циклоокта-1,5-диен) платина (II) является более современным родственником и более широко используется.
Стабильность и разнообразие алкеновых комплексов платины (II) контрастирует с редкостью алкеновых комплексов никеля (II). Также распространены аллильные комплексы платины. В отличие от химии никеля, где распространены такие соединения, как CpNi (L) X, циклопентадиенил производные Pt (II) редки, что согласуется с нежеланием Pt (II) становиться пентакоординированными.
Алкил- и арил-комплексы платины (II) часто получают окислительная добавка из алкилгалогенид или же арилгалогенид к предшественнику Pt (0), такому как тетракис (трифенилфосфин) платина (0) или Pt (C2ЧАС4) (PPh3)2. С другой стороны, хлориды платины (II) подвержены алкилированию:[4][5]
- PtCl2(SMe2)2 + 2 MeLi → PtMe2(SMe2)2 + 2 LiCl
Диметилсульфидные лиганды в PtMe2(SMe2)2 могут быть замещены другими лигандами.
Многие комплексы платины (II) возникают в результате орто-металлирования и связанных с ним процессов внутримолекулярной активации C-H.
Органоплатина (IV)
Первое когда-либо синтезированное органо-платиновое соединение было иодид триметилплатины из хлорид платины (IV) и метилмагний йодид, сообщает Папа и Пичи в 1907 году.[6][7] Соединение имеет кубаноподобную структуру с четырьмя тройными мостиковыми мостиковыми связями иодидными лигандами. «Тетраметилплатина» была заявлена в 1952 г. Генри Гилман как производное этого тетрамера, но позже было показано, что это утверждение неверно («Тетраметилплатин» оказался [PtMe3ОЙ]4). Соли [PtMe6]2− и [PtMe4]2− были охарактеризованы.[8]

Гидриды платины (IV) встречаются редко.[10] Первые изолированные представители были приготовлены из галогенидов олова или кислот с ортометаллированными соединениями арилплатины (II). Соединение Me (PEt3)2PtOTf обратимо реагирует с трифликовая кислота от -60 до -80 ° C, образуя метан и (PEt3)2Pt (OTf)2 при -20 ° C. Слабых кислот часто бывает достаточно даже воды и спирта и в Активация связи C-H источник протонов - алкан.
Катализ
Гетерогенные катализаторы на основе платины играют важную роль в нефтехимическая промышленность, и предполагается, что эти полезные реакции протекают через поверхностно-связанные платиновые промежуточные соединения. Более определенными, но менее коммерчески значимыми являются гомогенные катализаторы на основе платины.
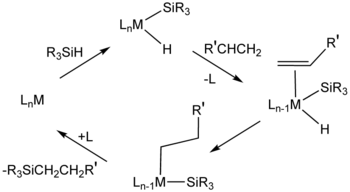
Для гидросилилирования, ЧАС2PtCl6 («Катализатор Шпейера») - важный катализатор. Механизмы этой каталитической системы обычно предполагают промежуточные соединения, содержащие гидрид, силильный лиганд (R3Si) и алкеновые лиганды.[11] Цис-дихлорбис (диэтилсульфид) платина (II) и Катализатор Карстедта (добавление дивинилтетраметилдисилоксан и платинохлористоводородная кислота ) также катализируют гидросилилирование.[12] Много металлодендримеры имеют повторяющиеся звенья на основе платиноорганических соединений.
Темы исследований
Соединения платины причастны к Система Шилова для преобразования метан в метилхлорид. Были предприняты активные попытки, до сих пор безуспешные, для распространения этой реакционной способности на практические методы функционализации метана.[13] Например, платиновые комплексы бипиримидин катализировать превращение метана, кислорода и триоксид серы в метилбисульфат.[14]
Рекомендации
- ^ Никель, палладий и платина (комплексная металлоорганическая химия II) Р.Дж. Puddephatt (редактор) 2002 0080423167
- ^ Синтез металлоорганических соединений: практическое руководство. Санширо Комия Эд. С. Комия, М. Хурано 1997 г.
- ^ Джву-Тинг Чен «Платина: Металлоорганическая химия» в Энциклопедии неорганической химии 2006, John Wiley & Sons, Нью-Йорк. Дои:10.1002 / 0470862106.ia195
- ^ Costa, E .; Pringle, P.G .; Равец, М. (1997). [(1,2,5,6-N) -1,5-Циклооктадиен] Диметил-платина (II). Неорганические синтезы. 31. п. 284. Дои:10.1002 / 9780470132623.ch49. ISBN 9780470132623.
- ^ Хилл, Джеффри С .; Ирвин, Майкл Дж .; Леви, Кристофер Дж .; Рендина, Луи М .; Puddephatt, Ричард Дж. (1998). Комплексы диметилсульфида платины (II). Неорганические синтезы. 32. п. 149. Дои:10.1002 / 9780470132630.ch25. ISBN 9780470132630.
- ^ "Труды химического общества, Том 23, № 323". Труды химического общества (Лондон). 23 (323): 81–94. 1907. Дои:10.1039 / PL9072300081.
- ^ Поуп, W.J .; Пичи, С. Дж. (1909). «LXXIII.? Алкильные соединения платины». Журнал химического общества, Сделки. 95: 571–576. Дои:10.1039 / CT9099500571.
- ^ Greenwood, N. N .; И Эрншоу, А. (1997). Химия элементов (2-е изд.), Оксфорд: Баттерворт-Хайнеманн. ISBN 0-7506-3365-4.
- ^ Ebert, K. H .; Massa, W .; Donath, H .; Lorberth, J .; Seo, B. S .; Хердтвек, Э. (1998). «Платинорганические соединения: VI. Тиометилат триметилплатины и иодид триметилплатины. Кристаллические структуры [(CH3)3PtS (CH3)]4 и [(CH3)3PtI]4· 0,5 канала3Я". J. Organomet. Chem. 559 (1–2): 203–207. Дои:10.1016 / S0022-328X (98) 00414-8.CS1 maint: использует параметр авторов (связь)
- ^ Puddephatt, R. (2001). «Химия гидрида платины (IV)». Обзоры координационной химии. 219–221: 157–185. Дои:10.1016 / S0010-8545 (01) 00325-3.
- ^ К. Эльшенбройх, Металлоорганические соединения (2006) Wiley and Sons-VCH: Weinheim. ISBN 978-3-527-29390-2
- ^ Кеттлер, П. Б. (2003). «Металлы платиновой группы в катализе: изготовление катализаторов и предшественников катализаторов». Исследования и разработки в области органических процессов. 7 (3): 342–354. Дои:10.1021 / op034017o.
- ^ Stahl, Shannon S .; Лабинджер, Джей А .; Bercaw, Джон Э. (1998). «Гомогенное окисление алканов электрофильными металлами с поздним переходом». Angewandte Chemie International Edition. 37 (16): 2180–2192. Дои:10.1002 / (SICI) 1521-3773 (19980904) 37:16 <2180 :: AID-ANIE2180> 3.0.CO; 2-A. PMID 29711451.
- ^ Брайан Г. Хасигучи, Стивен М. Бишоф, Майкл М. Конник, Рой А. Периана (2012). «Разработка катализаторов для функционализации неактивированных связей C – H на основе реакции активации CH». Соотв. Chem. Res. 45 (6): 885–898. Дои:10.1021 / ar200250r. PMID 22482496.CS1 maint: использует параметр авторов (связь)