Алюмоорганическая химия - Organoaluminium chemistry
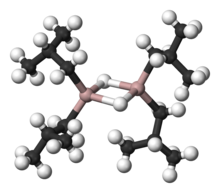
Алюмоорганическая химия это исследование соединений, содержащих связи между углерод и алюминий связь. Это одна из главных тем внутри металлоорганическая химия.[1][2] Иллюстративными алюмоорганическими соединениями являются димеры триметилалюминий, мономер триизобутилалюминий, и соединение титана с алюминием, называемое Реактив Теббе. Поведение алюминийорганических соединений можно понять с точки зрения полярности связи C-Al и высокой Кислотность Льюиса трехкоординированного вида. В промышленности эти соединения в основном используются для производства полиолефины.
История
Первое алюмоорганическое соединение (C2ЧАС5)3Al2я3 был открыт в 1859 году.[3] Однако алюминийорганические соединения были мало известны до 1950-х годов, когда Карл Циглер и его коллеги открыли прямой синтез соединений триалкилалюминия и применили эти соединения для каталитических полимеризация олефинов. Это направление исследований в конечном итоге привело к присуждению Зиглеру Нобелевской премии.
Структура и склеивание
Соединения алюминия (III)
Алюминиевоорганические соединения обычно имеют трех- и четырехкоординатные центры алюминия, хотя и выше. координационные номера наблюдаются с неорганическими лигандами, такими как фторид. В соответствии с обычными тенденциями, четырехкоординатный Al предпочитает быть тетраэдрическим. В отличие от бора алюминий имеет более крупный атом и легко вмещает четыре углеродных лиганда. Таким образом, триорганоалюминиевые соединения обычно являются димерами с парой мосты алкильные лиганды, например, Al2(C2ЧАС5)4(мк-С2ЧАС5)2. Таким образом, несмотря на общее название триэтилалюминия, это соединение содержит два алюминиевых центра и шесть этильные группы. Когда алюминийорганические соединения содержат гидрид или же галогенид эти более мелкие лиганды имеют тенденцию занимать мостиковые участки. Три координации происходит, когда R группы громоздкий, например Al (Mes)3 (Mes = 2,4,6-Me3C6ЧАС2 или же мезитил ) или изобутил.[4]
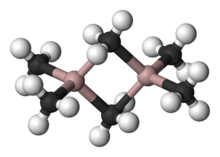
Обмен лиганда в соединениях триалкилалюминия
Димеры триалкилалюминия часто участвуют в динамических равновесиях, в результате чего происходит обмен мостиковыми и концевыми лигандами, а также обмен лигандами между димерами. Даже в нескоординированном растворители, Обмен Al-Me происходит быстро, что подтверждается протонный ЯМР спектроскопия. Например, при −25 ° C 1H ЯМР спектр Me6Al2 содержит два сигнала в соотношении 1: 2, как и ожидалось от твердотельной структуры. При 20 ° C наблюдается только один сигнал, поскольку обмен концевыми и мостиковыми метильными группами происходит слишком быстро, чтобы разрешить его с помощью ЯМР.[5] Высокая кислотность мономеров по Льюису связана с размером центра Al (III) и его тенденцией к достижению конфигурация октета.
Алюминийорганические соединения с низкой степенью окисления
О первом алюминийорганическом соединении со связью Al-Al было сообщено в 1988 г. как (((Me3Si)2CH)2Al)2 (диалан). Обычно их готовят восстановлением хлоридов диалкилалюминия металлическим калием:[6]
- (Р2AlCl)2 + 2 К → R2Al-AlR2 + 2 KCl
Другой примечательной группой аланов являются тетрааланы, содержащие четыре центра Al (I). Эти соединения принимают тетраэдран ядро, как показано (Cp * Al)4 и я3Si3C) Al)4. Кластер [Al12(i-Bu )12]2− был получен из связанных исследований по восстановлению алюминийорганических соединений. Этот дианион принимает структуру икосаэдра, напоминающую додекаборат ([B12ЧАС12]2−). Его формальная степень окисления меньше единицы.
Подготовка
Из алкилгалогенидов и алюминия
В промышленности простые алкилалюминий типа Al2р6 (R = Me, Et) получают в двухэтапном процессе, начиная с алкилирование алюминиевой пудры:
- 2 Al + 3 CH3CH2Cl → (CH3CH2)3Al2Cl3
Реакция напоминает синтез Реактивы Гриньяра. Продукт, (CH3CH2)3Al2Cl3, называется этилалюминий сесквихлорид. Термин сесквихлорид относится к тому факту, что в среднем соотношение Cl: Al составляет 1,5. Эти сесквихлориды можно превратить в триорганоалюминиевые производные путем восстановления:
- 2 (CH3CH2)3Al2Cl3 + 6 Na → (CH3CH2)6Al2 + 2 Al + 6 NaCl
Этот метод используется для производства триметилалюминия и триэтилалюминий.[7]
Гидроалюминирование
Алюминиевый порошок непосредственно реагирует с некоторыми терминальными алкенами в присутствии водорода. Процесс включает в себя две стадии, первая из которых дает гидриды диалкилалюминия. Такие реакции обычно проводятся при повышенных температурах и требуют активации триалкилалюминиевыми реагентами:
- 3 Al + 3/2 H2 + 6 кан.2= CHR → [HAl (CH2CHR)2]3
Для не объемных групп R алюминийорганические гидриды обычно являются тримерными. На следующем этапе эти гидриды обрабатывают большим количеством алкена, чтобы вызвать гидроалюминирование:
- 2 [HAl (CH2CHR)2]3 + 3 канала2= CHR → 3 [Al2(CH2CHR)3
Гидрид диизобутилалюминия, который является димером, получают отщеплением гидрида от триизобутилалюминия:
- 2 я-Bu3Al → (я-Bu2AlH)2 + 2 (CH3)2C = CH2
Карбоалюминирование
Алюминийорганические соединения могут реагировать с алкенами и алкинами, приводя к чистому присоединению одной органильной группы и металлического фрагмента через кратную связь (карбоалюминирование). Этот процесс может протекать чисто термическим способом или в присутствии катализатора переходного металла. Для некаталитического процесса монодобавление возможно только в том случае, если алкен замещен. Для этилена карбоалюминирование приводит к распределение Пуассона высших разновидностей алкилалюминия. Реакция региоселективный для 1-алкенов.[8] Так называемой ZACA реакция впервые сообщил E.-i. Негиши представляет собой пример асимметричного карбоалюминирования алкенов, катализируемого хиральным цирконоценовым катализатором.[9]
Метилалюминирование алкинов в присутствии Cp2ZrCl2[10][11] используется для синтеза стереотипных тризамещенных олефиновых фрагментов, общей субструктуры терпеновых и поликетидных природных продуктов. Синтез (E) -4-иод-3-метилбут-3-ен-1-ол[12] Ниже показано типичное применение этой реакции:
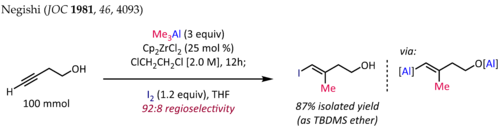
Для терминальных алкинов реакция обычно протекает с хорошей региоселективностью (> 90:10 rr) и полной син селективность, даже в присутствии пропаргильных или гомопропаргильных гетероатомных заместителей. К сожалению, распространение метилалюминирования, катализируемого цирконоценом, до алкилалюминирования высшими алкилами приводит к более низким выходам и плохой региоселективности.
Лабораторные препараты
Хотя простые элементы коммерчески доступны по низкой цене, для их синтеза в лаборатории было разработано множество методов, в том числе метатезис или же трансметалляция. Метатезис трихлорида алюминия с RLi или RMgX дает триалкил:
- AlCl3 + 3 БуЛи → Бу3Al + 3 LiCl
- Трансметалляция
- 2 Al + 3 HgPh2 → 2 AlPh3 + 3 рт.
Реакции
Высокая реакционная способность алюмоорганических соединений по отношению к электрофилам объясняется разделением зарядов между алюминий и углерод атом.
Кислотность Льюиса
Алюмоорганические соединения жесткие кислоты и легко образуют аддукты с такими основаниями, как пиридин, THF и третичные амины. Эти аддукты являются тетраэдрическими по Al.
Электрофилы
Связь Al – C поляризована, поэтому углерод является сильно основным. Кислоты реагируют с образованием алканов. Например, спирты дают алкоксиды:
- AlR '3 + ROH → 1 / n (R '2Al-OR)п + R'H
Помимо простых минеральных кислот, можно использовать широкий спектр кислот. Амины дают производные амидов. С углекислый газ, соединения триалкилалюминия дают карбоксилат диалкилалюминия, а затем дикарбоксилаты алкилалюминия:
- AlR3 + CO2 → R2AlO2CR
- р2AlO2CR + CO2 → RAl (O2CR)2
Преобразование напоминает карбонизацию Реактивы Гриньяра.[13][14][15]
Точно так же реакция между соединениями триалкилалюминия и диоксидом углерода использовалась для синтеза спиртов, олефинов,[13] или кетоны.[16]
С кислород получают соответствующие алкоксиды, которые можно гидролизовать до спиртов:
- AlR3 + 3/2 O2 → Al (ИЛИ)3
Органическийалюминий перекись это [{HC [C (Me) N-C6ЧАС5]2} Al (R) -O-O-CMe3] [R = CH (SiMe3)2].[17]
Реакция между чистыми соединениями триалкилалюминия и воды, спирты, фенолы, амины, углекислый газ, оксиды серы, оксиды азота, галогены, и галогенированные углеводороды может быть жестоким.[18][19]
Полимеризация алкенов
В промышленности алюминийорганические соединения используются в качестве катализаторов полимеризации алкенов для полиолефины, например катализатор метилалюмоксан.
Рекомендации
- ^ Д. Ф. Шрайвер; П. В. Аткинс (2006). Неорганическая химия. Издательство Оксфордского университета. ISBN 978-0199264636.
- ^ М. Витт; Х. В. Роески (2000). «Алюминиево-органохимия на переднем крае исследований и разработок» (PDF). Curr. Наука. 78 (4): 410. Архивировано с оригинал (PDF) на 2014-10-06.
- ^ Hallwachs, W .; Шафарик, А. (1859). "Ueber die Verbindungen der Erdmetalle mit organischen Radicalen". Liebigs Ann. Chem. 109 (2): 206–209. Дои:10.1002 / jlac.18591090214.
- ^ Эльшенбройх, К. (2006). Металлоорганические соединения (3-е изд.). Вайнхайм: Wiley-VCH. ISBN 978-3-527-29390-2.
- ^ Коттон, Фрэнк Альберт; Уилкинсон, Джеффри (1980). Продвинутая неорганическая химия. п. 343. ISBN 978-0-471-02775-1.
- ^ Уль, В. (2004). Элементоорганические соединения, содержащие одинарные связи Al --- Al, Ga --- Ga, In --- In и Tl --- Tl. Adv. Органомет. Chem. Успехи металлоорганической химии. 51. С. 53–108. Дои:10.1016 / S0065-3055 (03) 51002-4. ISBN 9780120311514.
- ^ Майкл Дж. Краузе, Франк Орланди, Альфред Т. Заурадж и Джозеф Р. Зиц «Соединения алюминия, органические» в Энциклопедии промышленной химии Ульмана, 2005, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a01_543
- ^ Барри М. Трост; Мартин Ф. Семмельхак; Ян Флеминг (1992). Комплексный органический синтез: добавления и замены в C-C [pi] -связях. Пергамон. ISBN 9780080405957.
- ^ Негиси, Эй-ичи (2011). «Открытие реакции ZACA: Zr-катализируемое асимметричное карбоалюминирование алкенов». Аркивок. 2011 (viii): 34–53. Дои:10.3998 / ark.5550190.0012.803.
- ^ Негиси, Эй-ичи; Ван, Гуанвэй; Рао, Хунхуа; Сюй, Чжаоцин (14.05.2010). "Алкиновые элементы - перекрестное связывание, катализируемое Pd. К синтезу всех возможных типов ациклических алкенов с высокими выходами, эффективно, селективно, экономично и безопасно:" зеленый "путь". Журнал органической химии. 75 (10): 3151–3182. Дои:10.1021 / jo1003218. ЧВК 2933819. PMID 20465291.
- ^ Негиси, Эй-ичи (2002). Металлоорганические соединения в синтезе: руководство (под ред. М. Шлоссера). Чичестер, Западный Суссекс, Великобритания: Wiley. С. 963–975. ISBN 978-0471984160.
- ^ Rand, Cynthia L .; Хорн, Дэвид Э. Ван; Мур, Марк В .; Негиси, Эйити (01.05.2002). «Универсальный и селективный способ получения дифункциональных тризамещенных (E) -алкен-синтонов посредством катализируемого цирконием карбоалюминирования алкинов». Журнал органической химии. 46 (20): 4093–4096. Дои:10.1021 / jo00333a041.
- ^ а б Юрьев, В.П .; Кучин, А.В .; Толстиков, Г.А. (1974). «Реакция триалкилов алюминия с диоксидом углерода». Органическая и биологическая химия. 23 (4): 817–819. Дои:10.1007 / BF00923507.
- ^ Зиглер, К. (1956). "Neue Entwicklungen der Metallorganischen Synthese". Энгью. Chem. 68 (23): 721–729. Дои:10.1002 / ange.19560682302.
- ^ Захаркин, Л.И .; Гавриленко, В.В .; Иванов, Л.Л. (1967). Ж. Общ. Хим. 377: 992. Отсутствует или пусто
| название =(помощь) - ^ Дэвид В. Маршалл, патент США US3168570, закрепленный за Континентальное масло
- ^ W. Uhl; Б. Яна (2008). «Стойкая перекись алкилалюминия: удивительная стабильность молекулы с сильными восстанавливающими и окислительными функциями в непосредственной близости». Chem. Евро. J. 14 (10): 3067–71. Дои:10.1002 / chem.200701916. PMID 18283706.
- ^ Паспорт безопасности данных Cameo Chemicals
- ^ Безопасное обращение с химическими веществами 1980. стр. 929
