Виртуальный кариотип - Virtual karyotype
Виртуальный кариотип отражает ли цифровая информация кариотип, полученный в результате анализа коротких последовательностей ДНК из определенных локусов по всему геному, которые изолированы и пронумерованы.[1] Он обнаруживает геномные варианты числа копий с более высоким разрешением по уровню, чем при обычном кариотипировании или на основе хромосом сравнительная геномная гибридизация (CGH).[2] Основные методы создания виртуальных кариотипов: сравнительная геномная гибридизация и Массивы SNP.
Фон
А кариотип (Рис.1) - характеристика хромосома дополнение эукариот разновидность.[3][4] Кариотип обычно представляет собой изображение хромосом из одной клетки, расположенное от самой большой (хромосома 1) к самой маленькой (хромосома 22), причем половые хромосомы (X и Y) показаны последними. Исторически кариотипы получали путем окрашивания клеток после того, как они были химически арестованы во время деления клеток. Кариотипы использовались в течение нескольких десятилетий для выявления хромосомных аномалий как в зародышевой линии, так и в раковых клетках. Обычные кариотипы могут оценивать весь геном на предмет изменений в структуре и количестве хромосом, но разрешение относительно низкое, с пределом обнаружения 5-10 МБ.

Метод
В последнее время появились платформы для создания кариотипов высокого разрешения. in silico из нарушенной ДНК, такие как матричная сравнительная геномная гибридизация (arrayCGH) и Массивы SNP. Концептуально массивы состоят из сотен и миллионов зондов, которые дополняют интересующую область генома. Нарушенная ДНК из тестового образца фрагментируется, маркируется и гибридизируется с массивом. Интенсивности гибридизационного сигнала для каждого зонда используются специализированным программным обеспечением для создания логарифмического отношения тест / норма для каждого зонда в массиве. Зная адрес каждого зонда в массиве и адрес каждого зонда в геноме, программа выстраивает зонды в хромосомном порядке и реконструирует геном. in silico (Рис. 2 и 3).
Виртуальные кариотипы имеют значительно более высокое разрешение, чем традиционная цитогенетика. Фактическое разрешение будет зависеть от плотности датчиков на массиве. В настоящее время Affymetrix SNP6.0 - это коммерчески доступный массив самой высокой плотности для приложений виртуального кариотипирования. Он содержит 1,8 миллиона полиморфных и неполиморфных маркеров с практическим разрешением 10–20 КБ, что примерно равно размеру гена. Это примерно в 1000 раз больше разрешения, чем у кариотипов, полученных с помощью традиционной цитогенетики.
Виртуальный кариотип может быть выполнен на образцах зародышевой линии при конституциональных нарушениях,[5][6] и клинические испытания доступны в десятках сертифицированных CLIA лабораторий (genetests.org ). Виртуальное кариотипирование также может быть выполнено на свежих или фиксированных формалином опухолях, залитых парафином.[7][8][9] CLIA-сертифицированные лаборатории, предлагающие тестирование на опухоли, включают: Медицинские лаборатории Крейтон (свежие и залитые в парафин образцы опухолей) и CombiMatrix Молекулярная диагностика (свежие образцы опухоли).


Различные платформы для виртуального кариотипирования
Кариотипирование на основе массива может быть выполнено с помощью нескольких различных платформ, как лабораторных, так и коммерческих. Сами массивы могут быть общегеномными (зонды, распределенные по всему геному) или целевыми (зонды для областей генома, которые, как известно, вовлечены в конкретное заболевание), или их комбинация. Кроме того, в массивах, используемых для кариотипирования, могут использоваться неполиморфные зонды, полиморфные зонды (т.е. содержащие SNP) или их комбинация. Неполиморфные зонды могут предоставить только информацию о количестве копий, в то время как массивы SNP могут предоставить как количество копий, так и статус потери гетерозиготности (LOH) в одном анализе. Типы зондов, используемые для неполиморфных массивов, включают кДНК, клоны ВАС (например, BlueGnome ) и олигонуклеотиды (например, Agilent, Санта-Клара, Калифорния, США или Нимблген, Мэдисон, Висконсин, США). Коммерчески доступные массивы олигонуклеотидных SNP могут быть твердофазными (Affymetrix, Санта-Клара, Калифорния, США) или на основе бусин (Иллюмина, Сан-Диего, Калифорния, США). Несмотря на разнообразие платформ, в конечном итоге все они используют геномную ДНК из разрушенных клеток для воссоздания кариотипа с высоким разрешением. in silico. Конечный продукт еще не имеет последовательного названия и получил название виртуального кариотипирования.[8][10] цифровое кариотипирование,[11] молекулярное аллелокариотипирование,[12] и молекулярное кариотипирование.[13] Другие термины, используемые для описания массивов, используемых для кариотипирования, включают SOMA (микроматрицы олигонуклеотидов SNP)[14] и CMA (хромосомный микрочип).[15][16] Некоторые считают, что все платформы являются своего рода матричная сравнительная геномная гибридизация (arrayCGH), в то время как другие резервируют этот термин для методов с двумя красителями, а третьи разделяют массивы SNP, потому что они генерируют больше и разную информацию, чем методы arrayCGH с двумя красителями.
Приложения
Обнаружение изменений количества копий
Изменения количества копий можно увидеть как в образцах зародышевой линии, так и в образцах опухолей. Изменения количества копий могут быть обнаружены массивами с неполиморфными зондами, такими как arrayCGH, и массивами на основе SNP. Люди диплоидны, поэтому нормальное число копий для неполовых хромосом всегда равно двум.
- Удаления: А удаление потеря генетического материала. Делеция может быть гетерозиготной (число копий 1) или гомозиготной (число копий 0, нуллисомия). Синдромы микроделеции являются примерами конституциональных нарушений из-за небольших делеций в ДНК зародышевой линии. Делеции в опухолевых клетках могут представлять собой инактивацию гена-супрессора опухоли и могут иметь диагностические, прогностические или терапевтические последствия.
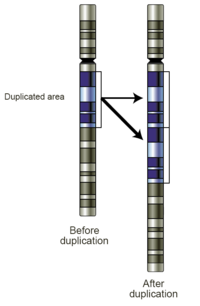
- Прибыль: Увеличение числа копий представляет собой увеличение генетического материала. Если прирост составляет всего одну дополнительную копию сегмента ДНК, это можно назвать дублирование (Рис 4). Если имеется одна дополнительная копия всей хромосомы, ее можно назвать трисомия. Увеличение числа копий в образцах зародышевой линии может быть связано с заболеванием или может быть доброкачественным вариант номера копии. При обнаружении в опухолевых клетках они могут иметь диагностическое, прогностическое или терапевтическое значение.
- Усиления: Технически усиление это тип увеличения количества копий, при котором количество копий> 10. В контексте биологии рака амплификации часто встречаются в онкогены. Это может указывать на худший прогноз, помочь классифицировать опухоль или указывать на соответствие лекарству. Примером приемлемости препарата является амплификация Her2Neu и Герцептин, а также изображение амплификации Her2Neu, обнаруженной с помощью виртуального кариотипирования массива SNP (рис. 5).
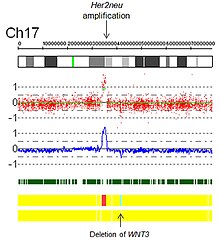 Рис. 5. Усиление Her2 с помощью виртуального кариотипа массива SNP.
Рис. 5. Усиление Her2 с помощью виртуального кариотипа массива SNP.
Утрата гетерозиготности (LOH), аутозиготные сегменты и однопородительская дисомия
Аутозиготный сегменты и однопородная дисомия (UPD) представляют собой диплоидные / «нейтральные к копированию» генетические находки, поэтому их можно обнаружить только с помощью массивов на основе SNP. И автозиготные сегменты, и UPD покажут потеря гетерозиготности (LOH) с числом копий два по кариотипированию массива SNP. Термин «Runs of Homozgygosity» (ROH) - это общий термин, который может использоваться как для аутозиготных сегментов, так и для UPD.
- Аутозиготный сегмент: Аутозиготный сегмент является двупародительским и встречается только в зародышевой линии. Это расширенные серии гомозиготных маркеров в геноме, и они возникают, когда идентичный гаплотип блок унаследован от обоих родителей. Их еще называют "идентичны по происхождению "(IBD), и их можно использовать для картирования гомозиготности.[17][18]
- Однородительская дисомия: UPD возникает, когда обе копии гена или геномной области унаследованы от одного и того же родителя. Это монородительские сегменты, в отличие от автозиготных сегментов, которые являются двойными. Когда они присутствуют в зародышевой линии, они могут быть безвредными или связаны с заболеванием, например: Прадер-Вилли или же Синдромы Ангельмана. Также, в отличие от аутозиготности, UPD может развиваться в опухолевых клетках, и в литературе это называется приобретенным UPD или копи-нейтральным LOH (рис. 6). Приобретенный UPD довольно часто встречается как в гематологических, так и в солидных опухолях, и, как сообщается, составляет от 20 до 80% LOH, наблюдаемого в опухолях человека.[19][20][21][22] Приобретенный UPD может служить вторым хитом в Гипотеза Кнудсона о опухолевом генезе, и, таким образом, может быть биологическим эквивалентом делеции.[23] Поскольку этот тип поражения не может быть обнаружен с помощью arrayCGH, FISH или традиционной цитогенетики, матрицы на основе SNP предпочтительны для виртуального кариотипирования опухолей.
 Рис. 6. Копирование нейтральной LOH / однопородной дисомии.
Рис. 6. Копирование нейтральной LOH / однопородной дисомии.

Фиг. 7 представляет собой виртуальный кариотип массива SNP из колоректальной карциномы, демонстрирующий делеции, прирост, амплификации и приобретенный UPD (копийно-нейтральный LOH).
Примеры клинического применения рака
Виртуальный кариотип может быть создан практически из любой опухоли, но клиническое значение идентифицированных геномных аберраций различно для каждого типа опухоли. Клиническая полезность варьируется, и целесообразность лучше всего определяется онкологом или патологом после консультации с директором лаборатории, выполняющей виртуальный кариотип. Ниже приведены примеры типов рака, в которых клинические последствия конкретных геномных аберраций хорошо известны. Этот список является репрезентативным, но не исчерпывающим. На веб-сайте цитогенетической лаборатории лаборатории гигиены штата Висконсин есть дополнительные примеры клинически значимых генетических изменений, которые легко обнаружить с помощью виртуального кариотипирования.[1]
Нейробластома
На основе серии 493 нейробластома образцов, сообщалось, что общий геномный образец, проверенный кариотипированием на основе массивов, является предиктором исхода при нейробластоме:[24]
- Опухоли, представляющие исключительно изменения числа копий целых хромосом, были связаны с отличной выживаемостью.
- Опухоли с любыми изменениями числа копий сегментных хромосом были связаны с высоким риском рецидива.
- В опухолях, демонстрирующих сегментарные изменения, дополнительными независимыми предикторами снижения общей выживаемости были амплификация MYCN, делеции 1p и 11q и увеличение 1q.
В более ранних публикациях нейробластомы были разделены на три основных подтипа на основе цитогенетических профилей:[25]
- Подтип 1: благоприятная нейробластома с почти триплоидией и преобладанием числовых прибылей и убытков, в основном представляющих неметастатические NB стадии 1, 2 и 4S.
- Подтипы 2A и 2B: обнаруживаются при неблагоприятной широко распространенной нейробластоме, стадии 3 и 4, с потерей 11q и увеличением 17q без амплификации MYCN (подтип 2A) или с амплификацией MYCN, часто вместе с делециями 1p и увеличением 17q (подтип 2B).
Опухоль Вильмса
Опухоль-специфическая потеря гетерозиготности (LOH) для хромосом 1p и 16q идентифицирует подмножество Опухоль Вильмса пациенты, у которых значительно повышен риск рецидива и смерти. LOH для этих хромосомных областей теперь можно использовать в качестве независимого прогностического фактора вместе со стадией заболевания, чтобы нацелить интенсивность лечения на риск неудачи лечения.[26][27]
Карцинома почек
Эпителиальные новообразования почек имеют характерные цитогенетические аберрации, которые могут помочь в классификации.[28] Смотрите также Атлас генетики и цитогенетики в онкологии и гематологии.
- Светлоклеточная карцинома: потеря 3p
- Папиллярный рак: трисомия 7 и 17
- Хромофобная карцинома: гиподиплоид с потерей хромосом 1, 2, 6, 10, 13, 17, 21
Кариотипирование на основе массива может использоваться для выявления характерных хромосомных аберраций в опухолях почек со сложной морфологией.[8][10] Кариотипирование на основе массива хорошо работает с парафиновыми опухолями[29] и поддается рутинному клиническому применению.
Кроме того, недавняя литература указывает на то, что определенные хромосомные аберрации связаны с исходом при определенных подтипах эпителиальных опухолей почек.[30]
Светлоклеточная карцинома почек: del 9p и del 14q - плохие прогностические показатели.[31][32]
Папиллярная почечно-клеточная карцинома: дупликация 1q свидетельствует о смертельном прогрессе.[33]
Хронический лимфолейкоз
Кариотипирование на основе массива - это экономичная альтернатива FISH для выявления хромосомных аномалий в хронический лимфолейкоз (CLL). Несколько клинических валидационных исследований показали> 95% соответствие стандартной панели CLL FISH.[12][34][35][36][37] Кроме того, многие исследования с использованием кариотипирования на основе массивов выявили «атипичные делеции», пропущенные стандартными зондами FISH, и приобретенную однопародительскую дисомию в ключевых локусах для прогностического риска при ХЛЛ.[38][39]
В клетках ХЛЛ распознаются четыре основных генетических отклонения, которые имеют большое влияние на поведение при болезни.[40]
- Делеции части короткого плеча хромосомы 17 (del 17p), которая нацелена на p53, особенно вредны. Пациенты с этой аномалией имеют значительно короткий интервал до начала терапии и более короткую выживаемость. Эта аномалия обнаруживается у 5–10% пациентов с ХЛЛ.
- Делеции длинного плеча на хромосоме 11 (del 11q) также неблагоприятны, хотя и не в такой степени, как при del 17p. Аномалия нацелена на ген ATM и нечасто встречается при ХЛЛ (5–10%).
- Трисомия 12, дополнительная хромосома 12, относительно часто встречается у 20–25% пациентов и дает промежуточный прогноз.
- Делеция 13q14 (del 13q14) является наиболее частой аномалией при ХЛЛ примерно у 50% пациентов с клетками, содержащими этот дефект. Когда del 13q14 рассматривается изолированно, пациенты имеют лучший прогноз, и большинство из них проживут многие годы, даже десятилетия, без необходимости в терапии.
Множественная миелома
Авет-Луазо и др. в Journal of Clinical Oncology использовалось кариотипирование массива SNP 192 множественная миелома (MM) образцы для выявления генетических поражений, связанных с прогнозом, которые затем были проверены в отдельной когорте (n = 273).[41] При ММ отсутствие пролиферативного клона делает традиционную цитогенетику информативной только в ~ 30% случаев. Панели FISH полезны при ММ, но стандартные панели не обнаруживают несколько ключевых генетических аномалий, о которых сообщалось в этом исследовании.
- Виртуальное кариотипирование выявило хромосомные аномалии в 98% случаев ММ
- del (12p13.31) - независимый неблагоприятный маркер
- amp (5q31.1) - благоприятный маркер
- Прогностическое влияние amp (5q31.1) превосходит влияние гипердиплоидии, а также позволяет выявить пациентов, которые получают большую пользу от терапии высокими дозами.
Кариотипирование на основе массива не может обнаружить сбалансированные транслокации, такие как t (4; 14), наблюдаемые в ~ 15% ММ. Следовательно, FISH для этой транслокации также должен выполняться при использовании массивов SNP для обнаружения изменений числа копий в масштабе всего генома, имеющих прогностическое значение для MM.
Медуллобластома
Массивное кариотипирование 260 медуллобластомы Пфистер С. и др. На основании цитогенетических профилей были выделены следующие клинические подгруппы:[42]
- Плохой прогноз: увеличение 6q или усиление MYC или MYCN
- Промежуточный: усиление 17q или i (17q) без усиления 6q или усиления MYC или MYCN
- Отличный прогноз: сбалансированные 6q и 17q или делеция 6q
Олигодендроглиома
Ко-делеция 1p / 19q считается «генетической сигнатурой» олигодендроглиома. Утрата аллелей 1p и 19q, отдельно или вместе, чаще встречается в классических олигодендроглиомах, чем в астроцитомах или олигоастроцитомах.[43] В одном исследовании классические олигодендроглиомы показали потерю 1p в 35 из 42 (83%) случаев, потерю 19q в 28 из 39 (72%), и они были объединены в 27 из 39 (69%) случаев; не было существенной разницы в потере статуса гетерозиготности 1p / 19q между низкосортными и анапластическими олигодендроглиомами.[43] Ко-делеция 1p / 19q коррелировала как с химиочувствительностью, так и с улучшением прогноза при олигодендроглиомах.[44][45] Большинство крупных онкологических центров обычно проверяют делецию 1p / 19q как часть патология отчет о олигодендроглиомах. Статус локусов 1p / 19q можно определить с помощью FISH или виртуального кариотипирования. Преимущество виртуального кариотипирования заключается в оценке всего генома за один анализ, а также локусов 1p / 19q. Это позволяет оценить другие ключевые локусы в глиальных опухолях, такие как статус числа копий EGFR и TP53.
В то время как прогностическая значимость делеций 1p и 19q хорошо известна для анапластических олигодендроглиом и смешанных олигоастроцитом, прогностическая значимость делеций для глиом низкой степени злокачественности более противоречива. Что касается глиом низкой степени злокачественности, недавнее исследование также предполагает, что ко-делеция 1p / 19q может быть связана с транслокацией (1; 19) (q10; p10), которая, как и комбинированная делеция 1p / 19q, связана с более высокой степенью общая выживаемость и выживаемость без прогрессирования у пациентов с глиомой низкой степени злокачественности.[46] Олигодендроглиомы очень редко обнаруживают мутации в гене p53, что контрастирует с другими глиомами.[47] Рецептор эпидермального фактора роста амплификация и цельное коделеция 1p / 19q являются взаимоисключающими и предсказывают совершенно разные исходы, а амплификация EGFR предсказывает плохой прогноз.[48]
Глиобластома
Инь и др.[49] учился 55 глиобластома и 6 клеточных линий GBM с использованием кариотипирования массива SNP. Приобретенный UPD был идентифицирован на 17p в 13 из 61 случаев. Значительно сокращенное время выживания было обнаружено у пациентов с делецией 13q14 (RB) или 17p13.1 (p53) / приобретенным UPD. Взятые вместе, эти результаты предполагают, что этот метод является быстрым, надежным и недорогим методом профилирования полногеномных аномалий при ГБМ. Поскольку кариотипирование массива SNP может быть выполнено на опухолях, залитых парафином, это привлекательный вариант, когда опухолевые клетки не могут расти в культуре для метафазной цитогенетики или когда возникает потребность в кариотипировании после того, как образец был зафиксирован формалином.
Важность выявления приобретенных UPD (копийно-нейтральный LOH) при глиобластоме:
- Из пациентов с аномалией 17p ~ 50% имели делеции и ~ 50% были UPD.
- И 17p del, и 17p UPD были связаны с худшим исходом.
- 9/13 имели гомозиготные мутации TP53, лежащие в основе UPD 17p.
Кроме того, в случаях с неопределенной степенью морфологии геномное профилирование может помочь в диагностике.
- Сопутствующее увеличение на 7 и снижение на 10 по существу патогномонично для ГБМ.[50]
- Амплификация EGFR, потеря PTEN (на 10q) и потеря p16 (на 9p) происходят почти исключительно в глиобластоме и могут предоставить средства для отличия анапластической астроцитомы от глиобластомы.[51]
Острый лимфобластный лейкоз
Цитогенетика, изучение характерных больших изменений хромосомы из раковые клетки, все чаще признается важным предиктором исхода в острый лимфобластный лейкоз (ВСЕ).[52]
NB: сбалансированные транслокации не могут быть обнаружены кариотипированием на основе массива (см. Ограничения ниже).
Некоторые цитогенетические подтипы имеют худший прогноз, чем другие. К ним относятся:
- Транслокация между хромосомы 9 и 22, известные как Филадельфийская хромосома, встречается примерно у 20% взрослых и 5% у детей при ОЛЛ.
- Транслокация между хромосомами 4 и 11 происходит примерно в 4% случаев и чаще всего встречается у детей младше 12 месяцев.
- Не все транслокации хромосом имеют худший прогноз. Некоторые транслокации относительно благоприятны. Например, гипердиплоидия (> 50 хромосом) является хорошим прогностическим фактором.
- Общегеномная оценка изменений числа копий может быть сделана с помощью традиционной цитогенетики или виртуального кариотипирования. Виртуальное кариотипирование массива SNP может обнаруживать изменения количества копий и статус LOH, в то время как arrayCGH может обнаруживать только изменения количества копий. Копировать нейтральный LOH (приобретенная униродительская дисомия) сообщалось в ключевых локусах при ОЛЛ, таких как ген CDKN2A в 9р, которые имеют прогностическое значение.[53][54][55] Виртуальное кариотипирование массива SNP может легко обнаружить копийно-нейтральный LOH. Массив CGH, FISH и обычная цитогенетика не могут обнаружить копийно-нейтральный LOH.
| Цитогенетическое изменение | Категория риска |
|---|---|
| Филадельфийская хромосома | Неблагоприятный прогноз |
| т (4; 11) (q21; q23) | Неблагоприятный прогноз |
| т (8; 14) (q24.1; q32) | Неблагоприятный прогноз |
| Сложный кариотип (более четырех аномалий) | Неблагоприятный прогноз |
| Низкий гиподиплоидия или рядом триплоидия | Неблагоприятный прогноз |
| Высоко гипердиплоидия | Хороший прогноз |
| дель (9п) | Хороший прогноз |
Корреляция прогноза с цитогенетическими данными костного мозга при остром лимфобластном лейкозе
| Прогноз | Цитогенетические данные |
|---|---|
| Благоприятный | Гипердиплоидия> 50; т (12; 21) |
| Средний | Гипердиолоидия 47-50; Нормальный (диплоидия); дель (6q); Перестройки 8q24 |
| Неблагоприятный | Гиподиплоидия - близкая гаплоидия; Рядом с тетраплоидией; дель (17п); т (9; 22); т (11q23) |
Считается, что неклассифицированный ОЛЛ имеет промежуточный прогноз.[56]
Миелодиспластический синдром
Миелодиспластический синдром (MDS) имеет значительную клиническую, морфологическую и генетическую неоднородность. Цитогенетика играет решающую роль в основанной на классификации Международной системе прогностической оценки (IPSS) для МДС, разработанной Всемирной организацией здравоохранения.[57][58]
- Хороший прогноз: нормальный кариотип, изолированный del (5q), изолированный del (20q), -Y
- Плохой прогноз: сложные аномалии (т. Е.> = 3 аномалии), −7 или del (7q)
- Промежуточный прогноз: все другие аномалии, включая трисомию 8 и del (11q).
При сравнении метафазной цитогенетики, панели FISH и кариотипирования массива SNP для МДС было обнаружено, что каждый метод обеспечивает аналогичную диагностическую ценность. Ни один метод не обнаружил все дефекты, а уровень обнаружения улучшился примерно на 5% при использовании всех трех методов.[59]
Приобретенный UPD, который не может быть обнаружен с помощью FISH или цитогенетики, был зарегистрирован в нескольких ключевых локусах при МДС с использованием кариотипирования массива SNP, включая делецию 7 / 7q.[60][61]
Миелопролиферативные новообразования / миелопролиферативные заболевания
Филадельфийская хромосома отрицательная миелопролиферативные новообразования (MPN), включая истинную полицитемию, эссенциальную тромбоцитемию и первичный миелофиброз, демонстрируют врожденную тенденцию к трансформации в лейкоз (фаза MPN-бласта), которая сопровождается приобретением дополнительных геномных повреждений. В исследовании 159 случаев,[62] Анализ массива SNP позволил выявить практически все цитогенетические аномалии и выявить дополнительные поражения с потенциально важными клиническими последствиями.
- Количество геномных изменений было более чем в 2–3 раза больше в бластной фазе, чем в хронической фазе заболевания.
- Делеция 17p (TP53) была в значительной степени связана с предшествующим воздействием гидроксимочевины, а также со сложным кариотипом в образцах с кризисом MPN-бласта. И делеция, и 17p-копийный нейтральный LOH были связаны со сложным кариотипом, плохим прогностическим маркером миелоидных злокачественных новообразований. Копирующий нейтральный LOH (приобретенный UPD) легко определяется кариотипом массива SNP, но не цитогенетикой, FISH или массивом CGH.
- Пациенты с бластной фазой с потерей хромосомного материала на 7q показали плохую выживаемость. Известно, что потеря 7q является предиктором быстрого прогрессирования и плохого ответа на терапию ОМЛ. Пациенты с фазой MPN-бласта с цитогенетически неопределяемым 7q копий нейтральным LOH имели сравнимую выживаемость с пациентами с 7 / 7q в их лейкозных клетках.
- 9p копия нейтрального LOH с гомозиготной мутацией JAK2 также была связана с худшим исходом в кризисе MPN-бласта по сравнению с пациентами с гетерозиготным JAK2V617F или JAK2 дикого типа. В отличие от LOH на 17p, прогностическое влияние 9pCNN-LOH не зависело от установленных факторов риска, таких как 7 / 7q, 5q или сложный кариотип.
Колоректальный рак
Идентификация биомаркеров в колоректальный рак особенно важен для пациентов со II стадией заболевания, когда рецидив опухоли наблюдается менее чем у 20%. 18q LOH - установленный биомаркер, связанный с высоким риском рецидива опухоли при раке толстой кишки II стадии.[63] На рис. 7 показан кариотип массива SNP колоректальной карциномы (вид на весь геном).
Колоректальный рак классифицируется по определенным опухолевым фенотипам на основе молекулярных профилей.[63] которые можно интегрировать с результатами других дополнительных тестов, таких как тестирование микросателлитной нестабильности, IHC и статус мутации KRAS:
- Хромосомная нестабильность (CIN), которая имеет аллельный дисбаланс по ряду хромосомных локусов, включая 5q, 8p, 17p и 18q (рис. 7).
- Микросателлитная нестабильность (MSI), имеющая тенденцию к диплоидному кариотипу.
Злокачественные рабдоидные опухоли
Злокачественные рабдоидные опухоли редкие, очень агрессивные новообразования, чаще всего обнаруживаемые у младенцев и детей младшего возраста. Из-за их гетерогенных гистологических особенностей диагностика часто может быть затруднена, и возможна ошибочная классификация. В этих опухолях ген INI1 (SMARCB1) на хромосоме 22q функционирует как классический ген-супрессор опухоли. Инактивация INI1 может происходить через делецию, мутацию или приобретенный UPD.[64]
В недавнем исследовании[64] Кариотипирование массива SNP выявило делеции или LOH 22q в 49/51 рабдоидных опухолях. Из них 14 были копийно-нейтральными LOH (или приобретенными UPD), которые можно обнаружить с помощью кариотипирования массива SNP, но не с помощью FISH, цитогенетики или arrayCGH. MLPA обнаружила гомозиготную делецию одного экзона в одном образце, которая была ниже разрешающей способности массива SNP.
Кариотипирование массива SNP можно использовать, чтобы отличить, например, медуллобластому с изохромосомой 17q от первичной рабдоидной опухоли с потерей 22q11.2. Если указано, затем можно использовать молекулярный анализ INI1 с использованием MLPA и прямого секвенирования. После обнаружения связанных с опухолью изменений можно провести анализ ДНК зародышевой линии пациента и родителей, чтобы исключить наследственную или de novo мутацию зародышевой линии или делецию INI1, чтобы можно было провести соответствующую оценку риска рецидива.[64]
Увеальная меланома
Наиболее важное генетическое изменение, связанное с плохим прогнозом увеальная меланома потеря всей копии Хромосома 3 (Моносомия 3), что сильно коррелирует с метастатическим распространением.[65] Прирост по хромосомам 6 и 8 часто используются для уточнения прогностической ценности экрана моносомии 3, причем усиление 6p указывает на лучший прогноз, а усиление 8q указывает на худший прогноз в дисомия 3 опухоли.[66] В редких случаях опухоли моносомии 3 могут дублировать оставшуюся копию хромосомы, чтобы вернуться в дисомное состояние, называемое изодисомия.[67] Изодизомия 3 прогностически эквивалентна моносомии 3, и обе могут быть обнаружены с помощью тестов на хромосому 3. потеря гетерозиготности.[68]
Ограничения
В отличие от кариотипов, полученных с помощью традиционной цитогенетики, виртуальные кариотипы реконструируются компьютерными программами с использованием сигналов, полученных из разрушен ДНК. По сути, компьютерная программа исправляет транслокации, когда выстраивает сигналы в хромосомном порядке. Следовательно, виртуальные кариотипы не могут обнаружить сбалансированные транслокации и инверсии. Они также могут обнаруживать генетические аберрации только в тех областях генома, которые представлены зондами на матрице. Кроме того, виртуальные кариотипы создают родственник число копий нормализовано относительно диплоидного генома, поэтому тетраплоидные геномы будут конденсироваться в диплоидное пространство, если не выполняется перенормировка. Для перенормировки требуется дополнительный анализ на основе клеток, такой как FISH, если используется arrayCGH. Для кариотипов, полученных из массивов на основе SNP, о тетраплоидии часто можно судить по поддержанию гетерозиготности в области очевидной потери числа копий.[22] Мозаицизм низкого уровня или небольшие субклоны не могут быть обнаружены виртуальными кариотипами, потому что присутствие нормальных клеток в образце ослабляет сигнал от аномального клона. Точная точка отказа с точки зрения минимального процента неопластических клеток будет зависеть от конкретной платформы и используемых алгоритмов. Многие программы анализа числа копий, используемые для генерации кариотипов на основе массивов, будут давать сбои при менее 25–30% опухолевых / аномальных клеток в образце. Однако в онкологических приложениях это ограничение можно минимизировать с помощью стратегий обогащения опухолей и программного обеспечения, оптимизированного для использования с онкологическими образцами. Алгоритмы анализа быстро развиваются, и некоторые из них даже рассчитаны на «нормальное заражение клонами»,[69] поэтому ожидается, что это ограничение будет и дальше исчезать.
Смотрите также
- РАСШИФРОВАТЕЛЬ, База данных хромосомного дисбаланса и фенотипа у людей с использованием Ensembl Resources
Рекомендации
- ^ Цифровое кариотипирование - Wang et al., 10.1073 / pnas.202610899 - Proceedings of the National Academy of Sciences
- ^ Шинави М., Чунг С.В. (2008). «Массив CGH и его клиническое применение». Drug Discov сегодня. 13 (17–18): 760–70. Дои:10.1016 / j.drudis.2008.06.007. PMID 18617013.
- ^ Белый M.J.D. 1973 г. Хромосомы. 6-е изд., Chapman & Hall, Лондон. стр.28
- ^ Стеббинс Г. Л. 1950. Вариации и эволюция растений. Глава XII: Кариотип. Columbia University Press N.Y.
- ^ Шаффер Л.Г., Беджани Б. (2006). «Медицинские применения массива CGH и трансформация клинической цитогенетики». Cytogenet. Genome Res. 115 (3–4): 303–9. Дои:10.1159/000095928. PMID 17124414.
- ^ Эдельманн Л., Хиршхорн К. (январь 2009 г.). «Клиническая полезность массива CGH для обнаружения хромосомного дисбаланса, связанного с умственной отсталостью и множественными врожденными аномалиями». Летопись Нью-Йоркской академии наук. 1151 (1): 157–66. Дои:10.1111 / j.1749-6632.2008.03610.x. PMID 19154522.
- ^ Датт А., Бероухим Р. (январь 2007 г.). "Анализ массива однонуклеотидного полиморфизма рака". Текущее мнение в области онкологии. 19 (1): 43–9. Дои:10.1097 / CCO.0b013e328011a8c1. PMID 17133111.
- ^ а б c Hagenkord JM; Парвани А.В.; Lyons-Weiler MA; Альварес К; Amato R; Gatalica Z; Гонсалес-Берджон JM; Петерсон Л; Dhir R; Monzon FA (ноябрь 2008 г.). «Виртуальное кариотипирование с помощью микрочипов SNP снижает неопределенность в диагностике опухолей почечного эпителия». Диагно Патол. 3 (1): 44. Дои:10.1186/1746-1596-3-44. ЧВК 2588560. PMID 18990225.
- ^ Боде А.Л., Бельмонт Дж. (2008). «ДНК-диагностика на основе массивов: пусть начнется революция». Анну Рев Мед. 59 (1): 113–29. Дои:10.1146 / annurev.med.59.012907.101800. PMID 17961075.
- ^ а б Monzon FA; Hagenkord JM; Lyons-Weiler MA; Balani JP; Парвани А.В.; Sciulli CM; Ли Дж; Chandran UR; Бастаки С.И.; Дхир Р. (май 2008 г.). «Полногеномные массивы SNP как потенциальный диагностический инструмент для обнаружения характерных хромосомных аберраций в опухолях почечного эпителия». Мод Pathol. 21 (5): 599–608. Дои:10.1038 / modpathol.2008.20. PMID 18246049.
- ^ Лири Р.Дж.; Lin JC; Cummins J; Boca S; Дерево LD; Парсонс DW; Джонс С; Sjöblom T; Park BH; Парсонс Р; Уиллис Дж; Dawson D; Уилсон Дж. К.; Никольская Т; Никольский Y; Копелович Л; Пападопулос Н; Pennacchio LA; Ван Т.Л .; Марковиц С.Д .; Parmigiani G; Kinzler KW; Фогельштейн B; Велкулеску В.Е. (2008). «Комплексный анализ гомозиготных делеций, очаговых амплификаций и изменений последовательностей при раке груди и колоректального рака». Proc Natl Acad Sci U S A. 105 (42): 16224–9. Дои:10.1073 / pnas.0808041105. ЧВК 2571022. PMID 18852474.
- ^ а б Lehmann S; Огава С; Raynaud SD; Sanada M; Няня Ы; Ticchioni M; Ублюдок C; Kawamata N; Koeffler HP (март 2008 г.). «Молекулярное аллелокариотипирование нелеченой ранней стадии хронического лимфоцитарного лейкоза». Рак. 112 (6): 1296–305. Дои:10.1002 / cncr.23270. PMID 18246537.
- ^ Vermeesch JR; Fiegler H; de Leeuw N; Szuhai K; Schoumans J; Ciccone R; Speleman F; Раух А; Клейтон-Смит Дж; Ван Равенсваай К; Sanlaville D; Patsalis PC; Ферт H; Devriendt K; Зуффарди О. (ноябрь 2007 г.). «Рекомендации по молекулярному кариотипу в конституциональной генетической диагностике». Eur J Hum Genet. 15 (11): 1105–14. Дои:10.1038 / sj.ejhg.5201896. PMID 17637806.
- ^ Кульхарья А.С., Фланнери ДБ, Норрис К., Ловелл С., Леви Б., Велагалети Г. (сентябрь 2008 г.). «Точное картирование контрольных точек у двух неродственных пациентов с редкими перекрывающимися интерстициальными делециями 9q с легкими дисморфическими особенностями». Американский журнал медицинской генетики. 146A (17): 2234–41. Дои:10.1002 / ajmg.a.32397. PMID 18666229.
- ^ Новаковская Б; Станкевич П; Obersztyn E; Ou Z; Ли Дж; Chinault AC; Смык М; Borg K; Mazurczak T; Cheung SW; Босиан Э. (сентябрь 2008 г.). «Применение метафазного HR-CGH и целевого анализа хромосомных микрочипов для геномной характеристики 116 пациентов с умственной отсталостью и дисморфическими особенностями». Американский журнал медицинской генетики. 146A (18): 2361–9. Дои:10.1002 / ajmg.a.32475. PMID 18698622.
- ^ Probst FJ; Roeder ER; Enciso VB; Ou Z; Cooper ML; Eng P; Ли Дж; Парень; Страттон РФ; Chinault AC; Shaw CA; Саттон VR; Cheung SW; Нельсон Д.Л. (июнь 2007 г.). «Хромосомный микроматричный анализ (CMA) обнаруживает большую делецию Х-хромосомы, включая FMR1, FMR2 и IDS, у пациентки с умственной отсталостью». Американский журнал медицинской генетики. 143A (12): 1358–65. Дои:10.1002 / ajmg.a.31781. PMID 17506108.
- ^ Hildebrandt, F; и другие. (Январь 2009 г.). «Системный подход к картированию генов рецессивных заболеваний у людей из беспородных популяций». PLOS Genet. 5 (1): e1000353. Дои:10.1371 / journal.pgen.1000353. ЧВК 2621355. PMID 19165332.
- ^ McQuillan R; Leutenegger AL; Абдель-Рахман Р; Франклин С.С.; Pericic M; Barac-Lauc L; Смолей-Наранчич Н; Janicijevic B; Поласек О; Tenesa A; Macleod AK; Фаррингтон С.М.; Рудан П; Hayward C; Vitart V; Рудан I; Wild SH; Dunlop MG; Райт А.Ф .; Кэмпбелл H; Уилсон Дж. Ф. (2008). «Беги гомозиготности в европейских популяциях». Am J Hum Genet. 83 (3): 359–72. Дои:10.1016 / j.ajhg.2008.08.007. ЧВК 2556426. PMID 18760389.
- ^ Gondek LP, Tiu R, O'Keefe CL, Sekeres MA, Theil KS, Maciejewski J (февраль 2008 г.). «Хромосомные поражения и однопородительская дисомия, обнаруженные с помощью массивов SNP при МДС, МДС / MPD и ОМЛ на основе МДС». Кровь. 111 (3): 1534–42. Дои:10.1182 / кровь-2007-05-092304. ЧВК 2214746. PMID 17954704.
- ^ Бероухим Р; Lin M; Парк Y; Ха, хорошо; Чжао X; Garraway LA; Fox EA; Hochberg EP; Меллингхофф И.К .; Hofer MD; Descazeaud A; Рубин М.А.; Мейерсон М; Вонг WH; Продавцы WR; Ли С (май 2006 г.). «Выявление потери гетерозиготности из непарных опухолей с использованием массивов олигонуклеотидных SNP высокой плотности». PLOS Comput. Биол. 2 (5): e41. Дои:10.1371 / journal.pcbi.0020041. ЧВК 1458964. PMID 16699594.
- ^ Ishikawa S; Komura D; Tsuji S; Нисимура К; Ямамото S; Панда Б; Хуанг Дж; Fukayama M; Джонс KW; Абуратани Х. (август 2005 г.). «Анализ дозировки аллелей с помощью микрочипов генотипирования». Biochem Biophys Res Commun. 333 (4): 1309–14. Дои:10.1016 / j.bbrc.2005.06.040. PMID 15982637.
- ^ а б Lo KC, Bailey D, Burkhardt T., Gardina P, Turpaz Y, Cowell J (март 2008 г.). «Комплексный анализ случаев потери гетерозиготности в глиобластоме с использованием массивов картирования 100K SNP и сравнение с аномалиями числа копий, определенными сравнительной геномной гибридизацией массива ВАС». Гены Хромосомы Рак. 47 (3): 221–37. Дои:10.1002 / gcc.20524. PMID 18050302.
- ^ Мао X, Young BD, Лу И (июнь 2007 г.). «Применение микрочипов однонуклеотидного полиморфизма в исследованиях рака». Curr Genomics. 8 (4): 219–28. Дои:10.2174/138920207781386924. ЧВК 2430687. PMID 18645599.
- ^ Janoueix-Lerosey I, Schleiermacher G, Michels E, et al. (Март 2009 г.). «Общий геномный паттерн является предиктором исхода нейробластомы». J. Clin. Онкол. 27 (7): 1026–33. Дои:10.1200 / JCO.2008.16.0630. PMID 19171713.
- ^ Михельс Э., Вандесомпеле Дж., Хобек Дж., Ментен Б., Де Претер К., Лаурис Дж., Ван Рой Н., Спелеман Ф (2006). «Полногеномное измерение изменений числа копий ДНК в нейробластоме: рассечение ампликонов и картирование потерь, прироста и контрольных точек». Cytogenet. Genome Res. 115 (3–4): 273–282. Дои:10.1159/000095924. PMID 17124410.
- ^ Messahel B; Williams R; Ридольфи А; A'hern R; Уоррен В; Tinworth L; Hobson R; Аль-Саади Р; Whyman G; Брандлер MA; Келси А; Sebire N; Джонс С; Вуянич G; Причард-Джонс К; Детская группа по раку и лейкемии (CCLG) (март 2009 г.). «Детская группа по раку и лейкемии (CCLG). Потеря аллелей на 16q определяет худший прогноз опухоли Вильмса независимо от подхода к лечению в клинических испытаниях UKW1-3: исследование детской группы рака и лейкемии (CCLG)». Eur J Cancer. 45 (5): 819–26. Дои:10.1016 / j.ejca.2009.01.005. PMID 19231157.
- ^ Гранди PE; Breslow NE; Li S; Perlman E; Беквит Джей Би; Ричи ML; Шамбергер RC; Haase GM; D'Angio GJ; Дональдсон М; Coppes MJ; Малоголовкин М; Shearer P; Томас PR; Macklis R; Tomlinson G; Хафф V; Зеленая DM; Национальная группа по изучению опухолей Вильмса (октябрь 2005 г.). «Национальная группа исследования опухолей Вильмса. Потеря гетерозиготности по хромосомам 1p и 16q является неблагоприятным прогностическим фактором при благоприятной гистологии опухоли Вильмса: отчет Национальной группы исследования опухолей Вильмса». J Clin Oncol. 23 (29): 7312–21. Дои:10.1200 / JCO.2005.01.2799. PMID 16129848.
- ^ ван ден Берг, Э; Стёркель, S (2003). «Почки: светлоклеточная почечно-клеточная карцинома». Атлас Генет Цитогенет Онкол Гематол. 7 (3): 424–431. Получено 14 декабря 2010.
- ^ Lyons-Weiler MA, Hagenkord JM, Sciulli CM, Dhir R, Monzon F (2008). «Оптимизация анализа Affymetrix GeneChip Mapping 10K 2.0 для рутинного клинического использования на фиксированных формалином парафиновых тканях». Путь Диаг-Мол. 17 (1): 3–13. Дои:10.1097 / PDM.0b013e31815aca30. PMID 18303412.
- ^ Klatte T; Pantuck AJ; Сказал JW; Селигсон БД; Рао Н.П .; LaRochelle JC; Shuch B; Зисман А; Каббинавар Ф.Ф .; Belldegrun AS (2009). «Цитогенетическое и молекулярное профилирование опухолей для папиллярно-клеточной карциномы 1 и 2 типа». Клинические исследования рака. 15 (4): 1162–9. Дои:10.1158 / 1078-0432.CCR-08-1229. PMID 19228721.
- ^ Brunelli M; Эккер А; Gobbo S; Ficarra V; Novara G; Cossu-Rocca P; Bonetti F; Menestrina F; Cheng L; Eble JN; Мартинони Г (2008). «Потеря хромосомы 9p является независимым прогностическим фактором у пациентов со светлоклеточной почечно-клеточной карциномой». Современная патология. 21 (1): 1–6. Дои:10.1038 / modpathol.3800967. PMID 17906617.
- ^ Klatte T; Рао ПН; де Мартино М; LaRochelle J; Shuch B; Зомородян N; Сказал J; Каббинавар Ф.Ф .; Belldegrun AS; Пантак Эй Джей (2009). «Цитогенетический профиль предсказывает прогноз пациентов со светлоклеточным почечно-клеточным раком». Журнал клинической онкологии. 27 (5): 746–53. Дои:10.1200 / JCO.2007.15.8345. PMID 19124809.
- ^ Шпонар А, Зубаков Д, Павляк Дж, Эмили А, Ковач Г (2009). «Три генетических стадии развития папиллярных почечно-клеточных опухолей: дупликация хромосомы 1q означает фатальное прогрессирование». Международный журнал рака. 124 (9): 2071–6. Дои:10.1002 / ijc.24180. PMID 19123481.
- ^ Schwaenen C; Nessling M; Wessendorf S; Salvi T; Wrobel G; Radlwimmer B; Kestler HA; Haslinger C; Stilgenbauer S; Döhner H; Bentz M; Лихтер П. (2004). «Автоматизированное геномное профилирование на основе массива при хроническом лимфолейкозе: разработка клинического инструмента и обнаружение повторяющихся геномных изменений». Proc Natl Acad Sci U S A. 101 (4): 1039–44. Дои:10.1073 / pnas.0304717101. ЧВК 327147. PMID 14730057.
- ^ Pfeifer D; Pantic M; Скатулла I; Rawluk J; Kreutz C; Martens UM; Fisch P; Тиммер Дж; Велкен Х (февраль 2007 г.). «Полногеномный анализ изменений числа копий ДНК и LOH при ХЛЛ с использованием массивов SNP высокой плотности». Кровь. 109 (3): 1202–10. Дои:10.1182 / кровь-2006-07-034256. PMID 17053054.
- ^ Gunn SR; Мохаммед М.С. Gorre ME; Коттер ПД; Ким Дж; Bahler DW; Преображенский С.Н.; Хиггинс Р.А.; Bolla AR; Ismail SH; де Йонг Д; Eldering E; van Oers MH; Меллинк СН; Китинг MJ; Schlette EJ; Абруццо LV; Робеторье РС (сентябрь 2008 г.). «Сканирование всего генома с помощью сравнительной геномной гибридизации массива как клинический инструмент для оценки риска хронического лимфолейкоза». Журнал молекулярной диагностики. 10 (5): 442–451. Дои:10.2353 / jmoldx.2008.080033. ЧВК 2518739. PMID 18687794.
- ^ Сарджент Р; Джонс Д; Абруццо LV; Яо Х; Bonderover J; Cisneros M; Wierda WG; Китинг MJ; Лутра Р. (январь 2009 г.). «Индивидуальная сравнительная геномная гибридизация на основе массива олигонуклеотидов в качестве клинического анализа геномного профилирования хронического лимфолейкоза». Дж Мол Диаг. 11 (1): 25–34. Дои:10.2353 / jmoldx.2009.080037. ЧВК 2607562. PMID 19074592.
- ^ 2009 Май; 23 (5): 829-33
- ^ Хагенкорд JM, Monzon FA, Kash SF, Lilleberg S, Xie Q, Kant JA (2010). «Кариотипирование на основе массивов для прогностической оценки при хроническом лимфолейкозе: сравнение производительности массивов affymetrix 10K2.0, 250K Nsp и SNP6.0». Дж Мол Диаг. 12 (2): 184–96. Дои:10.2353 / jmoldx.2010.090118. ЧВК 2871725. PMID 20075210.
- ^ Dohner H, Stilgenbauer S, Benner A и др. (2000). «Геномные аберрации и выживаемость при хроническом лимфолейкозе». NEJM. 343 (26): 1910–6. Дои:10.1056 / NEJM200012283432602. PMID 11136261.
- ^ Эрве Авет-Луазо; Ченг Ли; Флоренс Магтензия; Вильфрид Гуро; Кэтрин Шарбоннель; Жан-Люк Гаруссо; Мишель Атталь; Джеральд Марит; Клэр Матиот; Тьерри Факон; Филипп Моро; Кеннет С. Андерсон; Лоик Кэмпион; Никхил С. Мунши; Стефан Минвьель (сентябрь 2009 г.). «Прогностическое значение изменений числа копий при множественной миеломе». Журнал клинической онкологии. 27 (27): 4585–90. Дои:10.1200 / JCO.2008.20.6136. ЧВК 2754906. PMID 19687334.
- ^ Pfister S; Ремке М; Беннер А; Mendrzyk F; Toedt G; Felsberg J; Виттманн А; Devens F; Гербер НУ; Joos S; Кулозик А; Reifenberger G; Рутковски S; Вистлер OD; Radlwimmer B; Scheurlen W; Lichter P; Коршунов А (апрель 2009 г.). «Прогнозирование исходов медуллобластомы у детей на основе аберраций числа копий ДНК хромосом 6q и 17q и локусов MYC и MYCN». J Clin Oncol. 27 (10): 1627–1636. Дои:10.1200 / JCO.2008.17.9432. PMID 19255330.
- ^ а б Барбашина В., Салазар П., Holland EC, Rosenblum MK, Ladanyi M (1 февраля 2005 г.). «Потери аллелей на 1p36 и 19q13 в глиомах: корреляция с гистологической классификацией, определение минимальной удаленной области размером 150 т.п.н. на 1p36 и оценка CAMTA1 в качестве гена-кандидата опухолевого супрессора». Clin. Рак Res. 11 (3): 1119–28. PMID 15709179.
- ^ Laigle-Donadey F, Benouaich-Amiel A, Hoang-Xuan K, Sanson M (2005). «[Молекулярная биология олигодендроглиальных опухолей]». Нейро-Хирургия (На французском). 51 (3–4, часть 2): 260–8. Дои:10.1016 / s0028-3770 (05) 83487-3. PMID 16292170.
- ^ Уокер С., Хейлок Б., Муж Д. и др. (2006). «Клиническое использование генотипа для прогнозирования химиочувствительности при олигодендроглиальных опухолях». Неврология. 66 (11): 1661–7. Дои:10.1212 / 01.wnl.0000218270.12495.9a. PMID 16769937.
- ^ Дженкинс РБ, Блэр Х., Баллман К.В. и др. (Октябрь 2006 г.). «A t (1; 19) (q10; p10) опосредует комбинированные делеции 1p и 19q и предсказывает лучший прогноз пациентов с олигодендроглиомой». Рак Res. 66 (20): 9852–61. Дои:10.1158 / 0008-5472.CAN-06-1796. PMID 17047046.
- ^ Огаки Х., Эйбл Р.Х., Вистлер О.Д., Ясаргил М.Г., Ньюкомб Е.В., Клейхуес П. (15 ноября 1991 г.). «Мутации p53 в неастроцитарных опухолях головного мозга человека». Рак Res. 51 (22): 6202–5. PMID 1933879.
- ^ Ducray F, Idbaih A, de Reyniès A, et al. (2008). «Анапластические олигодендроглиомы с коделецией 1p19q имеют профиль экспрессии пронейрального гена». Мол. Рак. 7 (1): 41. Дои:10.1186/1476-4598-7-41. ЧВК 2415112. PMID 18492260.
- ^ Дун Инь; Сейши Огава; Норихико Кавамата; Патриция Туничи; Гаэтано Финоккиаро; Марика Эоли; Кристиан Рукерт; Thien Huynh; Гентао Лю; Мотохиро Като; Масаси Санада; Анна Яух; Мартин Дугас; Кейт Л. Блэк; Х. Филип Кёффлер (май 2009 г.). "Профилирование числа копий генома мультиформной глиобластомы с помощью ДНК-микрочипа с полиморфизмом одного нуклеотида с высоким разрешением". Мол Рак Res. 7 (5): 665–77. Дои:10.1158 / 1541-7786.MCR-08-0270. PMID 19435819.
- ^ Цитогенетика рака, 3-е изд., Глава 19, Опухоли нервной системы, Уайли Блэквелл, 2009.
- ^ Опухоли центральной нервной системы. Том 7. Вашингтон, округ Колумбия: Американский регистр патологии; 2007 г.
- ^ Мурман А., Харрисон С., Бак Дж., Ричардс С., Секер-Уокер Л., Мартино М., Вэнс Дж., Черри А., Хиггинс Р., Филдинг А., Форони Л., Пайетта Е., Таллман М., Литцов М., Верник П., Роу Дж., Голдстоун А, Девальд Г (2007). «Кариотип является независимым прогностическим фактором при остром лимфобластном лейкозе (ОЛЛ) у взрослых: анализ цитогенетических данных пациентов, получавших лечение в исследовании UKALLXII / Восточной кооперативной онкологической группы (ECOG) 2993 Совета медицинских исследований (MRC)». Кровь. 109 (8): 3189–97. Дои:10.1182 / кровь-2006-10-051912. PMID 17170120.
- ^ Kawamata N; Огава С; Zimmermann M; Като М; Sanada M; Хемминки К; Yamatomo G; Няня Ы; Koehler R; Flohr T; Миллер CW; Харботт Дж; Людвиг WD; Stanulla M; Schrappe M; Бартрам CR; Koeffler HP (январь 2008 г.). «Молекулярное аллелокариотипирование острых лимфобластных лейкозов у детей с помощью полиморфного олигонуклеотидного геномного микрочипа с высоким разрешением». Кровь. 111 (2): 776–84. Дои:10.1182 / кровь-2007-05-088310. ЧВК 2200831. PMID 17890455.
- ^ Bungaro S; Dell'Orto MC; Zangrando A; Basso D; Горлетта Т; Lo Nigro L; Leszl A; Young BD; Basso G; Bicciato S; Бионди А; te Kronnie G; Cazzaniga G (январь 2009 г.). «Интеграция данных генома и экспрессии генов ОЛЛ детского возраста без известных отклонений позволяет идентифицировать подгруппы со специфическими генетическими признаками». Гены Хромосомы Рак. 48 (1): 22–38. Дои:10.1002 / gcc.20616. PMID 18803328.
- ^ Sulong S; Мурман А.В.; Ирвинг Дж. А.; Strefford JC; Konn ZJ; Корпус MC; Minto L; Парикмахер К.Е.; Parker H; Райт С.Л.; Стюарт AR; Bailey S; Bown NP; Hall AG; Харрисон CJ (январь 2009 г.). «Комплексный анализ гена CDKN2A при остром лимфобластном лейкозе у детей выявил делецию генома, потерю гетерозиготности с нейтральным числом копий и связь с конкретными цитогенетическими подгруппами». Кровь. 113 (1): 100–7. Дои:10.1182 / кровь-2008-07-166801. PMID 18838613.
- ^ Ден Бур М.Л., ван Слегтенхорст М., Де Менезес RX и др. (Январь 2009 г.). «Подтип острого лимфобластного лейкоза у детей с плохим результатом лечения: исследование классификации всего генома». Ланцет Онкол. 10 (2): 125–34. Дои:10.1016 / S1470-2045 (08) 70339-5. ЧВК 2707020. PMID 19138562.
- ^ Хассе Д. (2008). «Цитогенетические особенности при миелодиспластических синдромах». Энн Гематол. 87 (7): 515–526. Дои:10.1007 / s00277-008-0483-y. ЧВК 2413090. PMID 18414863.
- ^ Классификация опухолей гемопоэтических и лимфоидных тканей ВОЗ, под редакцией Swerdlow SH, et al. IARC Press, 2008, Лион.
- ^ Makishima H; Ратаул М; Gondek LP; Ха Дж; Cook JR; Тейл К.С.; Секерес MA; Kuczkowski E; О'Киф С; Мацеевский JP (2010). «FISH и SNP-A кариотипирование при миелодиспластических синдромах: улучшение цитогенетического выявления del (5q), моносомии 7, del (7q), трисомии 8 и del (20q)». Leuk Res. 34 (4): 447–453. Дои:10.1016 / j.leukres.2009.08.023. ЧВК 2826525. PMID 19758696.
- ^ Санада и др. «Усиление функции мутировавшего опухолевого супрессора C-CBL в миелоидных новообразованиях». Природа 13 августа 2009 г .; 460, 904–909.
- ^ Gondek LP, Tiu R, O'Keefe CL, Sekeres MA, Theil KS, MacIejewski JP (2008). «Хромосомные поражения и однопародительская дисомия, обнаруженные с помощью массивов SNP при МДС, МДС / MPD и ОМЛ на основе МДС». Кровь. 111 (3): 1534–42. Дои:10.1182 / кровь-2007-05-092304. ЧВК 2214746. PMID 17954704.
- ^ Thoennissen NH; Круг УО; Lee DH; Kawamata N; Иванский Г.Б .; Лашо Т; Weiss T; Новак Д; Корен-Миховиц М; Като М; Sanada M; Shih LY; Наглер А; Raynaud SD; Müller-Tidow C; Mesa R; Haferlach T; Gilliland DG; Tefferi A; Огава С; Koeffler HP (апрель 2010 г.). «Распространенность и прогностическое влияние аллельных дисбалансов, связанных с лейкемической трансформацией миелопролиферативных новообразований, отрицательных по хромосоме Филадельфии». Кровь. 115 (14): 2882–2890. Дои:10.1182 / кровь-2009-07-235119. ЧВК 2854432. PMID 20068225.
- ^ а б Ленц Х. Дж., «Установленные биомаркеры колоректальной карциномы», Учебная книга Американского общества клинической онкологии, 2009 г., стр. 215-219.
- ^ а б c Джексон Э.М.; Sievert AJ; Gai X; Hakonarson H; Judkins AR; Tooke L; Perin JC; Xie H; Шейх TH; Бигель Я.А. (2009). «Геномный анализ с использованием массивов олигонуклеотидов на основе однонуклеотидного полиморфизма высокой плотности и мультиплексной лигирования-зависимой амплификации зонда обеспечивает всесторонний анализ INI1 / SMARCB1 в злокачественных рабдоидных опухолях». Clin Cancer Res. 15 (6): 1923–1930. Дои:10.1158 / 1078-0432.CCR-08-2091. ЧВК 2668138. PMID 19276269.
- ^ Прешер Г., Борнфельд Н., Хирче Н., Хорстхемке Б., Йокель К. Х., Бехер Р. (1996). «Прогностические последствия моносомии 3 в увеальной меланоме». Ланцет. 347 (9010): 1222–1225. Дои:10.1016 / S0140-6736 (96) 90736-9. PMID 8622452.
- ^ Дамато Б.Е., Допьерала Дж., Клаасен А., ван Дейк М., Сиббринг Дж., Коупленд С. (2009). «Мультиплексное усиление увеальной меланомы, зависящее от лигирования: корреляция с метастатической смертью» (PDF). Инвестируйте офтальмол Vis Sci. 50 (7): 3048–55. Дои:10.1167 / iovs.08-3165. PMID 19182252.
- ^ Белый В.А., Макнил Б.К., Хорсман Д.Е. (1998). «Приобретенная гомозиготность (изодизомия) хромосомы 3 при увеальной меланоме». Рак Genet Cytogenet. 102 (1): 40–45. Дои:10.1016 / S0165-4608 (97) 00290-2. PMID 9530338.
- ^ Онкен, доктор медицины, Уорли, Лос-Анджелес, человек E, Чарльз Д.Х., Bowcock AM, Harbour JW (2007). «Потеря гетерозиготности хромосомы 3, обнаруженная с помощью однонуклеотидных полиморфизмов, превосходит моносомию 3 для прогнозирования метастазов в увеальной меланоме». Clin Cancer Res. 13 (10): 2923–2937. Дои:10.1158 / 1078-0432.CCR-06-2383. PMID 17504992.
- ^ Yamamoto G; Няня Ы; Като М; Sanada M; Левин Р.Л .; Kawamata N; Хангаиси А; Курокава М; Chiba S; Gilliland DG; Koeffler HP; Огава С. (июль 2007 г.). «Высокочувствительный метод полногеномного определения аллельного состава в непарных образцах первичных опухолей с использованием микрочипов для генотипирования однонуклеотидного полиморфизма affymetrix». Am J Hum Genet. 81 (1): 114–26. Дои:10.1086/518809. ЧВК 1950910. PMID 17564968.


