Цинковый палец типа BTK - Btk-type zinc finger
| Btk мотив | |||||||||
|---|---|---|---|---|---|---|---|---|---|
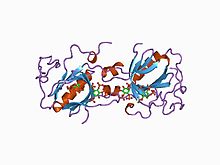 ph домен и мотив btk из мутанта тирозинкиназы Брутона e41k в комплексе с ins (1,3,4,5) p4 | |||||||||
| Идентификаторы | |||||||||
| Символ | БТК | ||||||||
| Pfam | PF00779 | ||||||||
| ИнтерПро | IPR001562 | ||||||||
| УМНАЯ | БТК | ||||||||
| SCOP2 | 1btk / Объем / СУПФАМ | ||||||||
| |||||||||
В молекулярная биология, то Цинковый палец типа BTK или мотив Btk (BM) - это консервированный цинк-связующий мотив содержащий консервированные цистеины и гистидин что присутствует в некоторых эукариотический сигнализация белки. Мотив назван в честь Тирозинкиназа Брутона (Btk), ан фермент что важно для В клетка созревание в люди и мышей.[1][2] Btk является членом семейства белков Tec. тирозинкиназы (ПТК). Эти киназы содержат консервативный домен гомологии Tec (TH) между N-концевым гомология плекстрина (PH) и домен Src гомология 3 (SH3) домен. N-конец домена TH является высококонсервативным и известен как мотив Btf, в то время как C-концевой участок домена TH содержит пролин -богатый регион (PRR). Мотив Btk содержит консервативный His и три Cys остатки которые образуют цинк Палец (хотя они отличаются от известных топологий цинковых пальцев), в то время как PRR обычно участвуют в белок-протеин взаимодействия, включая взаимодействие с G белки.[3][4] Домен TH может иметь функциональное значение в различных сигнальные пути в разных разновидность.[1] Полный TH-домен, содержащий как области Btk, так и PRR, не был обнаружен вне семейства Tec; однако мотив Btk сам по себе встречается в других белках, обычно на С-конце по отношению к домену PH (обратите внимание, что хотя мотив Btk всегда находится на C-конце домена PH, не все PH домены сопровождаются мотивом Btk).
В кристаллические структуры из Btk показывают, что цинковый палец Btk-типа имеет глобулярную сердцевину, образованную длинной петлей, которая удерживается вместе с помощью иона цинка, и что мотив Btk упакован против домена PH.[1] Цинк-связывающие остатки представляют собой гистидин и три цистеина, которые полностью консервативны в мотиве Btk.[5]
Белки Известно, что цинковые пальцы типа Btk содержат:
- Млекопитающее Тирозинкиназа Брутона (Btk), протеинтирозинкиназа, участвующая в модуляции различных сотовый процессы. Мутации влияющие на Btk, являются причиной X-связанной агаммаглобулинемии (XLA) в люди и Х-сцепленный иммунодефицит у мышей.
- Млекопитающее Tec, BMX, и Itk белки, которые являются тирозином протеинкиназы подсемейства Tec.
- Дрозофила тирозин-протеинкиназа Btk29A, необходимая для разработка правильных кольцевых каналов и мужских гениталий и необходимы для выживания взрослых.
- Белки, активирующие ГТФазу Ras млекопитающих (РасГАП ), которые регулируют активацию неактивных GDP-связанных Рас путем конвертации ВВП в GTP.
Рекомендации
- ^ а б c Вихинен М., Нильссон Л., Смит К.И. (август 1994 г.). «Гомология Tec (TH), прилегающая к домену PH». FEBS Lett. 350 (2–3): 263–5. Дои:10.1016/0014-5793(94)00783-7. PMID 8070576.
- ^ Линдвалл Дж. М., Бломберг К. Э., Валиахо Дж., Варгас Л., Хейнонен Дж. Э., Берглоф А., Мохамед А. Дж., Нор Б. Ф., Вихинен М., Смит К. И. (февраль 2005 г.). «Тирозинкиназа Брутона: клеточная биология, сохранение последовательности, спектр мутаций, модификации siRNA и профили экспрессии». Иммунол. Rev. 203: 200–15. Дои:10.1111 / j.0105-2896.2005.00225.x. PMID 15661031.
- ^ Вихинен М., Норе Б.Ф., Маттссон П.Т., Бакешо С.М., Нарс М., Коутаниеми С., Ватанабе С., Лестер Т., Джонс А., Охс HD, Смит К.И. (август 1997 г.). «Миссенс-мутации, затрагивающие консервативную пару цистеина в TH-домене Btk». FEBS Lett. 413 (2): 205–10. Дои:10.1016 / S0014-5793 (97) 00912-5. PMID 9280283.
- ^ Цзян И, Ма В., Ван И, Козаса Т., Хаттори С., Хуан Си (октябрь 1998 г.). «G-белок G alpha12 стимулирует тирозинкиназу Брутона и rasGAP через консервативный домен PH / BM». Природа. 395 (6704): 808–13. Bibcode:1998Натура.395..808J. Дои:10.1038/27454. PMID 9796816.
- ^ Хивонен М., Сарасте М. (июнь 1997 г.). «Структура домена PH и Btk мотива из тирозинкиназы Брутона: молекулярные объяснения Х-связанной агаммаглобулинемии». EMBO J. 16 (12): 3396–404. Дои:10.1093 / emboj / 16.12.3396. ЧВК 1169965. PMID 9218782.
