Вирус денге - Dengue virus
| Вирус денге | |
|---|---|
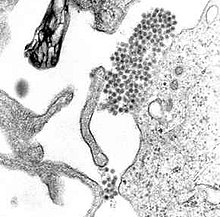 | |
| А ТЕМ микрофотография показывая вирус денге вирионы (скопление темных точек около центра) | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область: | Рибовирия |
| Королевство: | Орторнавиры |
| Тип: | Kitrinoviricota |
| Учебный класс: | Flasuviricetes |
| Заказ: | Амарилловиралес |
| Семья: | Flaviviridae |
| Род: | Флавивирус |
| Разновидность: | Вирус денге |
Вирус денге (DENV) является причиной лихорадка денге. Это комар одинарный, одноцепочечный РНК вирус семьи Flaviviridae; род Флавивирус.[1][2] Пять серотипы вируса были обнаружены,[3][4] все это может вызвать полный спектр заболеваний.[1] Тем не менее, понимание учеными вируса денге может быть упрощенным, поскольку, скорее, чем отдельные антигенные группы, континуум кажется, существует.[5] Это же исследование выявило 47 штаммов вирус денге.[6] Кроме того, коинфекция и отсутствие экспресс-тестов на вирус Зика и чикунгунья усложняют дело в реальных инфекциях.[7]
Вирус денге резко возросло за последние 20 лет, став одним из самых распространенных патогенов человека, переносимых комарами, с которыми приходится иметь дело тропическим странам. Текущие оценки показывают, что ежегодно происходит до 390 миллионов случаев инфицирования, и многие инфекции денге все чаще рассматриваются как бессимптомные или субклинические.[8]
Эволюция
На основании анализа белка оболочки не менее трех генотипы (От 1 до 3) известны. В 2013 г. четвертый серотип Сообщалось.[3] Скорость нуклеотид замещение этого вируса оценивается в 6.5×10−4 на нуклеотид в год, аналогично другим РНК-вирусам. Американско-африканский генотип, по оценкам, эволюционировал между 1907 и 1949 годами. Первая Мировая Война и Вторая Мировая Война, которые были связаны со значительным перемещением популяций и нарушением окружающей среды - факторами, которые, как известно, способствуют развитию новых трансмиссивных вирусные виды.
Байесовский анализ всех четырех серотипов показал, что их самый последний общий предок существовало около 340 г. н.э. (95% доверительный интервал: 280 г. до н.э. - 850 г. н.э.).[9]
Жизненный цикл
Еще несколько сотен лет назад вирус денге был передан в лесные циклы в Африке, Юго-Восточной Азии и Южной Азии между комарами рода Aedes и нечеловеческий приматы, с редкими случаями появления в человеческих популяциях.[10][11] Глобальное распространение вирус денгетем не менее, он возник после лесных циклов, и основной жизненный цикл теперь включает исключительно передачу между людьми и Aedes комары.[12] Вертикальная передача от комара до комара также наблюдалось у некоторых видов переносчиков.[13] Было обнаружено, что собаки инфицированы этим вирусом, но необходимы дополнительные исследования, чтобы определить, могут ли собаки или другие животные служить резервуарами или просто случайными хозяевами.[14]
Недавние результаты показывают, что по мере того, как вирус поражает клетки человека, гомеостатические процессы хозяина, такие как аутофагия и ER стресс Ответ, не говоря уже об апоптозе, запускается в зависимости от типа инфицированной клетки.[15] Активация аутофагии и стресса ER во время инфекции усиливает размножение вируса.[16][17] Попытки предоставить подробные сведения о жизненном цикле денге на клеточном уровне опубликованы в обзорных статьях различных исследовательских групп.[18][19]
Геном
ДЕНВ геном составляет около 11000 базы положительно-смысловой одноцепочечной РНК (оцРНК), которая кодирует три структурные белки (капсид протеин С, мембранный белок М, белок оболочки E) и семь неструктурные белки (NS1, NS2a, NS2b, NS3, NS4a, NS4b, NS5).[4] Он также включает короткие некодирование области на обоих концах 5 'и 3'.[1][20]
Структурные и ферментативные белки

Е протеин
Белок DENV E (оболочка), обнаруженный в виде димера на поверхности зрелой вирусной частицы, важен для начального прикрепления этой частицы к клетке-хозяину. Каждый мономер белка E включает три эктодомена, ED1-ED3, и трансмембранный сегмент. ED2 включает интерфейс димеризации, два сайта гликозилирования и пептид слияния с клеточной мембраной. ED3 представляет собой непрерывный полипептидный сегмент; его складка компактна и похожа на иммуноглобулин.[21][22] Вирус денге передается видами рода комаров Aedes. Несколько молекул, которые взаимодействуют с вирусным белком Е (неинтегрин, захватывающий ICAM3,[23] CD209,[24] Раб 5,[25] ВРП 78,[26] и рецептор маннозы[27]), как было показано, являются важными факторами, опосредующими прикрепление и проникновение вируса.[22] Мембранная форма рибосомальный белок SA также может быть задействован во вложении.[28] Рекомбинантные домены белка E используются в качестве четко определенных антигенов при серологическом обнаружении антител, направленных против вирус денге и в качестве иммуногенов в вакцинах-кандидатах.[29][30][31]
ПрМ / М белок
Белок DENV prM (мембранный), который важен для образования и созревания вирусной частицы, состоит из семи антипараллельных β-цепей, стабилизированных тремя дисульфидными связями.[22]
Гликопротеиновая оболочка зрелого вириона DENV состоит из 180 копий каждого из белков Е и М. Незрелый вирион начинается с белков E и prM, образующих 90 гетеродимеров, которые придают шипастой внешности вирусной частице. Эта незрелая вирусная частица прорастает в эндоплазматический ретикулум и в конечном итоге перемещается по секреторному пути к аппарату Гольджи. Когда вирион проходит через сеть транс-Гольджи, он подвергается воздействию низкого pH. Эта кислая среда вызывает конформационное изменение белка E, которое отделяет его от белка prM и заставляет его образовывать гомодимеры E, которые лежат на поверхности вируса, придавая созревающему вириону гладкий вид. Во время этого созревания pr пептид отщепляется от пептида M протеазой хозяина, фурин. Затем белок М действует как трансмембранный белок под оболочкой Е-белка зрелого вириона. Пептид pr остается связанным с белком E до тех пор, пока вирусная частица не высвобождается во внеклеточную среду. Этот pr-пептид действует как колпачок, покрывая петлю гидрофобного слияния белка Е, пока вирусная частица не выйдет из клетки.[22]
Белок NS3
DENV NS3 представляет собой сериновую протеазу, а также РНК-геликазу и RTPase / NTPase. Домен протеазы состоит из шести β-цепей, расположенных в два β-цилиндра, образованных остатками 1–180 белка. Каталитическая триада (His-51, Asp-75 и Ser-135) находится между этими двумя β-барабанами, и активность зависит от присутствия кофактора NS2B. Этот кофактор оборачивается вокруг домена протеазы NS3 и становится частью активного сайта. Остальные остатки NS3 (180–618) образуют три субдомена геликазы DENV. Шестицепочечный параллельный β-лист, окруженный четырьмя α-спиралями, составляет субдомены I и II, а субдомен III состоит из четырех α-спиралей, окруженных тремя более короткими α-спиралями и двумя антипараллельными β-цепями.[22]
Белок NS4A
DENV NS4A - это неструктурный белок, участвующий в изменении кривизны клеточной мембраны.[32] и индукция аутофагии.[17] В дополнение к своей способности изменять мембрану NS4A является каркасом для комплекса репликации вируса и подвергается олигомеризации.[33] Мутации NS4A, которые влияют на взаимодействие с NS4B, отменяют или сильно снижают репликацию вируса, что указывает на важность NS4A и его взаимодействия с NS4B в репродукции денге.[34] Кроме того, все NS4A четырех из пяти серотипов денге индуцируют аутофагию и защищают инфицированные клетки от токсинов через путь ATM, что свидетельствует о консервативной функции этого белка среди вирусов денге.[35]
Белок NS5
Белок DENV NS5 представляет собой пептид из 900 остатков с доменом метилтрансферазы на его N-конце (остатки 1–296) и РНК-зависимой РНК-полимеразой (RdRp) на его C-конце (остатки 320–900). Домен метилтрансферазы состоит из сэндвича α / β / β, фланкированного N- и C-концевыми субдоменами. DENV RdRp похож на другие RdRps, содержащие субдомены ладони, пальца и большого пальца, а также мотив GDD для включения нуклеотидов.[22]
Комплексы между белком Е и нейтрализующими антителами
Кристаллические структуры комплексов между антителами и эктодоменом (sE) вирусного белка E или его доменом 3 (ED3) помогли понять молекулярные основы распознавания и нейтрализации вируса. Некоторые из эпитопов частично или полностью недоступны в известной структуре зрелого вириона. Следовательно, предполагается, что соответствующие антитела связываются с альтернативными или переходными конформациями вируса при 37 ° C.
- Мышиное антитело E111 нейтрализует DENV1. Его фрагменты Fab и scFv кристаллизовались в комплексе с доменом ED3 DENV1. Его эпитоп расположен вокруг β-нитей C и C 'ED3 и промежуточной петли.[36]
- Мышиное антитело 1A1D-2 сильно нейтрализует DENV1, DENV2 и DENV3. Его Fab-фрагмент кристаллизовался в комплексе с ED3-доменом DENV2. Его эпитоп охватывает β-цепи A и G ED3.[37]
- Мышиное антитело 2H12 перекрестно реагирует со всеми четырьмя серотипами DENV. Он нейтрализует соответствующие вирусы, кроме DENV2. Его Fab-фрагмент кристаллизовался в комплексе с доменами ED3 DENV1, DENV3 и DENV4. Его эпитоп расположен вокруг консервативной петли AB ED3.[38]
- Мышиное антитело 4E11 нейтрализует все четыре серотипа DENV с различной эффективностью. Его scFv-фрагмент кристаллизовался в комплексе с доменами ED3 четырех серотипов DENV. Его эпитоп охватывает β-цепи A и G ED3, как и эпитоп 1A1D-2.[39][40] Структуры с разрешением 2,0 Å позволили проанализировать роли молекул воды в границах раздела белков и роль соматических гипермутаций вне этих интерфейсов во взаимодействиях и перекрестном распознавании.[41]
- Антитело шимпанзе 5H2 эффективно нейтрализует DENV4. Его Fab-фрагмент кристаллизовался в комплексе с sE-белком DENV4. Его эпитоп входит в домен 1 (ED1) белка E.[42]
- Человеческие антитела Ede1-C10, Ede2-A11 и Ede2-B7 эффективно нейтрализуют все четыре серотипа DENV. Их фрагменты Fab или scFv кристаллизовались в комплексе с sE-белком DENV2. Детерминанты распознавания этих антител находятся в инвариантном к серотипу сайте на границе раздела димера E и включают открытые боковые цепи слитой петли E и две консервативные боковые цепи гликана.[43]
Болезнь
Общие названия лихорадки денге включают лихорадку ломаной кости, рвоту и денди-лихорадку; геморрагическая лихорадка денге и синдром шока денге являются тяжелыми формами.[44] Денге встречается во всем мире в тропическом и субтропическом климате, в основном в городских и пригородных районах.[45] Люди всех возрастов, контактирующие с инфицированными комарами, могут стать жертвами лихорадки денге. Заболевание чаще всего возникает в сезон дождей в тропических странах Юго-Восточной Азии, Южной Азии и Южной Америки, где много инфицированных комаров.[46] Вирус передается людям через укусы инфицированных самок комаров, хотя люди не способны передавать болезнь и не заразны.[45][47][46] Инкубационный период составляет от 3 до 14 дней, а период болезни - от 3 до 7 дней.[47][48] Признаки и симптомы могут включать сильную головную боль; ретроорбитальная боль; боль в мышцах, суставах и костях; макулярная или макулопапулезная сыпь; и незначительные геморрагические проявления, включая петехии, экхимозы, пурпуру, носовое кровотечение, кровоточивость десен, гематурию или положительный результат теста на жгут.[49] Недавний систематический обзор и метаанализ показали, что аллергические симптомы являются одними из основных симптомов, которые тесно связаны с тяжестью денге.[50]
Механизм заражения
- Вирус денге'(DENV) E белок оболочки связывается с клеточным рецептором. Точная природа клеточного рецептора полностью не выяснена.
- ДЭНВ подвергается эндоцитозу. Подкисление эндосомы приводит к конформационному изменению E, обнажая последовательность слитого пептида, которая облегчает слияние оболочки с эндосомной мембраной, высвобождая капсид вириона в цитоплазму.
- В цитоплазме происходит отслоение оболочки.
- Механизм трансляции хозяина (рибосомы) переводит (+) оцРНК в единый полипептид
- Клеточные и вирусные протеиназы расщепляют полипептид на 10 белков (E, M, C и 7 неструктурных / ферментативных белков), будучи встроенными в мембрану ER.
- Как только функциональная РНК-зависимая РНК-полимераза синтезируется, может начаться репликация РНК. Синтез асимметричен, он дает в 10 раз больше положительной нити, чем отрицательной.
- Сборка происходит на внутриклеточных мембранах, которые попадают в ER (формируя оболочку из мембраны ER). Последующее отпочкование от ER через Гольджи и в пузырьки позволяет созревать посредством посттрансляционных модификаций, например гликозилирование и трансформационные перестройки pH
- Выход происходит через экзоцитоз[51]
Тяжелое заболевание
Некоторые люди страдают более тяжелыми формами денге, такими как геморрагическая лихорадка денге. Различные штаммы вирусов, взаимодействующие с людьми с разным иммунным фоном, приводят к сложному взаимодействию. Среди возможных причин - перекрестный серотипический иммунный ответ через механизм, известный как антитело-зависимое усиление, что происходит, когда человек, ранее инфицированный лихорадкой денге, заражается второй, третий или четвертый раз. Предыдущие антитела к старому штамму вирус денге теперь мешают иммунному ответу на текущий штамм, что парадоксальным образом приводит к большему проникновению и захвату вируса.[52]
Взаимодействие с иммунной системой
В последние годы многие исследования показали, что флавивирусы, особенно вирус денге, обладает способностью подавлять врожденный иммунный ответ во время инфекции.[53][54]В самом деле, вирус денге содержит много неструктурных белков, которые позволяют ингибировать различные медиаторы ответа врожденной иммунной системы. Эти белки действуют на двух уровнях:
Подавление передачи сигналов интерферона путем блокировки преобразователя сигнала
NS4B представляет собой небольшой гидрофобный белок, расположенный в эндоплазматическом ретикулуме. Он может блокировать фосфорилирование STAT 1 после индукции интерферонами типа I альфа и бета. Фактически, поскольку активность киназы Tyk2 снижается в связи с вирус денгето же самое происходит и с фосфорилированием STAT 1. [55] Кроме того, реакция врожденной иммунной системы на вирус дополнительно подавляется, поскольку экспрессия интерферон-стимулирующего гена (ов) (ISG) ограничивается вышеупомянутым белком NS4B. NS2A и NS4A кофактор также может принимать участие в ингибировании STAT 1.[56]
NS5 - присутствие этого белка массой 105 кДа приводит к инактивации STAT2 (через передачу сигнала ответа на интерферон), когда он экспрессируется отдельно.[57] Когда NS5 расщепляется NS4B протеазой (NS2B3), он может разрушать STAT2. Фактически, после расщепления NS5 протеазой происходит ассоциация лигазы E3 со STAT2, и лигаза E3 нацелена на деградацию STAT2.[58][59]
Подавление интерфероновой реакции I типа
Комплекс протеаз NS2B3-b представляет собой протеолитическое ядро, состоящее из последних 40 аминокислот NS2B и первых 180 аминокислот NS3. Расщепление предшественника NS2B3 активирует протеазный комплекс.[60]
Этот протеазный комплекс позволяет ингибировать продукцию интерферона типа I за счет снижения активности промотора IFN-бета; Комплекс протеаз NS2B3 участвует в ингибировании фосфорилирования IRF3.[61]Комплекс протеазы NS2B3 ингибирует (расщепляя) белок MITA, что делает возможной активацию IRF3.[62]
Белок слюны Mosquito D7
Вирус денге передается комарами Aedes aegypti, который производит слюну, содержащую более 100 уникальных белков, включая семейство белков D7.[63] Ученые считали, что A. aegypti слюна при передаче фактически усиливается вирус денге в организме. Считалось, что слюна комара ускоряет распространение вируса из-за ослабленного иммунного ответа его хозяина. Однако текущее исследование показало, что белок D7 препятствует передаче вируса в клетки-хозяева.[63]
Иммунные ответы антител, которые пытаются бороться с чужеродным вирусом, фактически усиливают передачу и усугубляют инфекцию. Уровни протеина D7 больше преобладают в слюнных железах комаров, инфицированных денге, по сравнению с неинфицированными.[63] D7 содержится в слюне комаров и, как считалось, помогает процессу кровоснабжения. Несмотря на предыдущие предположения, D7 может модулировать клетку-хозяин и действовать против вируса, чтобы предотвратить вирусную инфекцию.[63] К сожалению, белки D7 вызывают иммунные ответы, которые повышают уровень антител к D7. Эти антитела подавляют функцию белков D7, которые усиливают передачу вирус денге[нужна цитата ]. Хотя иммунные ответы против белков D7 могут снижать их противовирусную активность, исследование показало, что субъекты, не относящиеся к DENV, имеют несколько более высокие уровни анти-D7 IgG, чем инфицированные, хотя это не было статистически значимым.[64] Таким образом, необходимы дополнительные исследования семейства белков D7, чтобы прояснить его роль в заражении DENV и его применимость в медицине.
Исследования вакцин
Только один вакцина от денге в настоящее время одобрено в 11 странах (Мексика, Филиппины, Индонезия, Бразилия, Сальвадор, Коста-Рика, Парагвай, Гватемала, Перу, Таиланд и Сингапур).[65][66][67] Частные и государственные исследователи разрабатывают несколько вакцин.[68] Разработка вакцины против этой болезни - непростая задача. Вакцина с четырьмя различными серотипами вируса, которые могут вызывать заболевание, должна иммунизировать против всех четырех типов, чтобы быть эффективной.[3] Вакцинация только против одного серотипа может привести к тяжелому геморрагическому шоку денге при инфицировании другим серотипом из-за антителозависимого усиления. При заражении вирус денге, иммунная система вырабатывает перекрестно-реактивные антитела, которые обеспечивают иммунитет к этому конкретному серотипу. Однако эти антитела не способны нейтрализовать другие серотипы при повторном заражении и фактически увеличивают вирусная репликация. Когда макрофаги потребляют «нейтрализованный» вирус, вирус может размножаться внутри макрофага, вызывая заболевание. Эти перекрестно-реактивные, неэффективные антитела облегчают доступ вируса к макрофагам, что вызывает более тяжелое заболевание (геморрагическая лихорадка денге, синдром шока денге). Распространенная проблема, с которой сталкиваются в регионах, эндемичных по денге, - это заражение матери лихорадкой денге; после рождения потомство несут иммунитет от матери и подвержены геморрагической лихорадке, если заражены любым из трех других серотипов.[69] Одна вакцина проходила III фазу испытаний в 2012 году, и началось планирование использования вакцины и эпиднадзора за ее эффективностью.[70]
В 2009, Санофи-Пастер начал строительство нового объекта в Невиль-сюр-Сон' (fr ), пригород Лион (Франция). Это подразделение производит вакцину с четырьмя серотипами для испытаний III фазы. В сентябре 2014 г. генеральный директор Санофи-Пастер представил первые результаты исследования эффективности III фазы в Латинской Америке. Эффективность по серотипу (ST) широко варьировала: 42,3% для ST2, 50,3% для ST1, 74,0% для ST3 и 77,7% для ST4. Полный анализ данных фазы III исследования Латинской Америки и Карибского бассейна будет рассмотрен внешними экспертами перед публикацией в рецензируемом научном журнале. Первичные результаты должны быть представлены на Американское общество тропической медицины и гигиены Ежегодное собрание, проведенное 2–6 ноября 2014 г. в Новом Орлеане.[71]
В сентябре 2012 года сообщалось, что одна из вакцин не прошла клинические испытания.[3]
В конце 2015 - начале 2016 года первая вакцина против денге, Dengvaxia (CYD-TDV) от компании Sanofi-Pasteur, была зарегистрирована в нескольких странах для использования у людей в возрасте 9–45 лет, проживающих в эндемичных районах.
1 мая 2019 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США объявило об одобрении Dengvaxia, первой вакцины для предотвращения болезни денге, вызываемой всеми серотипами вируса денге, у людей в возрасте от 9 до 16 лет, у которых была лабораторно подтверждена предыдущая инфекция денге и которые живут в эндемичных районах. Денге является эндемическим заболеванием на американских территориях Американского Самоа, Гуама, Пуэрто-Рико и Виргинских островов США.[72]
Исследования наркотиков
Не существует утвержденных прямых противовирусных препаратов для лечения лихорадки денге. Большинство исследований противовирусных препаратов от инфекций денге сосредоточено на ингибировании протеазы NS2B / NS3 или белков NS5. Один препарат, Балапиравир, перепрофилированный гепатит С Ингибитор полимеразы NS5 перешел в клиническое испытание фазы II, прежде чем был остановлен из-за отсутствия эффективности.[73][74]
Рекомендации
- ^ а б c Роденхейс-Зиберт И.А., Вильшут Дж., Смит Дж. М. (август 2010 г.). «Жизненный цикл вируса денге: факторы вируса и хозяина, модулирующие инфекционность». Клеточные и молекулярные науки о жизни. 67 (16): 2773–86. Дои:10.1007 / s00018-010-0357-z. PMID 20372965. S2CID 4232236.
- ^ ВОЗ (2009 г.). Рекомендации по диагностике, лечению, профилактике и борьбе с денге (PDF). Всемирная организация здоровья. ISBN 978-92-4-154787-1.
- ^ а б c d Нормиль Д. (октябрь 2013 г.). «Тропическая медицина. Неожиданный новый вирус денге бросает вызов усилиям по борьбе с болезнями». Наука. 342 (6157): 415. Bibcode:2013Наука ... 342..415N. Дои:10.1126 / science.342.6157.415. PMID 24159024.
- ^ а б Двиведи В. Д., Трипати И. П., Трипати Р. К., Бхарадвадж С. и Мишра С. К. (2017). Геномика, протеомика и эволюция Вирус денге. Брифинги по функциональной геномике. 16 (4): 217–227, https://doi.org/10.1093/bfgp/elw040
- ^ "Новое понимание Вирус денге". ScienceDaily. 18 сентября 2015 г.. Получено 7 мая, 2016.
- ^ «Вторая инфекция денге может быть опасной для жизни, - говорят исследования». NDTV. Объединенное Королевство. 18 сентября 2015 г.. Получено 2016-05-07.
- ^ Vogels CB, Rückert C, Cavany SM, Perkins TA, Ebel GD, Grubaugh ND (январь 2019 г.). «Коинфекция и совместная передача арбовирусов: игнорируемая проблема общественного здравоохранения?». PLOS Биология. 17 (1): e3000130. Дои:10.1371 / journal.pbio.3000130. ЧВК 6358106. PMID 30668574.
- ^ Бхатт С., Гетинг П.У., Брэди О.Дж., Мессина Дж. П., Фарлоу А. В., Мойес С. Л., Дрейк Дж. М., Браунштейн Дж. С., Хоен А. Г., Санко О., Майерс М. Ф., Джордж Д. Б., Джениш Т., Винт Г. Р., Симмонс С. П., Скотт Т. В., Фаррар Дж. , Хэй С.И. (апрель 2013 г.). «Глобальное распространение и бремя денге». Природа. 496 (7446): 504–7. Bibcode:2013Натура.496..504Б. Дои:10.1038 / природа12060. ЧВК 3651993. PMID 23563266.
- ^ Коста Р.Л., Волоч С.М., Шраго К.Г. (2012) Сравнительная эволюционная эпидемиология серотипов вируса денге. Заразить Genet Evol 12 (2): 309-314
- ^ «Вирус денге». Информация о патогенах (PathInfo). Институт биоинформатики Вирджинии, Технологический институт Вирджинии. Архивировано из оригинал на 30.08.2010.
- ^ Холмс ЕС, Твидди СС (май 2003 г.). «Происхождение, возникновение и эволюционная генетика вируса денге». Инфекция, генетика и эволюция. 3 (1): 19–28. Дои:10.1016 / с 1567-1348 (03) 00004-2. PMID 12797969.
- ^ Холстед С.Б. (январь 1988 г.). «Патогенез денге: вызовы молекулярной биологии». Наука. 239 (4839): 476–81. Bibcode:1988Научный ... 239..476H. Дои:10.1126 / science.3277268. PMID 3277268.
- ^ Хаддов А.Д., Гусман Х., Попов В.Л., Вуд Т.Г., Уайден С.Г., Хаддов А.Д., Теш РБ, Уивер СК (июнь 2013 г.). «Первая изоляция флавивируса Aedes в Западном полушарии и свидетельство вертикальной передачи у комара Aedes (Stegomyia) albopictus (Diptera: Culicidae)». Вирусология. 440 (2): 134–9. Дои:10.1016 / j.virol.2012.12.008. PMID 23582303.
- ^ Thongyuan S, Kittayapong P (30 августа 2017 г.). «Первые свидетельства инфекции денге у домашних собак, живущих в различных экологических условиях Таиланда». PLOS ONE. 12 (8): e0180013. Bibcode:2017PLoSO..1280013T. Дои:10.1371 / journal.pone.0180013. ЧВК 5576688. PMID 28854207.
- ^ Гош Рой С., Садиг Б., Датан Е., Локшин Р.А., Закери З. (май 2014 г.). «Регулирование выживаемости и гибели клеток при флавивирусных инфекциях». Всемирный журнал биологической химии. 5 (2): 93–105. Дои:10.4331 / wjbc.v5.i2.93 (неактивно 01.09.2020). ЧВК 4050121. PMID 24921001.CS1 maint: DOI неактивен по состоянию на сентябрь 2020 г. (связь)
- ^ Датан Э., Рой С.Г., Жермен Дж., Зали Н., Маклин Дж. Э., Голшан Г., Харбаджан С., Локшин Р.А., Закери З. (март 2016 г.). «Вызванная денге аутофагия, репликация вируса и защита от гибели клеток требуют активации пути ER-стресса (PERK)». Смерть и болезнь клеток. 7 (e2127): e2127. Дои:10.1038 / cddis.2015.409. ЧВК 4823927. PMID 26938301.
- ^ а б McLean JE, Wudzinska A, Datan E, Quaglino D, Zakeri Z (июнь 2011 г.). «Аутофагия, индуцированная флавивирусом NS4A, защищает клетки от гибели и усиливает репликацию вируса». Журнал биологической химии. 286 (25): 22147–59. Дои:10.1074 / jbc.M110.192500. ЧВК 3121359. PMID 21511946.
- ^ Закери З., Гош-Рой С., Датан Э., Маклин Дж. Э., Занди К., Жермен Дж. (2015). «Гибель клеток и вирусное заражение - краткий обзор». 20 лет смерти клетки. 1 (1): 292–325. Дои:10.13140 / RG.2.2.35359.97447.
- ^ Neufeldt CJ, Cortese M, Acosta EG, Bartenschlager R (февраль 2018 г.). «Переналадка сотовых сетей членами семейства Flaviviridae». Обзоры природы. Микробиология. 16 (3): 125–142. Дои:10.1038 / nrmicro.2017.170. ЧВК 7097628. PMID 29430005.
- ^ Хэнли К.А., Weaver SC, ред. (2010). Границы исследования вируса денге. Caister Academic. п. 13. ISBN 978-1-904455-50-9. Получено 22 сентября 2020.
- ^ Модис Й., Огата С., Клементс Д., Харрисон С.К. (июнь 2003 г.). «Лиганд-связывающий карман в гликопротеине оболочки вируса денге». Труды Национальной академии наук Соединенных Штатов Америки. 100 (12): 6986–91. Bibcode:2003ПНАС..100.6986М. Дои:10.1073 / pnas.0832193100. ЧВК 165817. PMID 12759475.
- ^ а б c d е ж Перера Р., Кун Р. Дж. (Август 2008 г.). «Структурная протеомика вируса денге». Текущее мнение в микробиологии. 11 (4): 369–77. Дои:10.1016 / j.mib.2008.06.004. ЧВК 2581888. PMID 18644250.
- ^ Tassaneetrithep B, Burgess TH, Granelli-Piperno A, Trumpfheller C, Finke J, Sun W, Eller MA, Pattanapanyasat K, Sarasombath S, Birx DL, Steinman RM, Schlesinger S, Marovich MA (апрель 2003 г.). «DC-SIGN (CD209) опосредует инфицирование дендритных клеток человека вирусом денге». Журнал экспериментальной медицины. 197 (7): 823–9. Дои:10.1084 / jem.20021840. ЧВК 2193896. PMID 12682107.
- ^ Кришнан М.Н., Сукумаран Б., Пал У, Агаэсс Х., Мюррей Д.Л., Ходж Т.В., Фикриг Э. (май 2007 г.). «Rab 5 необходим для проникновения в клетки вирусов денге и Западного Нила». Журнал вирусологии. 81 (9): 4881–5. Дои:10.1128 / JVI.02210-06. ЧВК 1900185. PMID 17301152.
- ^ Jindadamrongwech S, Thepparit C, Smith DR (май 2004 г.). «Идентификация GRP 78 (BiP) как рецепторного элемента, экспрессируемого клетками печени для серотипа 2 вируса денге». Архив вирусологии. 149 (5): 915–27. Дои:10.1007 / s00705-003-0263-х. PMID 15098107. S2CID 12062084.
- ^ Миллер Дж. Л., Де Вет Би Джей, Де Вет Би Джей, Мартинес-Помарес Л., Рэдклифф К. М., Двек Р. А., Радд П. М., Гордон С. (февраль 2008 г.). «Рецептор маннозы опосредует инфицирование макрофагов вирусом денге». PLOS Патогены. 4 (2): e17. Дои:10.1371 / journal.ppat.0040017. ЧВК 2233670. PMID 18266465.
- ^ Зидан Н., Ульд-Абей М.Б., Петит-Топен I, Бедуель Н. (декабрь 2012 г.). «Сложенные и неупорядоченные домены человеческого рибосомного белка SA имеют как идиосинкразические, так и общие функции в качестве мембранных рецепторов». Отчеты по бионауке. 33 (1): 113–24. Дои:10.1042 / BSR20120103. ЧВК 4098866. PMID 23137297.
- ^ Зидан Н., Дюссар П., Бреманд Л., Бедуель Н. (июль 2013 г.). «Перекрестная реактивность между человеческими IgM и четырьмя серотипами вируса денге при исследовании с помощью искусственных гомодимеров домена III из белков оболочки». BMC Инфекционные болезни. 13: 302. Дои:10.1186/1471-2334-13-302. ЧВК 3701519. PMID 23815496.
- ^ Зидан Н., Дуссар П., Бреманд Л., Виллани М.Э., Бедуэль Г. (июнь 2013 г.). «Термодинамическая стабильность домена III из белка оболочки флавивирусов и ее улучшение молекулярным дизайном». Белковая инженерия, дизайн и выбор. 26 (6): 389–99. Дои:10.1093 / белок / gzt010. PMID 23479674.
- ^ Brandler S, Ruffie C, Najburg V, Frenkiel MP, Bedouelle H, Desprès P, Tangy F (сентябрь 2010 г.). «Детская вакцина против кори, экспрессирующая четырехвалентный антиген денге, вырабатывает нейтрализующие антитела против всех четырех вирусов денге». Вакцина. 28 (41): 6730–9. Дои:10.1016 / j.vaccine.2010.07.073. PMID 20688034.
- ^ Миллер С., Кастнер С., Крайнсе-Локер Дж., Бюлер С., Бартеншлагер Р. (март 2007 г.). «Неструктурный белок 4A вируса денге представляет собой интегральный мембранный белок, вызывающий мембранные изменения регулируемым 2K способом». Журнал биологической химии. 282 (12): 8873–82. Дои:10.1074 / jbc.M609919200. PMID 17276984. S2CID 19927382.
- ^ Ли СМ, Се Икс, Цзоу Дж., Ли Ш., Ли М.Й., Донг Х., Цинь С.Ф., Кан Си, Ши Пай (июнь 2015 г.). «Детерминанты олигомеризации белка NS4A вируса денге». Журнал вирусологии. 89 (12): 6171–83. Дои:10.1128 / JVI.00546-15. ЧВК 4474302. PMID 25833044.
- ^ Цзоу Дж, Се Х, Ван Цюй, Донг Х, Ли М.Ю., Кан Ц., Юань З., Ши ПЙ (апрель 2015 г.). «Характеристика взаимодействия белков NS4A и NS4B вируса денге». Журнал вирусологии. 89 (7): 3455–70. Дои:10.1128 / JVI.03453-14. ЧВК 4403404. PMID 25568208.
- ^ Зали Н., Рой С.Г., Датан Е., Маклин Дж., Альварес Л., Локшин Р.А., Закери З. (октябрь 2018 г.). «Белки NS4A из 4 серотипов лихорадки денге, существенно различающиеся по последовательности, функции аналогичны индукции аутофагии и защите клеток млекопитающих с использованием путей ATM». Журнал новых болезней и вирусологии. 4 (2): 1–7. Дои:10.16966/2473-1846.144.
- ^ Остин С.К., Дауд К.А., Шреста Б., Нельсон КА, Эделинг М.А., Джонсон С., Пирсон Т.С., Даймонд М.С., Фремонт Д.Х. (2012). «Структурные основы дифференциальной нейтрализации генотипов DENV-1 антителом, распознающим криптический эпитоп». PLOS Патогены. 8 (10): e1002930. Дои:10.1371 / journal.ppat.1002930. ЧВК 3464233. PMID 23055922.
- ^ Лок С.М., Костюченко В., Нюбаккен Г.Е., Холдэуэй Х.А., Баттисти А.Дж., Сукуполви-Петти С., Седлак Д., Фремонт Д.Х., Чипман П.Р., Рериг Дж. Т., Даймонд МС, Кун Р. Дж., Россманн М. Г. (март 2008 г.). «Связывание нейтрализующего антитела с вирусом денге изменяет расположение поверхностных гликопротеинов». Структурная и молекулярная биология природы. 15 (3): 312–7. Дои:10.1038 / nsmb.1382. PMID 18264114. S2CID 64886.
- ^ Midgley CM, Flanagan A, Tran HB, Dejnirattisai W., Chawansuntati K, Jumnainsong A, Wongwiwat W., Duangchinda T., Mongkolsapaya J, Grimes JM, Screaton GR (май 2012 г.). «Структурный анализ перекрестно-реактивного антитела денге в комплексе с доменом оболочки III показывает молекулярную основу перекрестной реактивности». Журнал иммунологии. 188 (10): 4971–9. Дои:10.4049 / jimmunol.1200227. ЧВК 3364712. PMID 22491255.
- ^ Лисова О., Харди Ф, Пети В, Бедуель Х (сентябрь 2007 г.). «Картирование полноты и трансплантация группоспецифичного прерывистого нейтрализующего эпитопа в белке оболочки вируса денге». Журнал общей вирусологии. 88 (Pt 9): 2387–97. Дои:10.1099 / vir.0.83028-0. PMID 17698647.
- ^ Кокберн Дж. Дж., Наварро Санчес М. Э., Фретес Н., Урвоас А., Старополи И., Кикути С. М., Коффи Л. Л., Арензана Сейсдедос Ф., Бедуэль Н., Рей Ф. А. (февраль 2012 г.). «Механизм широкой перекрестной нейтрализации вируса денге моноклональным антителом». Структура. 20 (2): 303–14. Дои:10.1016 / j.str.2012.01.001. PMID 22285214.
- ^ Лисова О., Белкади Л., Бедуель Х (апрель 2014 г.). «Прямые и непрямые взаимодействия в распознавании перекрестно нейтрализующих антител и четырех серотипов вируса денге». Журнал молекулярного распознавания. 27 (4): 205–14. Дои:10.1002 / jmr.2352. PMID 24591178.
- ^ Кокберн Дж. Дж., Наварро Санчес М. Э., Гонсалвез А. П., Зайцева Е., Стура Е. А., Кикути С. М., Дукеррой С., Дуссарт П., Черномордик Л. В., Лай С. Дж., Рей Ф. А. (февраль 2012 г.). «Структурное понимание механизма нейтрализации высших антител приматов против вируса денге». Журнал EMBO. 31 (3): 767–79. Дои:10.1038 / emboj.2011.439. ЧВК 3273384. PMID 22139356.
- ^ Rouvinski A, Guardado-Calvo P, Barba-Spaeth G, Duquerroy S, Vaney MC, Kikuti CM, Navarro Sanchez ME, Dejnirattisai W, Wongwiwat W, Haouz A, Girard-Blanc C, Petres S, Shepard WE, Desprès P, Arenzana -Seisdedos F, Dussart P, Mongkolsapaya J, Screaton GR, Rey FA (апрель 2015 г.). «Детерминанты распознавания широко нейтрализующих человеческих антител против вирусов денге» (PDF). Природа. 520 (7545): 109–13. Bibcode:2015Натура.520..109р. Дои:10.1038 / природа14130. HDL:10044/1/34173. PMID 25581790. S2CID 4394235.
- ^ Виатрек, Мелисса. Лихорадка денге. http://www.austincc.edu/microbio/2993p/df.htm В архиве 2018-07-26 в Wayback Machine
- ^ а б Всемирная организация здоровья. Денге и тяжелая денге. Апрель 2017 г. http://www.who.int/mediacentre/factsheets/fs117/en/
- ^ а б РАЙОН КОЛУМБИИ ДЕПАРТАМЕНТ ЗДРАВООХРАНЕНИЯ. Информационный бюллетень о лихорадке денге. https://doh.dc.gov/sites/default/files/dc/sites/doh/publication/attachments/Dengue_Fever.pdf
- ^ а б Лучшее здоровье. Болезнь, вызванная вирусом денге. https://www.betterhealth.vic.gov.au/health/conditionsandtreatments/Dengue-virus-disease?viewAsPdf=true
- ^ Центры по контролю и профилактике заболеваний. Эпидемиология. https://www.cdc.gov/dengue/epidemiology/
- ^ Центры по контролю и профилактике заболеваний. Денге. https://wwwnc.cdc.gov/travel/yellowbook/2016/infectious-diseases-related-to-travel/dengue
- ^ Кин Н.Д., Эль-Кушайри А.Э., Ахмед А.М., Сафи А., Магид С.А., Мехьяр С.М. и др. (Февраль 2020 г.). «Связь аллергических симптомов с инфекцией денге и тяжестью: систематический обзор и метаанализ». Virologica Sinica. 35 (1): 83–92. Дои:10.1007 / s12250-019-00165-6. ЧВК 7035405. PMID 31637633.
- ^ Ачесон, Николас Х. (2011). Основы молекулярной вирусологии, 2-е изд.. Вайли.
- ^ Деджнираттисай В., Джумнайнсонг А., Онсирисакул Н., Фиттон П., Васанаватана С., Лимпитикул В., Путтихунт С., Эдвардс С., Дуангчинда Т., Супаса С., Чавансунтати К., Маласит П., Монгколсапая Д., Скреатон Г. (май 2010 г.) «Перекрестно реагирующие антитела усиливают инфицирование людей вирусом денге». Наука. 328 (5979): 745–8. Bibcode:2010Sci ... 328..745D. Дои:10.1126 / science.1185181. ЧВК 3837288. PMID 20448183.
- ^ Diamond MS (сентябрь 2009 г.). «Механизмы уклонения флавивирусов от противовирусного ответа интерферона I типа». Журнал исследований интерферона и цитокинов. 29 (9): 521–30. Дои:10.1089 / июл.2009.0069. PMID 19694536.
- ^ Джонс М., Дэвидсон А., Хибберт Л., Грюнвальд П., Шлаак Дж., Болл С., Фостер Г. Р., Джейкобс М. (май 2005 г.). «Вирус денге подавляет передачу сигналов альфа-интерферона за счет снижения экспрессии STAT2». Журнал вирусологии. 79 (9): 5414–20. Дои:10.1128 / JVI.79.9.5414-5420.2005. ЧВК 1082737. PMID 15827155.
- ^ Хо Л.Дж., Хунг Л.Ф., Вен CY, Ву В.Л., Чоу П, Лин Ю.Л., Чанг Д.М., Тай Т.Ю., Лай Дж.Х. (июнь 2005 г.). «Вирус денге типа 2 противодействует противовирусному действию IFN-альфа, но не IFN-гамма, посредством подавления передачи сигналов Tyk2-STAT в дендритных клетках человека». Журнал иммунологии. 174 (12): 8163–72. Дои:10.4049 / jimmunol.174.12.8163. PMID 15944325. S2CID 83577905.
- ^ Муньос-Джордан Дж. Л., Санчес-Бургос Г. Г., Лоран-Ролле М., Гарсия-Састре А. (ноябрь 2003 г.). «Ингибирование передачи сигналов интерферона вирусом денге». Труды Национальной академии наук Соединенных Штатов Америки. 100 (24): 14333–8. Bibcode:2003ПНАС..10014333М. Дои:10.1073 / пнас.2335168100. ЧВК 283592. PMID 14612562.
- ^ Ашур Дж., Лоран-Ролль М, Ши П.Й., Гарсия-Састре А (июнь 2009 г.). «NS5 вируса денге опосредует связывание и деградацию STAT2». Журнал вирусологии. 83 (11): 5408–18. Дои:10.1128 / JVI.02188-08. ЧВК 2681973. PMID 19279106.
- ^ Маззон М, Джонс М, Дэвидсон А, Цепь Б, Джейкобс М (октябрь 2009 г.). «NS5 вируса денге ингибирует передачу сигналов интерферона-альфа, блокируя преобразователь сигнала и активатор фосфорилирования транскрипции 2». Журнал инфекционных болезней. 200 (8): 1261–70. Дои:10.1086/605847. PMID 19754307.
- ^ Моррисон Дж., Агирре С., Фернандес-Сесма А. (март 2012 г.). "Врожденное уклонение от иммунитета вирусом денге". Вирусы. 4 (3): 397–413. Дои:10.3390 / v4030397. ЧВК 3347034. PMID 22590678.
- ^ Юсоф Р., Клам С., Ветцель М., Мурти Х. М., Падманабхан Р. (апрель 2000 г.). «Очищенная сериновая протеаза NS2B / NS3 вируса денге типа 2 проявляет зависимость от кофактора NS2B при расщеплении субстратов двухосновными аминокислотами in vitro». Журнал биологической химии. 275 (14): 9963–9. Дои:10.1074 / jbc.275.14.9963. PMID 10744671. S2CID 30345627.
- ^ Родригес-Мадос-младший, Белича-Вильянуэва А., Бернал-Рубио Д., Ашур Дж., Эйллон Дж., Фернандес-Сесма А. (октябрь 2010 г.). «Ингибирование ответа интерферона типа I в дендритных клетках человека инфекцией вируса денге требует каталитически активного комплекса NS2B3». Журнал вирусологии. 84 (19): 9760–74. Дои:10.1128 / JVI.01051-10. ЧВК 2937777. PMID 20660196.
- ^ Ю CY, Чанг TH, Liang JJ, Chiang RL, Lee YL, Liao CL, Lin YL (июнь 2012 г.). Diamond MS (ред.). «Вирус денге нацелен на адаптерный белок MITA, чтобы подорвать врожденный иммунитет хозяина». PLOS Патогены. 8 (6): e1002780. Дои:10.1371 / journal.ppat.1002780. ЧВК 3386177. PMID 22761576.
- ^ а б c d Конвей MJ, Londono-Renteria B, Troupin A, Watson AM, Klimstra WB, Fikrig E, Colpitts TM (сентябрь 2016 г.). «Белок слюны Aedes aegypti D7 ингибирует инфекцию, вызванную вирусом денге». PLOS забытые тропические болезни. 10 (9): e0004941. Дои:10.1371 / journal.pntd.0004941. ЧВК 5025043. PMID 27632170.
- ^ Londono-Renteria BL, Shakeri H, Rozo-Lopez P, Conway MJ, Duggan N, Jaberi-Douraki M, Colpitts TM (2018). «Белки слюны Aedes aegypti D7 в Колумбии». Границы общественного здравоохранения. 6: 111. Дои:10.3389 / fpubh.2018.00111. ЧВК 5968123. PMID 29868532.
- ^ «Вакцина Санофи против денге одобрена в 11 странах». Рейтер. 2016. Получено 13 августа 2017.
- ^ Восток, Сьюзи (6 апреля 2016 г.). «Первая в мире вакцина против лихорадки денге запущена на Филиппинах». CNN. Получено 17 октября 2016.
- ^ «Вакцина против лихорадки денге доступна в Индонезии». 17 октября 2016 г.
- ^ Разработка вакцины В архиве 2019-08-21 в Wayback Machine, Dengue Vaccine Initiative, ноябрь 2012 г., по состоянию на 5 ноября 2013 г.
- ^ Шмальджон А.Л., Макклейн Д. (1996). "Глава 54: Альфавирусы (Togaviridae) и флавивирусы (Flaviviridae)". В Бароне S (ред.). Медицинская микробиология (4-е изд.). Медицинский филиал Техасского университета в Галвестоне. ISBN 978-0-9631172-1-2. NBK7633.
- ^ Торрези Дж., Тапиа-Коньер Р., Марголис Х. (2013). «Подготовка к внедрению вакцины против денге: рекомендации 1-го Международного совещания против денге v2V». PLOS забытые тропические болезни. 7 (9): e2261. Дои:10.1371 / journal.pntd.0002261. ЧВК 3784468. PMID 24086776.
- ^ «Санофи Пастер, второе испытание вакцины против денге, вторая фаза III». Основные новости GEN. Новости генной инженерии и биотехнологии. 3 сентября 2014 г.
- ^ Первая вакцина, одобренная FDA для профилактики лихорадки денге в эндемичных регионах https://www.fda.gov/news-events/press-announcements/first-fda-approved-vaccine-prevention-dengue-disease-endemic-regions
- ^ Nguyen NM, Tran CN, Phung LK, Duong KT, Huynh HA, Farrar J и др. (Май 2013). «Рандомизированное двойное слепое плацебо-контролируемое исследование балапиравира, ингибитора полимеразы, у взрослых пациентов с лихорадкой денге». Журнал инфекционных болезней. 207 (9): 1442–50. Дои:10.1093 / infdis / jis470. ЧВК 3610419. PMID 22807519.
- ^ Чен Ю.Л., Абдул Гафар Н., Каруна Р., Фу Й., Лим С.П., Шул В. и др. (Февраль 2014). «Активация мононуклеарных клеток периферической крови инфекцией вируса денге депотенцирует балапиравир». Журнал вирусологии. 88 (3): 1740–7. Дои:10.1128 / JVI.02841-13. ЧВК 3911617. PMID 24257621.
внешняя ссылка
| Scholia имеет тема профиль для Вирус денге. |
- Структуры вируса денге для трехмерной электронной микроскопии из банка данных EM (EMDB)
- «Бразилия выпускает« хороших »комаров для борьбы с лихорадкой денге». BBC News Латинская Америка и Карибский бассейн. 24 сентября 2014 г.
