Димер (химия) - Dimer (chemistry)
Эта статья нужны дополнительные цитаты для проверка. (Апрель 2009 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |

А димер (/ˈdаɪмər/) (ди-, "два" + -мер, "части") является олигомер состоящий из двух мономеры связаны узами, которые могут быть сильными или слабыми, ковалентный или же межмолекулярный. Период, термин гомодимер используется, когда две молекулы идентичны (например, A – A) и гетеродимер когда это не так (например, A – B). Обратную димеризацию часто называют диссоциация. Когда два противоположно заряженных иона объединяются в димеры, их называют Пары Бьеррума.[1]
Нековалентные димеры
Карбоновые кислоты образуют димеры за счет водородной связи кислого водорода и карбонильного кислорода, когда безводный. Например, уксусная кислота образует димер в газовой фазе, где мономерные звенья удерживаются вместе за счет водородные связи. В особых условиях большинство ОН-содержащих молекул образуют димеры, например в димер воды.
Боран ("BH3") происходит как димер диборан (B2ЧАС6), из-за высокого Кислотность Льюиса из бор центр.
Эксимеры и эксиплексы находятся в восторге конструкции с коротким сроком службы. Например, благородные газы не образуют стабильных димеров, но они (димеры) образуют эксимеры Ar2*, Kr2* и Xe2* под высоким давлением и электростимуляцией.
Ковалентные димеры

Молекулярный димеры часто образуются в результате реакции двух идентичных соединений, например: 2A → A-A. В этом примере мономер Говорят, что "A" димеризуется с образованием димера "A-A". Примером является диаминокарбен, димеризу тетрааминоэтилен:
- 2 С (NR2)2 → (R2N)2C = C (NR2)2
Карбены обладают высокой реакционной способностью и легко образуют связи.
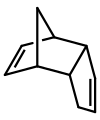
Дициклопентадиен представляет собой асимметричный димер двух циклопентадиен молекулы, которые прореагировали в Реакция Дильса-Альдера отдать продукт. При нагревании он "трескается" (подвергается ретро-реакции Дильса-Альдера) с образованием идентичных мономеров:
- C10ЧАС12 → 2 С5ЧАС6
Многие неметаллические элементы встречаются в виде димеров: водород, азот, кислород, то галогены, т.е. фтор, хлор, бром и йод. Благородные газы могут образовывать димеры, связанные между собой облигации Ван-дер-Ваальса, Например дигелий или же диаргон. Меркурий встречается в виде катиона ртути (I) (Hg22+), формально димерный ион. Другие металлы могут образовывать часть димеров в своих парах. Известные металлические димеры включают Ли2, Na2, K2, Руб.2 и CS2.
Многие небольшие органические молекулы, особенно формальдегид, легко образуют димеры. Димер формальдегида (CH2O) есть диоксетан (C2ЧАС4О2).
Полимерная химия
В контексте полимеры, «димер» также относится к степень полимеризации 2, независимо от стехиометрии или реакции конденсации.
Это применимо к дисахариды. Например, целлобиоза димер глюкоза, даже если реакция образования производит воды:
- 2C6ЧАС12О6 → С12ЧАС22О11 + H2О
Здесь димер имеет стехиометрию, отличную от пары мономеров.
Аминокислоты также могут образовывать димеры, которые называются дипептиды. Примером является глицилглицин, состоящий из двух глицин молекулы соединены пептидная связь. Другие примеры: аспартам и карнозин.
Биохимические димеры
Димеры пиримидина сформированы фотохимическая реакция из пиримидина Основания ДНК. Это перекрестное связывание вызывает Мутации ДНК, который может быть канцерогенный, вызывая рак кожи.
Смотрите также
Рекомендации
- "Определение" Золотой книги ИЮПАК ". Получено 2009-04-30.
- ^ Adar, Ram M .; Маркович, Томер; Андельман, Дэвид (2017-05-17). «Пары Бьеррума в ионных растворах: подход Пуассона-Больцмана». Журнал химической физики. 146 (19): 194904. arXiv:1702.04853. Bibcode:2017ЖЧФ.146с4904А. Дои:10.1063/1.4982885. ISSN 0021-9606. PMID 28527430.
