Дуокармицин - Duocarmycin - Wikipedia
В дуокармицины являются членами ряда связанных натуральные продукты впервые изолирован от Streptomyces бактерии в 1978 году.[1][2][3] Они отличаются крайней цитотоксичностью и, таким образом, представляют собой класс исключительно мощных противоопухолевых антибиотиков.[4][5]
Биологическая активность
В качестве низкомолекулярных синтетических алкилирующих агентов, связывающих малые бороздки ДНК, дуокармицины подходят для воздействия на солидные опухоли. Они привязаны к малая бороздка ДНК и алкилировать азотистое основание аденин на позиции N3.[6][7] Необратимое алкилирование ДНК нарушает архитектуру нуклеиновых кислот, что в конечном итоге приводит к гибели опухолевых клеток. Аналоги встречающихся в природе противоопухолевых средств, таких как дуокармицины, представляют новый класс высокоэффективных противоопухолевых соединений.[8][9]
Работа Дейл Л. Богер и другие создали лучшее понимание фармакофор и механизм действия дуокармицинов. Это исследование привело к синтетическим аналогам, включая адозелезин, бизелезин, и карзелезин которые перешли в клинические испытания для лечения рака. Аналогичное исследование, которое Богер использовал для сравнения с его результатами, касающимися устранения раковых опухолей и антигенов, было сосредоточено на использовании аналогичных иммуноконъюгатов, которые были введены в раковые клетки толстой кишки. Эти исследования связаны с исследованиями Богера, касающимися антиген-специфичности, которая необходима для успеха дуокармицинов в качестве противоопухолевого лечения.[10]
Аналоги дуокармицина против тубулинсвязывающих средств
Дуокармицин продемонстрировал активность в различных моделях с множественной лекарственной устойчивостью (МЛУ). Агенты, которые являются частью этого класса дуокармицинов, обладают эффективностью в низком пикомолярном диапазоне. Это делает их подходящими для максимального увеличения эффективности уничтожения клеток конъюгатов антитело-лекарственное средство, к которым они присоединены.[11]
Дуокармицины

Дуокармицин А
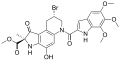
Дуокармицин B1
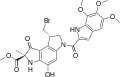
Дуокармицин В2
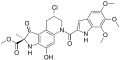
Дуокармицин С1
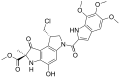
Дуокармицин C2

Дуокармицин D

Дуокармицин SA

CC-1065
Конъюгаты антитело-лекарственное средство
Агенты, модифицирующие ДНК, такие как дуокармицин, используются при разработке конъюгат антитело-лекарственное средство или АЦП. Ученые из нидерландской Synthon (ранее Syntarga) объединили уникальные линкеры с производными дуокармицина, которые имеют гидроксильную группу, которая имеет решающее значение для биологическая активность. Используя эту технологию, ученые стремятся создать ADC с оптимальным терапевтическим окном, уравновешивая действие сильнодействующих агентов, убивающих клетки, на опухолевые клетки по сравнению со здоровыми клетками.[12]
Синтетические аналоги
К синтетическим аналогам дуокармицинов относятся: адозелезин, бизелезин, и карзелезин. Как члены семейства циклопропилпирролоиндолов, эти исследуемые препараты прошли клинические испытания для лечения рака.
Бизелезин

Бизелезин представляет собой противоопухолевый антибиотик, который связывается с малой бороздой ДНК и вызывает межцепочечное сшивание ДНК, тем самым ингибируя репликацию ДНК и синтез РНК. Бизелезин также усиливает индукцию p53 и p21 и запускает остановку клеточного цикла G2 / M, что приводит к старению клеток без апоптоза.[13]


Рекомендации
- ^ Ясудзава, Тору; Иида, Такао; Мурои, Кен'Ичи; Ичимура, Мичио; Такахаши, Кейчи; Сано, Хироши (1988). «Структуры дуокармицинов, новых противоопухолевых антибиотиков, производимых Streptomyces sp». Химико-фармацевтический бюллетень. 36 (9): 3728–31. Дои:10.1248 / cpb.36.3728.
- ^ Такахаши, Исами; Такахаши, Кей-Ичи; Ичимура, Мичио; Моримото, Макото; Асано, Козо; Кавамото, Исао; Томита, Фусао; Накано, Хирофуми (1988). «Дуокармицин А, новый противоопухолевый антибиотик от Streptomyces». Журнал антибиотиков. 41 (12): 1915–7. Дои:10.7164 / антибиотики. 41.1915. PMID 3209484.
- ^ «Цитотоксические агенты». Обзор ADC / Журнал конъюгатов антитело-лекарственное средство. 29 октября 2013 г.
- ^ Богер, Дейл Л. (1991). «Дуокармицины: новый класс селективных по последовательности алкилирующих агентов малых бороздок ДНК». Chemtracts: органическая химия. 4 (5): 329–49.
- ^ Терсель, Моана; McManaway, Сара П .; Люнг, Юфимия; Лиянаге, Х. Д. Сарат; Лу, Го-Лян; Пруйн, Фредерик Б. (2013). «Цитотоксичность аналогов дуокармицина опосредована алкилированием ДНК, а не альдегиддегидрогеназой 1: комментарий». Angewandte Chemie International Edition. 52 (21): 5442–6. Дои:10.1002 / anie.201208373. PMID 23616474.
- ^ Богер, Д. Л. (1993). «Дизайн, синтез и оценка агентов, связывающих малые бороздки ДНК». Чистая и прикладная химия. 65 (6): 1123–32. Дои:10.1351 / pac199365061123.
- ^ Boger, Dale L .; Джонсон, Дуглас С. (1995). "CC-1065 и дуокармицины: разгадывая ключи к новому классу природных алкилирующих агентов ДНК". Труды Национальной академии наук Соединенных Штатов Америки. 92 (9): 3642–9. Bibcode:1995PNAS ... 92.3642B. Дои:10.1073 / пнас.92.9.3642. ЧВК 42018. PMID 7731958.
- ^ Tietze, Lutz F .; Кревер, Биргит (2009). «Антитело-направленная ферментная пролекарственная терапия: многообещающий подход к селективному лечению рака на основе пролекарств и моноклональных антител». Химическая биология и дизайн лекарств. 74 (3): 205–11. Дои:10.1111 / j.1747-0285.2009.00856.x.
- ^ Каччари, Барбара; Романьоли, Ромео; Баральди, Пьер Джованни; Рось, Татьяна Да; Спаллуто, Джампьеро (2000). «CC-1065 и дуокармицины: последние разработки». Экспертное заключение о терапевтических патентах. 10 (12): 1853–71. Дои:10.1517/13543776.10.12.1853.
- ^ Лю, К; Тадайони, Б. М.; Бурре, Л. А; Mattocks, KM; Derr, S M; Уиддисон, Вашингтон; Кедерша, Н Л; Ариниелло, П. Д.; Гольдмахер, В. С. (1996-08-06). «Ликвидация ксенотрансплантатов больших опухолей толстой кишки путем адресной доставки майтанзиноидов». Труды Национальной академии наук Соединенных Штатов Америки. 93 (16): 8618–8623. Bibcode:1996PNAS ... 93.8618L. Дои:10.1073 / пнас.93.16.8618. ISSN 0027-8424. ЧВК 38722. PMID 8710920.
- ^ «Аналоги дуокармицина». Обзор ADC / Журнал конъюгатов антитело-лекарственное средство. 26 ноября 2014 г. Архивировано с оригинал 26 ноября 2014 г.
- ^ Хофланд, Питер. «Первое испытание SYD985 на людях по оценке безопасности и эффективности у онкологических больных». ADCReview / Журнал конъюгатов антитело-лекарственное средство (Ноябрь 2014 г.).
- ^ "Бизелезин". MedKoo Biosciences.








