Конъюгат антитело-лекарственное средство - Antibody-drug conjugate
Конъюгаты антитело-лекарственное средство или же АЦП являются классом биофармацевтический препараты, разработанные как таргетная терапия для лечения рака.[1] В отличие от химиотерапия, ADC предназначены для нацеливания и уничтожения опухолевых клеток, сохраняя при этом здоровые клетки. По состоянию на 2019 год около 56 фармацевтических компаний разрабатывали ADC.[2]
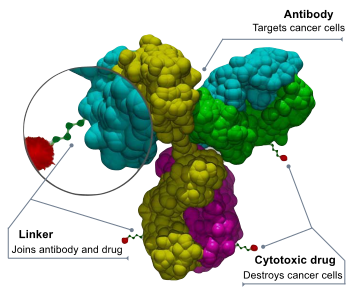
ADC - это сложные молекулы, состоящие из антитело связан с биологически активным цитотоксический (противоопухолевой) полезной нагрузки или лекарственного средства.[3] Конъюгаты антитело-лекарственное средство являются примерами биоконъюгаты и иммуноконъюгаты.
ADC сочетают в себе возможности нацеливания моноклональные антитела с противораковой способностью цитотоксических препаратов. Они могут быть предназначены для различения здоровой и больной ткани.[4][5]
Механизм действия
Противоопухолевое лекарство связано с антителом, которое нацелено на определенную опухоль. антиген (например, белок которые в идеале должны быть обнаружены только в опухолевых клетках или на них). Антитела прикрепляются к антигенам на поверхности раковых клеток. Биохимическая реакция между антителом и целевым белком (антигеном) запускает сигнал в опухолевой клетке, которая затем поглощает или интернализует антитело вместе со связанным цитотоксином. После интернализации ADC цитотоксин убивает рак.[6] Такая ориентация ограничивает побочные эффекты и дает более широкий терапевтическое окно чем другие химиотерапевтические средства.
Технологии ADC были представлены во многих публикациях,[7][8] в том числе научные журналы.
История
Лекарства, которые воздействуют на опухолевые клетки и игнорируют другие, были изобретены в 1900 году немецким нобелевским лауреатом. Пол Эрлих.[2]
В 2001 Pfizer /Wyeth наркотик Гемтузумаб озогамицин (торговое название: Mylotarg) был одобрен. Однако по запросу из США Управление по контролю за продуктами и лекарствами (FDA), компания отозвала его в июне 2010 года.[9] Он был повторно представлен на рынке США в 2017 году.[10]
Брентуксимаб ведотин (торговое название: Adcetris, продается компаниями Seattle Genetics и Millennium / Takeda)[11] был одобрен FDA 19 августа 2011 г. для лечения рецидива HL и sALCL и получил условное разрешение на продажу от Европейское агентство по лекарствам в октябре 2012 г.
Трастузумаб эмтанзин (адо-трастузумаб эмтанзин или T-DM1, торговое название: Kadcyla, продается Genentech и Roche) был одобрен в феврале 2013 года для лечения людей с HER2-положительный метастатический рак груди (mBC), ранее получавший лечение трастузумабом и таксан химиотерапия.[12][13]
В Европейская комиссия одобренный Инотузумаб озогамицин[14] в качестве монотерапии для лечения взрослых с рецидивирующим или рефрактерным CD22-положительным предшественником B-клеток острый лимфобластный лейкоз (ALL) 30 июня 2017 г. под торговым наименованием Besponsa® (Pfizer / Wyeth),[15] а затем 17 августа 2017 г. - FDA.[16]
Первый иммунология Конъюгат антитело-лекарственное средство (iADC), ABBV-3373, проходит клинические испытания для участников с умеренной и тяжелой ревматоидный артрит.[17]
В июле 2018 года Daiichi Sankyo Company, Limited и Glycotope GmbH подписали договор о комбинации исследуемого опухолево-ассоциированного антитела TA-MUC1 гатипотузумаба компании Glycotope и патентованной технологии ADC Daiichi Sankyo для разработки конъюгата лекарственного средства антитела гатипотузумаба.[18]
В 2019 г. АстраЗенека согласился заплатить до 6,9 млрд долларов США на совместную разработку DS-8201 с японской Дайичи Санкё. Он предназначен для замены Герцептина при лечении рака груди. DS8201 несет восемь полезных нагрузок по сравнению с обычными четырьмя.[2]
Коммерческие продукты
Девять ADC получили одобрение рынка - все для онкотерапия.
| Препарат, средство, медикамент | Производитель | Условие | Торговое наименование | |
|---|---|---|---|---|
| Гемтузумаб озогамицин | Pfizer /Wyeth | рецидив острый миелолейкоз (AML) | Mylotarg | |
| Брентуксимаб ведотин | Сиэтл Генетикс, Миллениум / Такеда | рецидив HL и рецидив sALCL | Адцетрис | |
| Трастузумаб эмтанзин | Genentech, Рош | HER2-положительный метастатический рак молочной железы (mBC) после лечения трастузумабом и майтансиноид | Кадсила | |
| Инотузумаб озогамицин | Pfizer /Wyeth | рецидивирующий или рефрактерный CD22-положительный предшественник B-клеток острый лимфобластный лейкоз | Беспона | |
| Полатузумаб ведотин-пиик | Genentech, Рош | рецидивирующий или рефрактерный (R / R) диффузная В-клеточная лимфома большого размера (DLBCL)[19] | Polivy | |
| Энфортумаб ведотин | Астеллас /Сиэтл Генетикс | взрослые пациенты с местнораспространенным или метастатическим уротелиальным раком, которые получали ингибитор PD-1 или PD-L1 и Pt-содержащую терапию[20] | Падцев | |
| Трастузумаб друкстекан | АстраЗенека /Дайичи Санкё | взрослые пациенты с неоперабельным или метастатическим HER2-положительным раком молочной железы, которые ранее получали две или более схемы лечения на основе анти-HER2[21] | Энхерту | |
| Сацитузумаб говитекан | Иммуномедика | взрослые пациенты с метастатическим тройным отрицательным раком молочной железы (mTNBC), которые получали как минимум два предшествующих курса лечения пациентов с рецидивирующим или рефрактерным метастатическим заболеванием[22] | Тродельвы | |
| Белантамаб мафодотин | GlaxoSmithKline | пациенты с множественной миеломой, заболевание которых прогрессировало, несмотря на предшествующее лечение иммуномодулирующим агентом, ингибитором протеасом и антителом к CD38[23] | Бленреп |
Линкеры
Стабильная связь между антителом и цитотоксическим (противораковым) агентом является важным аспектом ADC.[24] Стабильный линкер ADC гарантирует, что меньшая часть цитотоксической полезной нагрузки упадет до достижения опухолевой клетки, повышая безопасность и ограничивая дозировки.
Линкеры основаны на химических мотивах, включая дисульфиды, гидразоны или же пептиды (расщепляемый), или тиоэфиры (нерасщепляемый). В доклинических и клинических испытаниях было доказано, что расщепляемые и нерасщепляемые линкеры безопасны. Брентуксимаб ведотин содержит чувствительный к ферментам расщепляемый линкер который доставляет антимикротрубочковый агент монометил ауристатин E или MMAE, синтетический противоопухолевый агент, по отношению к человеческим CD30-положительным злокачественным клеткам. MMAE подавляет деление клеток, блокируя полимеризацию тубулина. Из-за высокой токсичности MMAE нельзя использовать в качестве химиотерапевтического препарата с одним агентом. Однако MMAE, связанный с моноклональным антителом к CD30 (cAC10, белок клеточной мембраны фактор некроза опухоли или рецептор TNF) был стабильным во внеклеточной жидкости. Он расщепляется катепсин и безопасен для терапии. Трастузумаб эмтанзин представляет собой комбинацию ингибитора образования микротрубочек мертанзин (DM-1) и антитело трастузумаб, которое содержит стабильный, нерасщепляемый линкер.
Доступность более качественных и стабильных линкеров изменила функцию химической связи. Тип линкера, расщепляемый или же нерасщепляемый, придает цитотоксическому препарату специфические свойства. Например, нерасщепляемый линкер удерживает лекарство внутри клетки. В результате все антитело, линкер и цитотоксический (противораковый) агент попадают в раковую клетку-мишень, где антитело разлагается до аминокислоты. Полученный комплекс - аминокислота, линкер и цитотоксический агент - считается активным лекарственным средством. В отличие, расщепляемые линкеры отделяются ферментами в раковой клетке. Затем цитотоксическая полезная нагрузка может покинуть целевую клетку и, в процессе, называемом «убийство свидетелей», атаковать соседние клетки.[25]
Другой тип расщепляемого линкера, который в настоящее время находится в разработке, добавляет дополнительную молекулу между цитотоксином и сайтом расщепления. Это позволяет исследователям создавать ADC с большей гибкостью без изменения кинетики расщепления. Исследователи разрабатывают новый метод расщепления пептидов на основе Эдман деградация, метод секвенирования аминокислот в пептиде.[26] Также в стадии разработки находятся сайт-специфическая конъюгация (TDC).[27] и новые техники спряжения[28][29] для дальнейшего улучшения стабильности и терапевтического индекса, альфа-излучающие иммуноконъюгаты,[30] наночастицы, конъюгированные с антителами[31] и конъюгаты антитело-олигонуклеотид.[32]
Исследование
Неприродные аминокислоты
Первое поколение использует технологии связывания, которые неизбирательно связывают лекарства с цистеин или же лизин остатки в антителе, в результате чего получается гетерогенная смесь. Такой подход приводит к неоптимальной безопасности и эффективности и затрудняет оптимизацию биологических, физических и фармакологических свойств.[27] Сайт-специфическое включение неприродных аминокислот создает сайт для контролируемого и стабильного прикрепления. Это позволяет производить гомогенные ADC с антителом, точно связанным с лекарством, и контролировать соотношение антитела к лекарству, что позволяет выбрать лучший в своем классе ADC.[27] An кишечная палочка -основан открытый бесклеточный синтез (OCFS) позволяет синтезировать белки, содержащие сайт-специфически включенные неприродные аминокислоты, и был оптимизирован для предсказуемого синтеза и фолдинга белков с высоким выходом. Отсутствие клеточной стенки позволяет добавлять в систему неприродные факторы для управления транскрипцией, трансляцией и фолдингом, чтобы обеспечить точную модуляцию экспрессии белка.[33]
Другие области заболеваний
Большинство ADC разрабатываются или проходят клинические испытания для онкологических и гематологических показаний.[34] Это в первую очередь обусловлено наличием моноклональных антител, нацеленных на различные типы рака. Однако некоторые разработчики стремятся расширить приложение для других важных областей болезни.[35][36]
Смотрите также
Рекомендации
- ^ Гамильтон GS (сентябрь 2015 г.). «Конъюгаты антитело-лекарственное средство для лечения рака: технологические и нормативные проблемы разработки лекарственно-биологических гибридов». Биологические препараты. 43 (5): 318–32. Дои:10.1016 / j.biologicals.2015.05.006. PMID 26115630.
- ^ а б c Мацуяма К. (11.06.2019). «Препарат, заменяющий химиотерапию, может изменить лечение рака». BNN Bloomberg. Получено 2019-06-14.
- ^ Фитцпатрик-Даймонд П.Ф. (9 марта 2010 г.). "Конъюгаты антитело-лекарственное средство возвращают в игру". GEN: Новости генной инженерии и биотехнологии.
- ^ ДиДжозеф Дж. Ф., Армеллино Д. К., Богарт Э. Р., Хандке К., Дугер М. М., Шридхаран Л. и др. (Март 2004 г.). «Направленная на антитела химиотерапия с CMC-544: нацеленный на CD22 иммуноконъюгат калихеамицина для лечения B-лимфоидных злокачественных новообразований». Кровь. 103 (5): 1807–14. Дои:10.1182 / кровь-2003-07-2466. PMID 14615373. S2CID 17543492.
- ^ Маллард А. (май 2013 г.). «Созревание конвейера конъюгата антитело-лекарственное средство достигает 30». Обзоры природы. Открытие наркотиков. 12 (5): 329–32. Дои:10.1038 / nrd4009. PMID 23629491. S2CID 28757488.
- ^ Чари Р.В., Мартелл Б.А., Гросс Дж.Л., Кук С.Б., Шах С.А., Блаттлер В.А. и др. (Январь 1992 г.). «Иммуноконъюгаты, содержащие новые майтанзиноиды: перспективные противоопухолевые препараты». Исследования рака. 52 (1): 127–31. PMID 1727373.
- ^ Поллак А (31 мая 2012 г.). "Один-два удара". Нью-Йорк Таймс.
- ^ «Перенос лекарства в раковую клетку». Нью-Йорк Таймс. 3 июня 2012 г.
- ^ «FDA: Pfizer добровольно снимает с рынка США препарат Mylotarg для лечения рака». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Архивировано из оригинал 18 января 2017 г.
- ^ «Одобренные препараты> FDA одобряет гемтузумаб озогамицин для лечения CD33-положительного ОМЛ». fda.gov. Сильвер-Спринг, США: Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 1 сентября 2017 г.. Получено 6 сентября 2017.
- ^ «Брентуксимаб ведотин (SGN35)]». Обзор ADC / Журнал конъюгатов антитело-лекарственное средство.
- ^ «FDA одобрило Genentech's Kadcyla® (адо-трастузумаб эмтанзин), первый конъюгат антитело-лекарственное средство для лечения Her2-положительного метастатического рака молочной железы». Genentech.
- ^ «Адо-трастузумаб эмтанзин». Министерство здравоохранения и социальных служб США, Национальные институты здравоохранения, Национальный институт рака.
- ^ «Инотузумаб озогамицин (описание препарата)». Обзор ADC / Журнал конъюгатов антитело-лекарственное средство.
- ^ «BESPONSA® одобрен в ЕС для взрослых пациентов с рецидивирующим или рефрактерным предшественником B-клеток, острым лимфобластным лейкозом».
- ^ «FDA США одобряет инотузумаб озогамицин для лечения пациентов с острым лимфобластным лейкозом, предшественником R / R B-клеток». Обзор ADC / Журнал конъюгатов антитело-лекарство. 17 августа 2017 года.
- ^ Номер клинического исследования NCT03823391 для «Исследования по оценке безопасности, переносимости, фармакокинетики и эффективности ABBV-3373 у пациентов с умеренным и тяжелым ревматоидным артритом» при ClinicalTrials.gov
- ^ "Размер рынка конъюгатов антител и лекарств, доля, тенденции, отчет об анализе роста, прикладная иммунотерапия, бизнес-возможности, прогноз будущих тенденций - 2023 г. |". 24 сентября 2019.
- ^ Комиссар, Офис (2019-06-10). «FDA одобряет первый режим химиоиммунотерапии для пациентов с рецидивирующей или рефрактерной диффузной крупноклеточной В-клеточной лимфомой». FDA. Получено 2019-06-14.
- ^ «FDA ускоряет одобрение энфортумаба ведотин-ejfv для лечения метастатического уротелиального рака». FDA. 2019-12-18. Получено 2020-01-03.
- ^ «FDA одобряет новый вариант лечения для пациентов с HER2-положительным раком молочной железы, которые достигли прогресса на доступных методах лечения». FDA. 2019-12-20. Получено 2020-01-03.
- ^ «FDA одобряет новую терапию для лечения тройного отрицательного рака груди, который распространился, но не поддается лечению». FDA. 2020-04-22. Получено 2020-04-24.
- ^ «FDA предоставило ускоренное разрешение на применение белантамаба мафодотин-blmf для лечения множественной миеломы». FDA. 2020-08-06. Получено 2020-08-06.
- ^ Бек А., Гётч Л., Дюмонте С., Корвайя Н. (май 2017 г.). «Стратегии и проблемы для следующего поколения конъюгатов антитело-лекарственное средство». Обзоры природы. Открытие наркотиков. 16 (5): 315–337. Дои:10.1038 / nrd.2016.268. PMID 28303026. S2CID 22045270.
- ^ Ковтун Ю.В., Гольдмахер В.С. (октябрь 2007 г.). «Уничтожение клеток конъюгатами антитело-лекарственное средство». Письма о раке. 255 (2): 232–40. Дои:10.1016 / j.canlet.2007.04.010. PMID 17553616.
- ^ Bąchor R, Kluczyk A, Stefanowicz P, Szewczuk Z (август 2013). «Новый метод расщепления пептидов, основанный на деградации Эдмана». Молекулярное разнообразие. 17 (3): 605–11. Дои:10.1007 / s11030-013-9453-у. ЧВК 3713267. PMID 23690169.
- ^ а б c Axup JY, Bajjuri KM, Ritland M, Hutchins BM, Kim CH, Kazane SA, et al. (Октябрь 2012 г.). «Синтез сайт-специфических конъюгатов антитело-лекарственное средство с использованием неприродных аминокислот». Труды Национальной академии наук Соединенных Штатов Америки. 109 (40): 16101–6. Bibcode:2012PNAS..10916101A. Дои:10.1073 / pnas.1211023109. ЧВК 3479532. PMID 22988081.
- ^ Лион Р.П., Сеттер-младший, Бови Т.Д., Доронина С.О., Хантер Дж. Х., Андерсон М.Э. и др. (Октябрь 2014 г.). «Самогидролизующиеся малеимиды улучшают стабильность и фармакологические свойства конъюгатов антитело-лекарственное средство». Природа Биотехнологии. 32 (10): 1059–62. Дои:10.1038 / nbt.2968. PMID 25194818. S2CID 5415162.
- ^ Колодыч С., Кониев О., Баатархуу З., Боннефой Ю.Ю., Дебаене Ф., Чианферани С. и др. (Февраль 2015 г.). «CBTF: новый реагент сочетания амина и тиола для приготовления конъюгатов антител с повышенной стабильностью в плазме». Биоконъюгат химия. 26 (2): 197–200. Дои:10.1021 / bc500610g. PMID 25614935.
- ^ Wulbrand C, Seidl C, Gaertner FC, Bruchertseifer F, Morgenstern A, Essler M, Senekowitsch-Schmidtke R (2013). Multhoff G (ред.). «Испускающие альфа-частицы иммуноконъюгаты 213Bi-анти-EGFR уничтожают опухолевые клетки независимо от оксигенации». PLOS ONE. 8 (5): e64730. Bibcode:2013PLoSO ... 864730 Вт. Дои:10.1371 / journal.pone.0064730. ЧВК 3665541. PMID 23724085.
- ^ Кардосо М.М., Печа И.Н., Роке А.С. (2012). «Наночастицы, конъюгированные с антителами, для терапевтического применения». Современная лекарственная химия. 19 (19): 3103–27. Дои:10.2174/092986712800784667. HDL:10362/20689. PMID 22612698. S2CID 38141058.
- ^ Довгань И., Кониев О., Колодыч С., Вагнер А. (октябрь 2019). «Конъюгаты антитело-олигонуклеотид в качестве терапевтических средств, средств визуализации и обнаружения». Биоконъюгат химия. 30 (10): 2483–2501. Дои:10.1021 / acs.bioconjchem.9b00306. PMID 31339691.
- ^ Завада Дж. Ф., Инь Дж., Штайнер А. Р., Ян Дж., Нареш А., Рой С. М. и др. (Июль 2011 г.). «Микромасштаб для увеличения производства бесклеточных цитокинов - новый подход к сокращению сроков разработки производства белка». Биотехнологии и биоинженерия. 108 (7): 1570–8. Дои:10.1002 / бит. 23103. ЧВК 3128707. PMID 21337337.
- ^ Flygare JA, Pillow TH, Aristoff P (январь 2013 г.). «Конъюгаты антитело-лекарственное средство для лечения рака». Химическая биология и дизайн лекарств. 81 (1): 113–21. Дои:10.1111 / cbdd.12085. PMID 23253133. S2CID 20523083.
- ^ Легар С.М., Подушка Т, Сюй М., Стабен Л., Кадихара К.К., Вандлен Р. и др. (Ноябрь 2015 г.). «Новый конъюгат антитело-антибиотик устраняет внутриклеточный S. aureus». Природа. 527 (7578): 323–8. Bibcode:2015Натура. 527..323л. Дои:10.1038 / природа16057. PMID 26536114. S2CID 205246581.
- ^ «Ambrx сотрудничает с Merck в разработке и разработке конъюгатов биологических лекарственных средств». Архивировано из оригинал (Пресс-релиз) на 2013-01-07.
