Антиген - Antigen
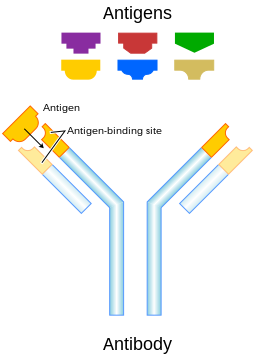
В иммунология, антиген (Ag) это молекула или молекулярный структура, например, которые могут присутствовать на внешней стороне возбудитель, которые могут быть связаны антигенспецифическим антитело или же Рецептор антигена В-клеток.[1] Присутствие антигенов в организме обычно вызывает иммунная реакция.[2] Аббревиатура Ag означает генератор антител.[3]
Антигены "нацелены" на антитела.[1] Каждое антитело специально вырабатывается иммунной системой, чтобы соответствовать антигену после клетки в иммунной системе с ним контактируют; это позволяет точно идентифицировать или сопоставить антиген и инициировать адаптивный ответ.[1][2] Говорят, что антитело «соответствует» антигену в том смысле, что оно может связываться с ним за счет приспособление в антигенсвязывающий фрагмент антитела.[1] В большинстве случаев адаптированное антитело может реагировать и связываться только с одним специфическим антигеном; однако в некоторых случаях антитела могут перекрестная реакция и связывают более одного антигена.
Антигены белки, пептиды (аминокислотные цепи) и полисахариды (цепочки моносахаридов / простых сахаров), но липиды а нуклеиновые кислоты становятся антигенами только в сочетании с белками и полисахаридами.[4]
Антиген может происходить изнутри тела («собственный антиген») или из внешней среды («чужой»).[2] Иммунная система идентифицирует и атакует «чужие» внешние антигены и обычно не реагирует на аутоантигены из-за отрицательный выбор из Т-клетки в вилочковая железа.[5]
Вакцина являются примерами антигенов в иммуногенной форме, которые преднамеренно вводятся реципиенту, чтобы вызвать функцию памяти адаптивная иммунная система к антигенам патогена, вторгающимся в этого реципиента, с вирус сезонного гриппа как типичный пример.[6]
Этимология
Пол Эрлих ввел термин антитело (на немецком Antikörper) в его теория боковой цепи в конце 19 века.[7] В 1899 г. Ладислас Дойч (Ласло Детре) (1874–1939) назвал гипотетические вещества, находящиеся на полпути между бактериальными составляющими и антителами, «веществами иммуногенами или антигенами» (антигенными или иммуногенными веществами). Первоначально он считал, что эти вещества являются предшественниками антител, так же как зимоген является предшественником фермента. Но к 1903 году он понял, что антиген индуцирует выработку иммунных тел (антител), и написал, что слово антиген сокращение антисоматогена (Immunkörperbildner). В Оксфордский словарь английского языка указывает, что логическая конструкция должна быть «анти (тело) -ген».[8]
Терминология
- Эпитоп - Отличительные особенности поверхности антигена, его антигенная детерминанта. Антигенные молекулы, обычно «большие» биологические полимеры, обычно имеют поверхностные элементы, которые могут действовать как точки взаимодействия для конкретных антител. Любая такая особенность составляет эпитоп. Большинство антигенов могут связываться с множеством антител, каждое из которых специфично к одному из эпитопов антигена. Используя метафору «замок и ключ», антиген можно рассматривать как цепочку ключей (эпитопов), каждый из которых соответствует другому замку (антителу). Другое антитело идиотипы, каждый отчетливо сформировал регионы, определяющие комплементарность.
- Аллерген - Вещество, способное вызывать аллергическая реакция. (Пагубная) реакция может возникнуть в результате воздействия при проглатывании, вдыхании, инъекции или контакте с кожей.
- Суперантиген - Класс антигенов, которые вызывают неспецифическую активацию Т-клеток, что приводит к активации поликлональных Т-клеток и массивному цитокин релиз.
- Tolerogen - Вещество, которое вызывает специфическую иммунную нечувствительность из-за своего молекулярная форма. Если его молекулярная форма изменится, толероген может стать иммуноген.
- Иммуноглобулин -связывающий белок - Белки, такие как белок А, белок G, и белок L которые способны связываться с антителами в положениях за пределами антигенсвязывающего сайта. В то время как антигены являются «мишенью» антител, иммуноглобулин-связывающие белки «атакуют» антитела.
- Т-зависимый антиген - Антигены, которым требуется помощь Т-клеток для индукции образования специфических антител.
- Т-независимый антиген - Антигены, которые напрямую стимулируют В-клетки.
- Иммунодоминантные антигены - Антигены, которые доминируют (над всеми другими из возбудитель ) в их способности вызывать иммунный ответ. Т-клеточные ответы обычно направлены против относительно небольшого числа иммунодоминантных эпитопов, хотя в некоторых случаях (например, инфицирование малярия возбудитель Plasmodium spp. ) он рассредоточен по относительно большому количеству паразитарных антигенов.[9]
Антигенпрезентирующие клетки представляют антигены в виде пептидов на молекулы гистосовместимости. Т-лимфоциты избирательно распознают антигены; В зависимости от антигена и типа молекулы гистосовместимости будут активироваться разные типы Т-клеток. Для распознавания Т-клеточного рецептора (TCR) пептид должен быть обработан в небольшие фрагменты внутри клетки и представлен главный комплекс гистосовместимости (MHC).[10] Антиген не может вызвать иммунный ответ без помощи иммунологический адъювант.[4] Точно так же адъювантный компонент вакцин играет важную роль в активации врожденной иммунной системы.[11][12]
Иммуноген - это антигенное вещество (или аддукт ), который способен вызывать гуморальный (врожденный) или клеточно-опосредованный иммунный ответ.[13] Сначала он запускает врожденный иммунный ответ, который затем вызывает активацию адаптивного иммунного ответа. Антиген связывает продукты иммунорецептора с высокой степенью вариабельности (рецептор В-клеток или рецептор Т-клеток), как только они образовались. Иммуногены - это те антигены, которые называются иммуногенный, способный вызывать иммунный ответ.[14]
На молекулярном уровне антиген можно охарактеризовать его способностью связываться с антителами. вариабельная область Fab. Различные антитела могут различать определенные эпитопы, присутствующие на поверхности антигена. А гаптен представляет собой небольшую молекулу, изменяющую структуру антигенного эпитопа. Чтобы вызвать иммунный ответ, он должен быть прикреплен к большой молекуле-носителю, такой как белок (комплекс пептидов). Антигены обычно переносятся белки и полисахариды, и реже, липиды. Сюда входят части (оболочки, капсулы, клеточные стенки, жгутики, фимбрии и токсины) бактерии, вирусы, и другие микроорганизмы. Липиды и нуклеиновые кислоты являются антигенными только в сочетании с белками и полисахаридами.[нужна цитата ] Немикробные несамоантигены могут включать пыльцу, яичный белок и белки из трансплантированных тканей и органов или на поверхности перелитых клеток крови.
Источники
Антигены можно классифицировать по их источнику.
Экзогенные антигены
Экзогенные антигены - это антигены, попавшие в организм извне, например, путем вдыхание, проглатывание или же инъекция. Ответ иммунной системы на экзогенные антигены часто бывает субклиническим. К эндоцитоз или же фагоцитоз экзогенные антигены попадают в антигенпрезентирующие клетки (APC) и переработаны в фрагменты. Затем БТР представляют фрагменты Т-хелперные клетки (CD4+) с помощью гистосовместимость класса II молекулы на их поверхности. Некоторые Т-клетки специфичны для комплекса пептид: MHC. Они активируются и начинают секретировать цитокины, вещества, которые активируют цитотоксические Т-лимфоциты (CTL), секретирующие антитела В-клетки, макрофаги и другие частицы.
Некоторые антигены начинаются как экзогенные, а затем становятся эндогенными (например, внутриклеточные вирусы). Внутриклеточные антигены могут быть возвращены в кровоток после разрушения инфицированной клетки.
Эндогенные антигены
Эндогенные антигены генерируются в нормальных клетках в результате нормальных клеток. метаболизм, или из-за вирусного или внутриклеточного бактериального инфекционное заболевание. Затем фрагменты представлены на поверхности клетки в комплексе с MHC класс I молекулы. Если активировано цитотоксический CD8+ Т-клетки узнают их, Т-клетки секретируют различные токсины что вызывает лизис или же апоптоз инфицированной клетки. Чтобы цитотоксические клетки не убивали клетки только для представления собственных белков, цитотоксические клетки (самореактивные Т-клетки) удаляются в результате толерантность (отрицательный выбор). К эндогенным антигенам относятся: ксеногенный (гетерологичный), аутологичный и идиотипический или же аллогенный (гомологичные) антигены. Иногда антигены часть самого хоста в аутоиммунное заболевание.[2]
Аутоантигены
An аутоантиген обычно представляет собой нормальный белок или белковый комплекс (а иногда и ДНК или РНК), который распознается иммунной системой пациентов, страдающих определенным аутоиммунное заболевание. В нормальных условиях эти антигены не должны быть мишенью иммунной системы, но при аутоиммунных заболеваниях связанные с ними Т-клетки не удаляются, а вместо этого атакуют.
Неоантигены
Неоантигены - это те, которые полностью отсутствуют в нормальном геноме человека. По сравнению с немутантными аутоантигенами, неоантигены важны для контроля над опухолью, так как качество пула Т-клеток, доступного для этих антигенов, не зависит от толерантности центральных Т-клеток. Технология для систематического анализа реактивности Т-клеток против неоантигенов стала доступна только недавно.[15] Неоантигены могут быть непосредственно обнаружены и количественно определены с помощью метода под названием MANA-SRM, разработанного компанией молекулярной диагностики Complete Omics Inc., в сотрудничестве с командой Медицинской школы Университета Джона Хопкинса. [16]
Вирусные антигены
Для опухолей, связанных с вирусами, таких как рак шейки матки и подмножество рак головы и шеи, эпитопы полученные из открытых рамок считывания вирусов, вносят свой вклад в пул неоантигенов.[15]
Опухолевые антигены
Опухолевые антигены те антигены, которые представлены MHC класс I или же MHC класс II молекулы на поверхности опухолевые клетки. Антигены, обнаруженные только на таких клетках, называются опухолеспецифические антигены (TSA) и обычно возникают в результате опухолево-специфической мутация. Чаще встречаются антигены, представленные опухолевыми и нормальными клетками, называемые опухоль-ассоциированные антигены (TAA). Цитотоксические Т-лимфоциты которые распознают эти антигены, могут разрушать опухолевые клетки.[15]
Опухолевые антигены могут появляться на поверхности опухоли, например, в форме мутировавшего рецептора, и в этом случае они распознаются В-клетки.[15]
Новинка для опухолей человека без вирусной этиологии. пептиды (неоэпитопы) создаются опухолеспецифическими изменениями ДНК.[15]
Процесс
Большая часть мутаций опухолей человека зависит от конкретного пациента. Следовательно, неоантигены также могут быть основаны на геномах отдельных опухолей. Технологии глубокого секвенирования могут идентифицировать мутации в кодирующей белок части геном (в экзом ) и прогнозировать потенциальные неоантигены. В моделях на мышах для всех новых белковых последовательностей были предсказаны потенциальные пептиды, связывающиеся с MHC. Полученный набор потенциальных неоантигенов использовали для оценки реактивности Т-клеток. Анализы на основе экзома использовались в клинических условиях для оценки реактивности у пациентов, получавших либо лимфоцит, инфильтрирующий опухоль (TIL) клеточная терапия или блокада контрольных точек. Идентификация неоантигенов была успешной для множества экспериментальных модельных систем и злокачественных опухолей человека.[15]
Уровень ложноотрицательных результатов при секвенировании экзома рака низок, т. Е. Большинство неоантигенов встречается в экзонной последовательности с достаточным охватом. Однако подавляющее большинство мутаций в экспрессируемых генах не продуцируют неоантигены, которые распознаются аутологичными Т-клетками.[15]
По состоянию на 2015 г. разрешение масс-спектрометрии недостаточно, чтобы исключить множество ложноположительных результатов из пула пептидов, которые могут быть представлены молекулами MHC. Вместо этого используются алгоритмы для определения наиболее вероятных кандидатов. Эти алгоритмы учитывают такие факторы, как вероятность протеасомный обработка, транспортировка в эндоплазматический ретикулум, сродство к соответствующему MHC класса I аллели и уровни экспрессии генов или трансляции белков.[15]
Большинство человеческих неоантигенов, идентифицированных на объективных экранах, демонстрируют высокую предсказуемую аффинность связывания MHC. Незначительные антигены гистосовместимости, концептуально подобный класс антигенов также правильно идентифицируются с помощью алгоритмов связывания MHC. Другой потенциальный фильтр проверяет, улучшит ли мутация связывание MHC. Природа центральных TCR-экспонированных остатков MHC-связанных пептидов связана с иммуногенностью пептида.[15]
Рождество
Нативный антиген - это антиген, который еще не процессируется APC на более мелкие части. Т-клетки не могут связывать нативные антигены, но требуют, чтобы они обрабатывались APC, тогда как В-клетки можно активировать родными.
Антигенная специфичность
Антигенная специфичность - это способность клеток-хозяев специфически распознавать антиген как уникальное молекулярное образование и отличать его от другого с исключительной точностью. Специфичность антигена обусловлена прежде всего конформациями боковых цепей антигена. Он поддается измерению и не обязательно должен быть линейным, ступенчатым или уравнением с ограничением скорости.[2][6] Обе Т-клетки и В-клетки являются клеточными компонентами адаптивный иммунитет.[2][17]
Смотрите также
Рекомендации
- ^ а б c d «Антитело». Национальный институт исследования генома человека, Национальные институты здравоохранения США. 2020 г.. Получено 13 октября 2020.
- ^ а б c d е ж «Иммунная система и нарушения». MedlinePlus, Национальный институт медицины США. 28 сентября 2020 г.. Получено 13 октября 2020.
- ^ Мужчина, Дэвид К. (2006). Иммунология. Elsevier Health Sciences. п. 10. ISBN 978-0323033992.
- ^ а б Гэвин, А.Л .; Hoebe, K; Дуонг, B; Ота, Т; Мартин, C; Beutler, B; Немазее, Д. (22 декабря 2006 г.). «Усиленные адъювантом ответы антител в отсутствие передачи сигналов толл-подобного рецептора». Наука. 314 (5807): 1936–38. Bibcode:2006Научный ... 314.1936G. Дои:10.1126 / science.1135299. ЧВК 1868398. PMID 17185603.
- ^ Галуччи, S; Лолкема, М; Мацингер, П. (ноябрь 1999 г.). «Природные адъюванты: эндогенные активаторы дендритных клеток». Природа Медицина. 5 (11): 1249–55. Дои:10.1038/15200. PMID 10545990. S2CID 29090284.
- ^ а б «Антигенная характеристика». Центры США по контролю и профилактике заболеваний. 15 октября 2019 г.. Получено 13 октября 2020.
- ^ Стребхардт, Клаус; Ульрих, Аксель (июнь 2008 г.). «Концепция волшебной пули Пауля Эрлиха: 100 лет прогресса». Обзоры природы Рак. 8 (6): 473–80. Дои:10.1038 / nrc2394. ISSN 1474-1768. PMID 18469827. S2CID 30063909.
- ^ Линденманн, Жан (1984). «Происхождение терминов« антитело »и« антиген »'". Сканд. J. Immunol. 19 (4): 281–85. Дои:10.1111 / j.1365-3083.1984.tb00931.x. PMID 6374880. Получено 2008-10-31.[мертвая ссылка ]
- ^ Дулан Д.Л., Саутвуд С., Фрейлих Д.А., Сидни Дж., Грабер Н.Л., Шатни Л., Бебрис Л., Флоренс Л., Добано С., Уитни А.А., Аппелла Е., Хоффман С.Л., Йейтс Дж.Р., Каруччи Д.Д., Сетте А. (август 2003 г.). «Идентификация антигенов Plasmodium falciparum с помощью антигенного анализа геномных и протеомных данных». Труды Национальной академии наук Соединенных Штатов Америки. 100 (17): 9952–57. Bibcode:2003ПНАС..100.9952Д. Дои:10.1073 / pnas.1633254100. ЧВК 187898. PMID 12886016.
- ^ Пархэм, Питер. (2009). Иммунная система, 3-е издание, стр. G: 2, Garland Science, Taylor and Francis Group, LLC.
- ^ Джейнвей, Калифорния, младший (1 ноября 2013 г.). «Статья Pillars: приближение к асимптоте? Эволюция и революция в иммунологии. Cold Spring harb symp Quant biol. 1989. 54: 1–13». Журнал иммунологии. 191 (9): 4475–87. PMID 24141854.
- ^ Гейед, PM (июнь 2011 г.). «К современному синтезу иммунитета: Чарльз А. Джейнвей-младший и маленький грязный секрет иммунолога». Йельский журнал биологии и медицины. 84 (2): 131–38. ISSN 1551-4056. ЧВК 3117407. PMID 21698045.
- ^ Пархэм, Питер. (2009). Иммунная система, 3-е издание, стр. G: 11, Garland Science, Taylor and Francis Group, LLC.
- ^ Кубы Иммунология (6-е изд.). Макмиллан. 2006. с. 77. ISBN 978-1-4292-0211-4.
- ^ а б c d е ж грамм час я Шумахер, Тон Н .; Шрайбер, Роберт Д. (3 апреля 2015 г.). «Неоантигены в иммунотерапии рака». Наука. 348 (6230): 69–74. Bibcode:2015Научный ... 348 ... 69S. Дои:10.1126 / science.aaa4971. PMID 25838375.
- ^ Ван, Цин .; Дуглас, Жаклин (16 сентября 2019 г.). «Прямое обнаружение и количественная оценка неоантигенов». Cancer Immunol Res. 7 (11): 1748–54. Дои:10.1158 / 2326-6066.CIR-19-0107. ЧВК 6825591. PMID 31527070.
- ^ К. Аббас, Абул; Лихтман, Эндрю; Пиллаи, Шив (2018). Клеточная и молекулярная иммунология (Девятое изд.). Филадельфия: Эльзевьер. п. 97. ISBN 978-0-323-52324-0.
