Посттравматический припадок - Post-traumatic seizure
Посттравматические припадки (PTS) находятся припадки это результат травматическое повреждение мозга (TBI), повреждение мозга вызванный физическая травма. ПИН может быть фактором риска посттравматическая эпилепсия (PTE), но у человека, у которого есть припадок или судороги из-за черепно-мозговой травмы, не обязательно есть PTE, которая является формой эпилепсия, хроническое состояние, при котором судороги возникают повторно. Однако «PTS» и «PTE» могут использоваться в медицинской литературе как взаимозаменяемые.[1]
Судороги обычно являются признаком более тяжелой ЧМТ.[1] Судороги, возникающие вскоре после травмы головного мозга, могут еще больше повредить и без того уязвимый мозг.[2] Они могут уменьшить количество кислорода, доступного для мозга,[3] вызывать возбуждающий нейротрансмиттеры быть выпущенным в избытке, увеличить мозг метаболический нужно, и поднять давление во внутричерепном пространстве, что еще больше способствует повреждению.[2] Таким образом, людям, получившим тяжелую травму головы, дается противосудорожное средство лекарства в качестве меры предосторожности против судорог.[3]
Около 5–7% людей, госпитализированных с ЧМТ, имеют по крайней мере один приступ.[4] Посттравматический стрессовый синдром более вероятен при более серьезных травмах, а некоторые виды травм еще больше увеличивают риск. Риск того, что человек пострадает от посттравматического стресса, постепенно снижается с течением времени после травмы. Однако люди, пережившие ЧМТ, могут по-прежнему подвергаться риску в течение 15 лет после травмы.[5] Дети и пожилые люди подвержены более высокому риску развития ПИН.
Классификация
В середине 1970-х PTS были впервые классифицированы Брайан Дженнетт в рано и поздние припадки, возникающие в течение первой недели после травмы и те, которые происходят через неделю, соответственно.[6] Хотя семидневный предел для ранних приступов широко используется, он является произвольным; судороги, возникающие после первой недели, но в течение первого месяца травмы, могут иметь общие характеристики с ранними приступами.[7] В некоторых исследованиях вместо этого используется 30-дневный предел для ранних приступов.[8] Позже было принято делить приступы на немедленный PTS, судороги, возникшие в течение 24 часов после травмы; ранний посттравматический стрессовый синдром с припадками в период от одного дня до недели после травмы; и поздний ПИН, судороги более чем через неделю после травмы.[9] Некоторые считают поздний ПИН синонимом посттравматическая эпилепсия.[10]
Ранний посттравматический синдром возникает, по крайней мере, один раз примерно у 4–5% людей, госпитализированных с ЧМТ, а поздний посттравматический синдром случается у 5% из них.[9] Примерно половина припадков, возникающих в течение первой недели после травмы, происходит в течение первых 24 часов.[11] У детей ранние припадки более вероятны в течение часа и дня после травмы, чем у взрослых.[12] Из припадков, возникающих в течение первых четырех недель после травмы головы, около 10% возникают после первой недели.[5] Поздние судороги чаще всего возникают в первые несколько недель после травмы.[7] Около 40% поздних приступов начинаются в течение шести месяцев после травмы, а 50% - в течение года.[11]
Опасное для жизни состояние стойких судорог, особенно у детей и людей с тяжелой ЧМТ, называется эпилептический статус есть риск ранних приступов; От 10 до 20% посттравматических стрессов перерастают в состояние.[11] В одном исследовании у 22% детей в возрасте до 5 лет развились статусные припадки, в то время как у 11% всей изученной популяции с ЧМТ развились.[12] Статусные судороги на ранней стадии после ЧМТ могут повысить шансы того, что у человека позже возникнут неспровоцированные приступы.[11]
Патофизиология
Не совсем понятно, какие физиологические механизмы вызывают судороги после травмы, но считается, что ранние судороги имеют другие основные процессы, чем поздние.[13] Считается, что немедленные и ранние судороги являются прямой реакцией на травму, в то время как поздние судороги считаются результатом повреждения сустава. кора головного мозга такими механизмами, как эксайтотоксичность и железо из крови.[2] Немедленные припадки, происходящие в течение двух секунд после травмы, вероятно, происходят из-за того, что сила от травмы стимулирует ткань мозга, которая имеет низкий порог припадков при стимуляции.[14] Ранние ППС считаются спровоцированными припадками, потому что они возникают в результате прямого воздействия травмы головы и, таким образом, не рассматриваются как настоящая эпилепсия, в то время как поздние припадки, как полагают, указывают на постоянные изменения в структуре мозга и подразумевают эпилепсию.[11] Ранние судороги могут быть вызваны такими факторами, как: отек мозга, внутричерепное кровоизлияние, ушиб головного мозга или разрыв.[14] Факторы, которые могут привести к припадкам, которые происходят в течение двух недель после инсульта, включают наличие крови в головном мозге; изменения в гематоэнцефалический барьер; чрезмерное высвобождение возбуждающих нейротрансмиттеров, таких как глутамат; повреждение тканей, вызванное свободные радикалы; и изменения в способе производства энергии клетками.[13] Считается, что поздние судороги являются результатом эпилептогенез, в котором нейронные сети реструктурированы таким образом, что увеличивается вероятность возбуждения, что приведет к припадкам.[13]
Диагностика
Медицинский персонал стремится определить, вызван ли приступ изменением биохимии пациента, например: гипонатриемия.[2] Неврологические осмотры и тесты для измерения уровня сыворотки электролиты выполняются.[2]
Не все приступы, возникающие после травмы, являются ПИН; они могут быть следствием уже существовавшего судорожного расстройства, которое могло даже стать причиной травмы.[15] Кроме того, посттравматические припадки не следует путать с сотрясения судороги, который может сразу следовать сотрясение но которые на самом деле не являются приступами и не являются прогностическим фактором эпилепсии.[16]
Нейровизуализация используется для руководства лечением. Часто, МРТ выполняется у любого пациента с ПТС, но менее чувствительна, но легче доступна компьютерная томография также могут быть использованы.[17]
Профилактика
Вскоре после ЧМТ людям назначают противосудорожные препараты, потому что судороги, возникающие сразу после травмы, могут усилить повреждение головного мозга. гипоксия,[3] чрезмерное высвобождение возбуждающего нейротрансмиттеры, повышенные метаболические потребности и повышенное давление во внутричерепном пространстве.[2] Лекарства, используемые для предотвращения судорог, включают: вальпроат, фенитоин, и фенобарбитал.[18] Рекомендуется начать лечение противосудорожными препаратами как можно скорее после ЧМТ.[8] Профилактика ранних приступов отличается от профилактики поздних припадков, поскольку цель первых - предотвратить повреждение, вызванное припадками, а цель последних - предотвратить эпилептогенез.[3] Убедительные доказательства клинических испытаний показывают, что противоэпилептические препараты, назначаемые в течение дня после травмы, предотвращают судороги в течение первой недели после травмы, но не после нее.[4] Например, обзор медицинской литературы 2003 года показал, что фенитоин предотвращает ранний, но, вероятно, не поздний посттравматический синдром.[7] У детей противосудорожные препараты могут быть неэффективными как при ранних, так и при поздних приступах.[4] По неизвестным причинам профилактическое применение противоэпилептических препаратов в течение длительного периода связано с повышенным риском судорог.[1] По этим причинам противоэпилептические препараты широко рекомендуются в течение короткого времени после травмы головы для предотвращения немедленных и ранних, но не поздних судорог.[1][19] Нет широко распространенного лечения для предотвращения развития эпилепсии.[3] Однако могут быть назначены лекарства для подавления большего числа приступов, если припадки все же происходят.[18]
Уход
Судороги, вызванные ЧМТ, часто трудно поддаются лечению.[13] Можно давать противоэпилептические препараты внутривенно вскоре после травмы включают фенитоин, вальпроат натрия, карбамазепин, и фенобарбитал.[2] Противоэпилептические препараты не предотвращают всех приступов у всех людей.[5] но фенитоин и вальпроат натрия обычно купируют уже начавшиеся припадки.[2]
Прогноз
Посттравматический стрессовый синдром обычно ассоциируется с хорошим прогнозом.[14] Точно неизвестно, через какое время после ЧМТ человек подвергается более высокому риску судорог, чем остальная часть населения, но оценки предполагают продолжительность от 10 до более 15 лет.[5] У большинства людей с ЧМТ судороги не возникают через три месяца, и только 20–25% людей, страдающих ЧМТ, страдают ПТС спустя более двух лет после травмы.[9] Тем не менее, умеренная и тяжелая ЧМТ по-прежнему сопряжены с высоким риском развития ПИН в течение пяти лет после травмы.[4]
Исследования показали, что 25-40% пациентов с посттравматическим синдромом впадают в ремиссия; более поздние исследования, проведенные после разработки более эффективных противосудорожных препаратов, показали более высокий общий уровень ремиссии.[5] У четверти людей, страдающих судорогами в результате травмы головы, лекарства хорошо контролируют их.[1] Однако у некоторой части пациентов приступы возникают, несмотря на агрессивную противоэпилептическую терапию.[5] Вероятность ремиссии посттравматического стресса ниже у людей, у которых в первый год после травмы случаются частые приступы.[5]
Риск развития ПТЭ
Неизвестно, увеличивает ли ПИН вероятность развития ПТЭ.[13] Ранний посттравматический стрессовый синдром, хотя и не обязательно эпилептический по своей природе, связан с более высоким риском PTE.[20] Однако PTS не указывают на то, что развитие эпилепсии обязательно произойдет.[21] и трудно отделить ПИН от тяжести травмы как фактора развития ПТЭ.[13] Примерно у 3% пациентов без ранних приступов развивается поздняя ПТЭ; это число составляет 25% у тех, у кого есть ранний посттравматический стрессовый синдром, и разница будет больше, если исключить другие факторы риска развития ПТС.[21] Обычно считается, что приступы, возникающие сразу после инсульта, не вызывают повышенного риска повторных приступов, но данные по крайней мере одного исследования показали, что как немедленные, так и ранние приступы могут быть факторами риска поздних приступов.[5] Ранние судороги могут быть менее вероятным предиктором ПТЭ у детей; в то время как у трети взрослых с ранними приступами развивается ПТЭ, доля детей с ранним ПТС с поздними приступами составляет менее одной пятой детей и может составлять всего одну десятую.[12] Частота поздних приступов примерно вдвое меньше, чем у взрослых с сопоставимыми травмами.[12]
Эпидемиология

Исследования показали, что заболеваемость СТВ широко варьируется в зависимости от исследуемой популяции; он может составлять от 4,4% до 53%.[5] Из всех госпитализированных пациентов с ЧМТ от 5 до 7% страдают ПТС.[4] ПТС случаются примерно в 3,1% черепно-мозговых травм, но серьезность травмы влияет на вероятность возникновения.[9]
Наиболее важным фактором, определяющим, разовьются ли у человека приступы ранние или поздние, является степень повреждения головного мозга.[2] Более серьезная черепно-мозговая травма также создает риск развития посттравматического стрессового синдрома в течение длительного времени после события.[4] Одно исследование показало, что вероятность возникновения судорог в течение 5 лет после травмы составляет 0,5% от легкие черепно-мозговые травмы (определяется как нет перелом черепа и менее 30 минут посттравматическая амнезия, сокращенно PTA, или потеря сознания, сокращенно LOC); 1,2% травм средней степени тяжести (перелом черепа или PTA или LOC длительностью от 30 минут до 24 часов); и 10,0% тяжелых травм (ушиб головного мозга, внутричерепная гематома, или LOC или PTA более 24 часов).[23] Другое исследование показало, что риск судорог через 5 лет после ЧМТ составляет 1,5% при легкой форме (определяемой как ПТА или НР в течение менее 30 минут), 2,9% при умеренной (длительность от 30 минут до 1 дня) и 17,2% в тяжелой форме. ЧМТ (ушиб головного мозга, субдуральная гематома или LOC более суток; изображение справа).[2][11]
Немедленные припадки имеют частоту от 1 до 4%, ранние припадки составляют от 4 до 25%, а поздние припадки - от 9 до 42%.[2]
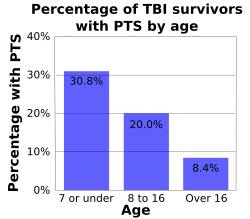
Возраст влияет на риск ПИН. С возрастом снижается риск ранних и поздних приступов; Одно исследование показало, что ранний посттравматический стрессовый синдром возник у 30,8% детей в возрасте 7 лет и младше, у 20% детей в возрасте от 8 до 16 лет и у 8,4% людей, которым на момент травмы было более 16 лет (график справа).[5][22] Ранние припадки у детей с черепно-мозговой травмой встречаются в два раза чаще, чем у их взрослых.[5] В одном исследовании дети в возрасте до пяти лет с незначительными травмами головного мозга (без LOC, без PTA, без депрессивного перелома черепа и без кровоизлияний) страдали ранним припадком в 17% случаев, в то время как люди старше 5 лет - только в 2% случаев. время.[5] У детей в возрасте до пяти лет припадки возникают в течение часа после травмы чаще, чем у взрослых.[11] Одно исследование показало, что частота ранних приступов наиболее высока среди младенцев младше одного года и особенно высока среди тех, кто пострадал. перинатальная травма.[14] Однако взрослые подвержены более высокому риску поздних приступов, чем дети.[24] Люди старше 65 лет также подвержены большему риску развития посттравматического стресса после травмы, причем риск посттравматического стресса в 2,5 раза выше, чем у их более молодых сверстников.[25]
Факторы риска
Вероятность того, что человек будет страдать от посттравматического стресса, зависит от факторов, связанных с травмой и человеком. Наибольшие риски для ПИН связаны с изменением уровня сознания в течение длительного времени после травмы, тяжелыми травмами с очаговыми поражениями и переломами.[8] Самый большой риск СТВ - это: проникающая травма головы, который несет от 35 до 50% риска судорог в течение 15 лет.[2] Если после травмы внутри черепа остается фрагмент металла, может возрасти риск как раннего, так и позднего ПИН.[5] Выжившие после травмы головы, которые злоупотреблял алкоголем до травмы также подвержены более высокому риску развития судорог.[4]
Случаи судорог широко варьируются даже среди людей с аналогичными травмами.[5] Неизвестно, играет ли генетика роль в риске ПИН.[11] Исследования дали противоречивые результаты в отношении вопроса о том, более ли вероятно, что у людей с посттравматическим синдромом будут члены семьи с припадками, что предполагает генетическую роль в посттравматическом стрессе.[11] Большинство исследований показали, что эпилепсия у членов семьи не увеличивает значительно риск ПТС.[5] Люди с ApoE-ε4 аллель также может иметь более высокий риск позднего ПИН.[1]
Риски позднего ПИН включают: гидроцефалия, снижение притока крови к височные доли мозга,[1] ушибы головного мозга, субдуральные гематомы,[5] разорванный твёрдая мозговая оболочка, и очаговые неврологические нарушения.[9] ПТА, продолжающаяся более 24 часов после травмы, является фактором риска как раннего, так и позднего ПИН.[1] До 86% людей, перенесших один поздний посттравматический припадок, переносят другой в течение двух лет.[5]
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час Такер GJ (2005). «16: Припадки». В Silver JM, McAllister TW, Yudofsky SC (ред.). Учебник по черепно-мозговой травме. American Psychiatric Pub., Inc., стр. 309–321. ISBN 1-58562-105-6.
- ^ а б c d е ж грамм час я j k л м Агравал А., Тимоти Дж., Пандит Л., Манджу М. (2006). «Посттравматическая эпилепсия: обзор». Клиническая неврология и нейрохирургия. 108 (5): 433–439. Дои:10.1016 / j.clineuro.2005.09.001. PMID 16225987. S2CID 2650670.
- ^ а б c d е Иудис А., Мурри Л. (2000). «Фармакологическая профилактика посттравматической эпилепсии». Наркотики. 59 (5): 1091–9. Дои:10.2165/00003495-200059050-00005. PMID 10852641. S2CID 28616181.
- ^ а б c d е ж грамм Тизелл Р., Байона Н., Липперт С., Вильямер Дж., Хеллингс С. (2007). «Посттравматическое судорожное расстройство после приобретенной черепно-мозговой травмы». Травма головного мозга. 21 (2): 201–214. Дои:10.1080/02699050701201854. PMID 17364531. S2CID 43871394.
- ^ а б c d е ж грамм час я j k л м п о п q р Фрей LC (2003). «Эпидемиология посттравматической эпилепсии: критический обзор». Эпилепсия. 44 (Приложение 10): 11–17. Дои:10.1046 / j.1528-1157.44.s10.4.x. PMID 14511389. S2CID 34749005.
- ^ Swash M (1998). Исходы при неврологических и нейрохирургических расстройствах. Кембридж, Великобритания: Издательство Кембриджского университета. С. 172–173. ISBN 0-521-44327-X.
- ^ а б c Чанг Б.С., Lowenstein DH (2003). «Практический параметр: Противоэпилептическая лекарственная профилактика при тяжелой черепно-мозговой травме: отчет подкомитета стандартов качества Американской академии неврологии». Неврология. 60 (1): 10–16. Дои:10.1212 / 01.wnl.0000031432.05543.14. PMID 12525711.
- ^ а б c Гарга Н, Lowenstein DH (2006). «Посттравматическая эпилепсия: серьезная проблема, остро нуждающаяся в серьезных достижениях». Эпилепсия Curr. 6 (1): 1–5. Дои:10.1111 / j.1535-7511.2005.00083.x. ЧВК 1363374. PMID 16477313.
- ^ а б c d е Cuccurullo S (2004). Обзор совета по физической медицине и реабилитации. Demos Medical Publishing. С. 68–71. ISBN 1-888799-45-5. Получено 2008-02-13.
- ^ Бенардо LS (2003). «Профилактика эпилепсии после травмы головы: нужны ли новые препараты или новый подход?». Эпилепсия. 44 (Приложение 10): 27–33. Дои:10.1046 / j.1528-1157.44.s10.2.x. PMID 14511392. S2CID 35133349.
- ^ а б c d е ж грамм час я Гупта А., Уилли Е., Лачвани Д.К. (2006). Лечение эпилепсии: принципы и практика. Хагерстаун, Мэриленд: Липпинкотт Уильямс и Уилкинс. С. 521–524. ISBN 0-7817-4995-6.
- ^ а б c d Молодой Б. (1992). «Посттравматическая эпилепсия». В Барроу DL (ред.). Осложнения и последствия травмы головы. Парк-Ридж, штат Иллинойс: Американская ассоциация неврологических хирургов. С. 127–132. ISBN 1-879284-00-6.
- ^ а б c d е ж Герман СТ (2002). «Эпилепсия после инсульта: нацеливание на эпилептогенез». Неврология. 59 (9 Дополнение 5): S21 – S26. Дои:10.1212 / wnl.59.9_suppl_5.s21. PMID 12428028. S2CID 6978609.
- ^ а б c d Менкес JH, Сарнат HB, Мария BL (2005). Детская неврология. Хагерстаун, Мэриленд: Липпинкотт Уильямс и Уилкинс. п. 683. ISBN 0-7817-5104-7. Получено 2008-06-12.
- ^ Кушнер Д (1998). «Легкая черепно-мозговая травма: к пониманию проявлений и лечению». Архивы внутренней медицины. 158 (15): 1617–1624. Дои:10.1001 / archinte.158.15.1617. PMID 9701095.
- ^ Роппер AH, Горсон KC (2007). «Клиническая практика. Сотрясение мозга». Медицинский журнал Новой Англии. 356 (2): 166–172. Дои:10.1056 / NEJMcp064645. PMID 17215534.
- ^ Познер Э., Лоренцо Н. (11 октября 2006 г.). "Посттравматическая эпилепсия ". Emedicine.com. Проверено 19 февраля 2008.
- ^ а б Эндрюс Б.Т. (2003). Интенсивная терапия в нейрохирургии. Нью-Йорк: Thieme Medical Publishers. п. 192. ISBN 1-58890-125-4. Получено 2008-06-08.
- ^ Беги Э (2003). «Обзор исследований по профилактике посттравматической эпилепсии». Эпилепсия. 44 (Приложение 10): 21–26. Дои:10.1046 / j.1528-1157.44.s10.1.x. PMID 14511391. S2CID 25635858.
- ^ Оливерос-Жюсте А., Бертоль В., Оливерос-Сид А. (2002). «Профилактическое лечение при посттравматической эпилепсии». Revista de Neurología (на испанском). 34 (5): 448–459. Дои:10.33588 / ном.3405.2001439. PMID 12040514.
- ^ а б Чедвик Д. (2005). «Эпилепсия у взрослых». Электронная эпилепсия - Библиотека статей Национального общества эпилепсии.
- ^ а б Асикайнен И., Касте М., Сарна С. (1999). «Ранние и поздние посттравматические припадки у пациентов, реабилитированных после черепно-мозговой травмы: факторы повреждения головного мозга, вызывающие поздние припадки, и влияние припадков на отдаленный исход». Эпилепсия. 40 (5): 584–589. Дои:10.1111 / j.1528-1157.1999.tb05560.x. PMID 10386527. S2CID 20233355.
- ^ D'Ambrosio R, Perucca E (2004). «Эпилепсия после травмы головы». Текущее мнение в неврологии. 17 (6): 731–735. Дои:10.1097/00019052-200412000-00014. ЧВК 2672045. PMID 15542983.
- ^ Фирлик К.С., Спенсер Д.Д. (2004). «Хирургия посттравматической эпилепсии». В Dodson WE, Avanzini G, Shorvon SD, Fish DR, Perucca E (ред.). Лечение эпилепсии. Оксфорд: Blackwell Science. п. 775. ISBN 0-632-06046-8. Получено 2008-06-09.
- ^ Питкянен А., Макинтош Т.К. (2006). «Животные модели посттравматической эпилепсии». Журнал нейротравмы. 23 (2): 241–261. Дои:10.1089 / neu.2006.23.241. PMID 16503807.