Общий синтез афлатоксина - Aflatoxin total synthesis
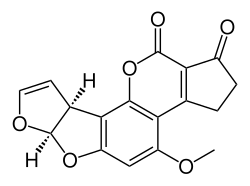
Общий синтез афлатоксина касается полный синтез группы органические соединения называется афлатоксины. Эти соединения встречаются в природе в нескольких грибы. Как и в случае с другими целями химического соединения в органическая химия, органический синтез афлатоксинов служит различным целям. Традиционно он служил для доказательства структуры сложного биосоединения в дополнение к свидетельствам, полученным с помощью спектроскопии. Он также демонстрирует новые концепции в органической химии (реагенты, типы реакций) и открывает путь к молекулярным производным, не встречающимся в природе. И для практических целей синтетическое биосоединение представляет собой коммерческую альтернативу выделению соединения из природных ресурсов. Афлатоксины, в частности, добавляют еще одно измерение, потому что есть подозрения, что в прошлом они производились массово из биологических источников как часть биологическое оружие программа.
О синтезе рацемического афлатоксина B1 сообщили Buechi et al. в 1967 г. [1] и рацемический афлатоксин B2 Робертс и др. в 1968 г. [2] Группа Барри Трост из Стэндфордский Университет несет ответственность за энантиоселективный полный синтез из (+) - Афлатоксин B1 и B2а в 2003 г.[3] В 2005 году группа Э. Дж. Кори из Гарвардский университет представили энантиоселективный синтез афлатоксина B2.[4]
Синтез афлатоксина В2
Полный синтез афлатоксина B2 представляет собой многоступенчатую последовательность, которая начинается с [2 + 3]циклоприсоединение между хинон 1 и 2,3-дигидрофуран. Эта реакция катализируется Катализатор CBS и является энантиоселективный. Следующий шаг - это ортоформилирование продукта реакции 2 в Дафф реакция. В гидроксил группа в 3 является этерифицированный с трифликовый ангидрид что добавляет тройной защитная группа. Этот шаг позволяет Реакция Гриньяра из альдегид группа в 4 с метилмагнийбромидом алкоголь 5 что тогда окисленный с Десс-Мартин периодинан к кетон 6. А Окисление Байера-Виллигера превращает кетон в сложный эфир (7) и снижение с Никель Ренея превращает сложный эфир в спирт и удаляет группу трифликовой кислоты. На последнем этапе кумарин скелет добавлен к 9 комбинированным реакция сочетания с карбонат цинка из винилбромид в 8 и стадию переэтерификации между фенольной группой и группой этилового эфира.
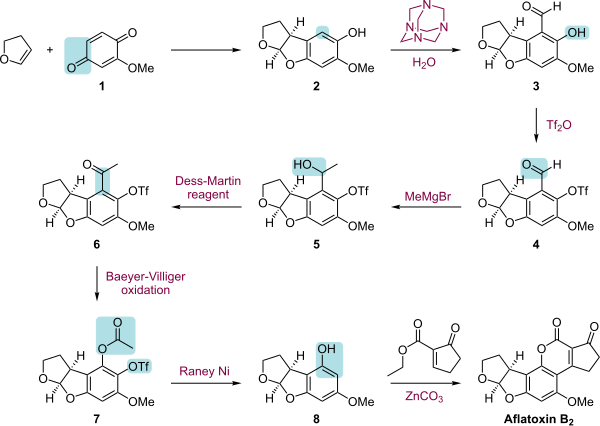 |
| Общий синтез афлатоксина В2 |
|---|
Рекомендации
- ^ Буэчи, Джордж; Фоулкс, Д. М .; Куроно, Масаясу; Митчелл, Гэри Ф .; Шнайдер, Ричард Стивен (1967). «Полный синтез рацемического афлатоксина В1». Журнал Американского химического общества. 89 (25): 6745–53. Дои:10.1021 / ja01001a062. PMID 6063661.
- ^ Робертс, Джон С .; Шеппард, А. Х .; Knight, J. A .; Роффи, Патрик (1968). «Исследования по микологической химии. Часть XXII. Полный синтез (±) -афлатоксина-B2». Журнал химического общества C: Органический: 22. Дои:10.1039 / J39680000022.
- ^ Trost, B.M .; Тост, Ф. Д. "Катализируемые палладием кинетические и динамические кинетические асимметричные превращения γ-ацилоксибутенолидов. Энантиоселективный полный синтез (+) - афлатоксина B1 и B2а". Варенье. Chem. Soc. 2003, 125, 3090–3100. Дои:10.1021 / ja020988s
- ^ Чжоу, G .; Кори, Э. Дж. "Краткий, энантиоселективный полный синтез афлатоксина B"2 Использование шага асимметричного [3 + 2] -циклоприсоединения ». Варенье. Chem. Soc. 2005, 127, 11958–11959. Дои:10.1021 / ja054503m
