Афлатоксин - Aflatoxin
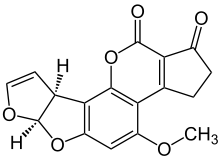
Афлатоксины находятся ядовитый канцерогены и мутагены которые производятся некоторыми формы (Aspergillus flavus и Паразитарный аспергилл ), которые растут в почве, гниющей растительности, сене и зернах. Их регулярно обнаруживают в неправильно хранимых основные товары такие как маниока, перцы чили, хлопок, просо, арахис, рис, семена кунжута, сорго, семена подсолнечника, сладкая кукуруза, орехи, пшеница, и различные специи. При переработке зараженных пищевых продуктов афлатоксины попадают в общую пищевую базу, где они были обнаружены как в кормах для домашних животных, так и в продуктах питания для людей, а также в кормах для сельскохозяйственных животных. Животные, которых кормили зараженной пищей, могут передавать продукты трансформации афлатоксина в яйца, молочные продукты и мясо.[1] Например, наличие контаминированного корма для домашней птицы подозревается в обнаружении высокого процента проб загрязненных афлатоксином куриного мяса и яиц в Пакистане.[2]
Дети особенно страдают от воздействия афлатоксина, которое связано с задержкой роста,[3] задержка развития,[4] повреждение печени и рак печени. Связь между задержкой роста в детстве и воздействием афлатоксина[5] сообщалось в некоторых исследованиях[6][7] но не удалось обнаружить во всех.[8][9] Более того, причинно-следственная связь между задержкой роста в детстве и воздействием афлатоксина еще предстоит окончательно продемонстрировать эпидемиологическими исследованиями, хотя такие исследования еще продолжаются.[10][11] Взрослые имеют более высокую переносимость воздействия, но также подвержены риску. Ни один вид животных не застрахован. Афлатоксины являются одними из самых канцерогенный известные вещества.[12] После попадания в организм афлатоксины могут метаболизироваться в печени до реактивных веществ. эпоксид промежуточный или гидроксилированный, чтобы стать менее вредным афлатоксином M1.
Афлатоксины чаще всего попадают в организм. Однако самый токсичный тип афлатоксина, B1, может проникать через кожу.[13]
В Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) уровни действия на афлатоксин, присутствующий в пище или подача от 20 до 300 ppb.[14] FDA имело возможность объявить отзыв кормов для людей и домашних животных в качестве меры предосторожности для предотвращения воздействия.
Термин «афлатоксин» происходит от названия одной из форм, которые его производят, Aspergillus flavus. Он был придуман примерно в 1960 году после открытия в качестве источника "Болезнь индейки X ".[15] Афлатоксины составляют одну из основных групп микотоксины.
Основные типы и их метаболиты
Афлатоксин B1 считается наиболее токсичным и производится обоими Aspergillus flavus и Паразитарный аспергилл. Афлатоксин М1 присутствует в ферментационном бульоне Паразитарный аспергилл, но он и афлатоксин М2 также производятся, когда инфицированная печень метаболизирует афлатоксин B1 и B2.
- Афлатоксин B1 и B2 (AFB), производства Aspergillus flavus и A. parasiticus
- Афлатоксин G1 и G2 (AFG), производятся некоторыми Группами II A. flavus и Паразитарный аспергилл[16]
- Афлатоксин М1 (АСМ1), метаболит афлатоксина B1 у людей и животных (воздействие в нг уровни могут поступать из материнского молока)
- Афлатоксин М2, метаболит афлатоксина B2 в молоке крупного рогатого скота, питающегося зараженными продуктами[17]
- Афлатоксикол (AFL): метаболит, образующийся при расщеплении лактонового кольца.
- Афлатоксин Q1 (AFQ1), главный метаболит AFB1 в in vitro препараты печени других высших позвоночных[18]
AFM, AFQ и AFL сохраняют возможность превращения в эпоксид. Тем не менее, они кажутся гораздо менее способными вызывать мутагенез чем неметаболизированный токсин.[19]
Условия загрязнения
Афлатоксины производятся обоими Aspergillus flavus и Паразитарный аспергилл, которые являются обычными формами «сорных» грибов, широко распространенных в природе. Присутствие этих плесневых грибов не всегда указывает на присутствие вредных уровней афлатоксина, но указывает на значительный риск. Плесневые грибки могут колонизировать и заражать пищу перед сбором урожая или во время хранения, особенно после длительного воздействия окружающей среды с высокой влажностью или стрессовых условий, таких как засуха.
Родная среда обитания Аспергиллы находится в почве, гниющей растительности, сено, и зерна подвергаются микробиологическому ухудшению, но он проникает во все типы органических субстратов, когда условия благоприятны для его роста. Благоприятные условия включают высокие содержание влаги (не менее 7%) и высокая температура. Афлатоксины были выделены из всех основных зерновых культур и из таких разнообразных источников, как арахисовое масло и каннабис. Основные продукты питания, регулярно зараженные афлатоксинами, включают маниоку, перец чили, кукурузу, семена хлопка, просо, арахис, рис, сорго, семена подсолнечника, древесные орехи, пшеницу и различные специи, предназначенные для употребления людьми или животными. Продукты преобразования афлатоксина иногда обнаруживаются в яйцах, молочных продуктах и мясе, когда животных кормят зараженным зерном.[1][20]
Исследование, проведенное в Кения и Мали обнаружил, что преобладающие методы сушки и хранения кукуруза были недостаточны для минимизации воздействия афлатоксинов.[21]
Органические культуры, которые не обрабатываются фунгициды, может быть более восприимчивым к заражению афлатоксинами.[22]
Профилактика
Имеются очень ограниченные доказательства того, что просвещение в области сельского хозяйства и питания может снизить воздействие афлатоксина в странах с низким и средним уровнем доходов.[23]
Патология
Ни один вид животных не застрахован от острая токсичность эффекты афлатоксинов. Взрослые люди имеют высокую толерантность к воздействию афлатоксина и редко заболевают острым афлатоксикозом.[24] но особенно страдают дети, и их воздействие может привести к задержке роста и задержке развития в дополнение ко всем симптомам, упомянутым ниже.[4]
Воздействие высокого уровня афлатоксина вызывает острый печеночный некроз (острый афлатоксикоз), приводящий позже к цирроз или рак печени. Острая печеночная недостаточность проявляется: кровотечение, отек, нарушение пищеварения, изменения всасывания и / или метаболизма питательных веществ, а также психические изменения и / или кома.[24]
Хронический, субклинический воздействие не приводит к таким драматическим симптомам, как острый афлатоксикоз. Хроническое воздействие увеличивает риск развития рака печени и желчного пузыря,[25] поскольку метаболиты афлатоксина могут вставлять в ДНК и алкилировать основы через эпоксид часть. Считается, что это вызывает мутации в p53 ген, важный ген в предотвращении прогрессирования клеточного цикла при мутациях ДНК или передаче сигналов апоптоз (запрограммированная гибель клеток). Эти мутации, по-видимому, влияют на расположение одних пар оснований больше, чем другие, например, третье основание кодона 249 гена p53, по-видимому, более восприимчиво к мутациям, опосредованным афлатоксином, чем соседние основания.[26] Как и другие ДНК-алкилирующие агенты, афлатоксин B1 может вызвать подавление иммунитета, и его воздействие связано с повышенным вирусная нагрузка в ВИЧ положительные личности.[27][28]
На проявление заболеваний, связанных с афлатоксином, влияют такие факторы, как вид, возраст, питание, пол и возможность одновременного воздействия других токсинов. Основным органом-мишенью у млекопитающих является печень, поэтому афлатоксикоз - это в первую очередь заболевание печени. Условия, повышающие вероятность афлатоксикоза у людей, включают ограниченную доступность пищи, условия окружающей среды, способствующие росту плесени на пищевых продуктах, и отсутствие систем регулирования для мониторинга и контроля афлатоксина.[29]
Регулярная диета, включающая обезьяноподобные овощи, такие как морковь, пастернак, сельдерей, и петрушка может уменьшить канцерогенный эффекты афлатоксина.[30]
Специфического антидота от афлатоксикоза не существует. Симптоматическая и поддерживающая терапия, адаптированная к степени тяжести заболевания печени, может включать внутривенное введение жидкости с декстрозой, активным витамином К, витаминами группы В и ограниченную, но высококачественную белковую диету с адекватным содержанием углеводов.
У других животных
У собак афлатоксин может вызвать заболевание печени. Низкие уровни воздействия афлатоксина требуют непрерывного потребления в течение нескольких недель или месяцев, чтобы появились признаки нарушения функции печени.[31] В некоторых статьях предполагается, что уровень токсичности в корме для собак составляет 100–300 частей на миллиард и требует постоянного воздействия или потребления в течение от нескольких недель до месяцев для развития афлатоксикоза.[32] Нет информации, позволяющей предположить, что выздоровевшие собаки позже погибнут от болезни, вызванной афлатоксином.
Индюки чрезвычайно подвержены афлатоксикозу. Недавние исследования показали, что это связано с эффективным цитохром P450 опосредованный метаболизм афлатоксина B1 в печени индеек и дефицитный глутатион-S-трансфераза опосредованная детоксикация.[33][34]
Некоторые исследования на беременных хомяках показали значительную взаимосвязь между воздействием афлатоксина B.1 (4 мг / кг, разовая доза) и появление аномалии развития в их потомстве.[35]
В 2005 году Diamond Pet Foods обнаружила афлатоксин в продукте, произведенном на их предприятии в г. Гастон, Южная Каролина.[36][37] В 23 штатах Diamond добровольно отозвала 19 продуктов, содержащих кукурузу и произведенных на предприятии в Гастоне. Лабораторные испытания более 2700 образцов готовой продукции подтвердили, что только два кода даты в двух смесях для взрослых собак потенциально могут быть токсичными.[38]
Обнаружение у людей
Есть два основных метода, которые наиболее часто используются для определения уровней афлатоксина у людей.
Первый метод - измерение AFB1-гуанин аддукт в моче испытуемых. Присутствие этого продукта распада указывает на воздействие афлатоксина B.1 в течение последних 24 часов. Однако этот метод измеряет только недавнее воздействие. Из-за период полураспада этого метаболита, уровень AFB1-гуанин может меняться изо дня в день, в зависимости от диеты, он не идеален для оценки долгосрочного воздействия.
Другой использованный метод - измерение AFB.1-альбумин уровень аддукта в сыворотке крови. Этот подход обеспечивает более комплексную оценку воздействия за несколько недель или месяцев.
Список вспышек
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Декабрь 2014 г.) |
Международные источники коммерческого арахисовое масло, кулинарные масла (например. оливковый, арахис и кунжутное масло ), и косметика были идентифицированы как загрязненные афлатоксином.[39][40][41] В некоторых случаях, жидкостная хроматография –тандемная масс-спектрометрия (ЖХ-МС / МС) и другие аналитические методы показали, что от 48% до 80% отобранных проб продуктов содержат определяемые количества афлатоксина. Во многих из этих загрязненных пищевых продуктов афлатоксин превышает безопасные пределы США. Управление по контролю за продуктами и лекарствами (FDA) или другой регулирующий орган.[40][41][42]
- 2003 Кения: острое отравление, 120 подтвержденных смертей.[43][44]
- Февраль – март 2013 г .: Румыния, Сербия, Хорватия импортировали в Западную Европу - Загрязнение афлатоксинами в 2013 г..
- Февраль 2013: Загрязнение штата Айова.[45]
- 2014 (в настоящее время): Непал и Бангладеш, неонатальные воздействия, обнаруженные в пуповина кровь.[43]
- Кения 2019: пять марок кукурузной муки отозваны из-за загрязнения.[46]
Смотрите также
Ресурсы
- ^ а б Fratamico PM, Bhunia AK, Smith JL (2008). Патогены пищевого происхождения: микробиология и молекулярная биология. Норофолк, Великобритания: Horizon Scientific Press. ISBN 978-1-898486-52-7.
- ^ Икбал С.З. и др. (2014). «Естественное распространение афлатоксинов, охратоксина А и зеараленона в курином мясе и яйцах». Контроль пищевых продуктов. 43: 98–103. Дои:10.1016 / j.foodcont.2014.02.046.
- ^ Хлангвисет П., Шепард Г.С., Ву Ф. (октябрь 2011 г.). «Афлатоксины и нарушение роста: обзор». Критические обзоры в токсикологии. 41 (9): 740–55. Дои:10.3109/10408444.2011.575766. PMID 21711088. S2CID 19262759.
- ^ а б Аббас HK (2005). Афлатоксин и безопасность пищевых продуктов. CRC Press. ISBN 978-0-8247-2303-3.
- ^ Смит Л. Е., Прендергаст А. Дж., Тернер П. К., Мбуя М. Н., Мутаса К., Кембо Дж., Штольцфус Р. Дж. (Декабрь 2015 г.). «Возможная роль микотоксинов как фактора задержки роста в испытании SHINE». Клинические инфекционные болезни. 61 Приложение 7: S733–7. Дои:10.1093 / cid / civ849. ЧВК 4657594. PMID 26602301.
- ^ Вот-Геддерт Л.Е., Стокер М., Торрес О., Эртер ДБ (апрель 2018 г.). "Ассоциация воздействия афлатоксина и соотношения роста к возрасту среди детей младшего возраста в Гватемале". Международный журнал исследований в области гигиены окружающей среды. 28 (3): 280–292. Дои:10.1080/09603123.2018.1468424. PMID 29706087. S2CID 23510545.
- ^ Turner PC, Collinson AC, Cheung YB, Gong Y, Hall AJ, Prentice AM, Wild CP (октябрь 2007 г.). «Воздействие афлатоксина в утробе матери вызывает задержку роста у младенцев из Гамбии». Международный журнал эпидемиологии. 36 (5): 1119–25. Дои:10.1093 / ije / dym122. PMID 17576701.
- ^ Митчелл Н.Дж., Сюй Х.Х., Чандио Р.К., Шреста Б., Бодхидатта Л., Ту Ю.К., Гонг Ю.Й., Эгнер ПА, Улак М., Групман Дж.Д., Ву Ф. (2017). «Воздействие афлатоксина в течение первых 36 месяцев жизни не было связано с нарушением роста у непальских детей: продолжение исследования MAL-ED». PLOS ONE. 12 (2): e0172124. Дои:10.1371 / journal.pone.0172124. ЧВК 5315312. PMID 28212415.
- ^ Chen C, Mitchell NJ, Gratz J, Houpt ER, Gong Y, Egner PA, Groopman JD, Riley RT, Showker JL, Svensen E, Mduma ER, Patil CL, Wu F (март 2018 г.). «Воздействие афлатоксина и фумонизина на детей из группы риска нарушения роста в сельских районах Танзании». Environment International. 115: 29–37. Дои:10.1016 / j.envint.2018.03.001. ЧВК 5989662. PMID 29544138.
- ^ Смит Л. Е., Прендергаст А. Дж., Тернер П. К., Мбуя М. Н., Мутаса К., Кембо Дж., Штольцфус Р. Дж. (Декабрь 2015 г.). «Возможная роль микотоксинов как фактора задержки роста в испытании SHINE». Клинические инфекционные болезни. 61 Дополнение 7 (Дополнение 7): S733–7. Дои:10.1093 / cid / civ849. ЧВК 4657594. PMID 26602301.
- ^ Хоффманн В., Джонс К., Лерой Дж. (Декабрь 2015 г.). «Снижение воздействия афлатоксина для улучшения роста ребенка в Восточной Кении: протокол рандомизированного контролируемого исследования». Испытания. 16: 552. Дои:10.1186 / s13063-015-1064-8. ЧВК 4669614. PMID 26634701.
- ^ Хадлер GW (1998). Волшебные грибы, озорные плесени: замечательная история о грибном королевстве и его влиянии на человеческие дела. Princeton University Press. ISBN 978-0-691-07016-2.
- ^ Бунен Дж., Малышева С.В., Тавернье Л., Диана Ди Мавунгу Дж., Де Сэгер С., Де Шпигелер Б. (ноябрь 2012 г.). «Проникновение в кожу человека выбранных модельных микотоксинов». Токсикология. 301 (1–3): 21–32. Дои:10.1016 / j.tox.2012.06.012. PMID 22749975.
- ^ «Руководство для промышленности: уровни действий в отношении ядовитых или вредных веществ в пищевых продуктах и кормах для животных». Управление по контролю за продуктами и лекарствами. Август 2000 г.. Получено 14 ноября, 2020.
- ^ Ванноп CC (март 1961 г.). «Гистопатология Турции» X «Болезнь в Великобритании». Заболевания птиц. 5 (4): 371–381. Дои:10.2307/1587768. JSTOR 1587768.
- ^ Гейзер Д.М., Дорнер Дж. В., Хорн Б. В., Тейлор Дж. В. (декабрь 2000 г.). «Филогенетика продукции микотоксинов и склероция у Aspergillus flavus и Aspergillus oryzae». Грибковая генетика и биология. 31 (3): 169–79. Дои:10.1006 / fgbi.2000.1215. PMID 11273679.
- ^ Афлатоксин М2 страница продукта из Ферментек
- ^ Смит Дж. Э., Сиверайт-Хендерсон Р. (1991). Микотоксины и продукты животного происхождения. CRC Press. п. 614. ISBN 978-0-8493-4904-1.
- ^ Neal GE, Eaton DL, Judah DJ, Verma A (июль 1998 г.). «Метаболизм и токсичность афлатоксинов M1 и B1 в человеческих системах in vitro». Токсикология и прикладная фармакология. 151 (1): 152–8. Дои:10.1006 / taap.1998.8440. PMID 9705898.
- ^ Pradeepkiran JA (декабрь 2018 г.). «Анализ афлатоксина B1 в загрязненных кормах, средах и образцах сыворотки Cyprinus carpio L. с помощью высокоэффективной жидкостной хроматографии». Качество и безопасность пищевых продуктов. 2 (4): 199–204. Дои:10.1093 / fqsafe / fyy013.
- ^ Нет шансов на афлатоксины В архиве 17 октября 2015 г. Wayback Machine Rural 21, Международный журнал развития сельских районов, 3 апреля 2013 г. - Проект Aflacontrol был проведен IFPRI с учеными из СИММИТ, то Международный научно-исследовательский институт сельскохозяйственных культур полузасушливых тропиков (ИКРИСАТ), Управление исследований арахиса и другие организации. Он стремился предоставить доказательства экономической эффективности стратегий снижения риска афлатоксина в кукуруза и арахис цепочки создания стоимости в Африке, и понять, что помешало принятию этих стратегий контроля.
- ^ Тосун Х, Арслан Р (2013). «Определение уровня афлатоксина B1 в органических специях и травах». Журнал ScienceWorld. 2013: 874093. Дои:10.1155/2013/874093. ЧВК 3677655. PMID 23766719.
- ^ Visser ME, Schoonees A, Ezekiel CN, Randall NP, Naude CE (апрель 2020 г.). «Мероприятия по просвещению в области сельского хозяйства и питания для снижения воздействия афлатоксина с целью улучшения роста младенцев и детей в странах с низким и средним уровнем доходов». Кокрановская база данных систематических обзоров. 4: CD013376. Дои:10.1002 / 14651858.cd013376.pub2. ЧВК 7141997. PMID 32270495.
- ^ а б Уильямс Дж. Х., Филлипс Т. Д., Веселый ЧП, Стайлз Дж. К., Веселый С. М., Аггарвал Д. (ноябрь 2004 г.). «Афлатоксикоз человека в развивающихся странах: обзор токсикологии, воздействия, потенциальных последствий для здоровья и вмешательств». Американский журнал клинического питания. 80 (5): 1106–22. Дои:10.1093 / ajcn / 80.5.1106. PMID 15531656.
- ^ Ногейра Л., Фёрстер С., Групман Дж., Эгнер П., Кошиол Дж., Ферреччио С. (май 2015 г.). «Ассоциация афлатоксина с раком желчного пузыря в Чили». JAMA. 313 (20): 2075–7. Дои:10.1001 / jama.2015.4559. ЧВК 7169945. PMID 26010638.
- ^ Агилар Ф., Хусейн С.П., Черутти П. (сентябрь 1993 г.). «Афлатоксин B1 индуцирует трансверсию G -> T в кодоне 249 гена-супрессора опухоли p53 в гепатоцитах человека». Труды Национальной академии наук Соединенных Штатов Америки. 90 (18): 8586–90. Дои:10.1073 / пнас.90.18.8586. ЧВК 47402. PMID 8397412.
- ^ Jolly PE, Инуса С., Лу Б., Эллис В.О., Ньярко А., Филлипс Т.Д., Уильямс Дж. Х. (2013). "Связь между высоким уровнем афлатоксина B1 уровни и высокая вирусная нагрузка у ВИЧ-положительных людей ». Всемирный журнал микотоксинов. 6 (3): 255–261. Дои:10.3920 / WMJ2013.1585. ЧВК 6750767. PMID 31534557.
- ^ «Обычный пищевой грибок может ускорить начало СПИДа». digitaljournal.com. 1 сентября 2013 г.
- ^ Мачида М., Гоми К., ред. (2010). Аспергиллы: Молекулярная биология и геномика. Caister Academic Press. ISBN 978-1-904455-53-0.
- ^ Петерсон С., Лампе Дж. В., Баммлер Т.К., Гросс-Штайнмейер К., Итон Д.Л. (сентябрь 2006 г.). «Компоненты апиальных овощей подавляют активность человеческого цитохрома P-450 1A2 (hCYP1A2) и hCYP1A2-опосредованную мутагенность афлатоксина B1». Пищевая и химическая токсикология. 44 (9): 1474–84. Дои:10.1016 / j.fct.2006.04.010. PMID 16762476.
- ^ Бингхэм А.К., Филлипс Т.Д., Бауэр Дж.Э. (март 2003 г.). «Возможности диетической защиты животных от воздействия афлатоксинов». Журнал Американской ветеринарной медицинской ассоциации. 222 (5): 591–6. Дои:10.2460 / javma.2003.222.591. PMID 12619837.
- ^ Bastianello SS, Nesbit JW, Williams MC, Lange AL (декабрь 1987 г.). «Патологические находки в естественной вспышке афлатоксикоза у собак». Журнал ветеринарных исследований Ондерстепорта. 54 (4): 635–40. PMID 3444619.
- ^ Равал С., Ип С.С., Куломб Р.А. (август 2010 г.). «Клонирование, экспрессия и функциональная характеристика цитохрома P450 3A37 из печени индейки с высокой активностью эпоксидирования афлатоксина B1». Химические исследования в токсикологии. 23 (8): 1322–9. Дои:10.1021 / ткс1000267. PMID 20707407.
- ^ Rawal S, Coulombe RA (август 2011 г.). «Метаболизм афлатоксина B1 в микросомах печени индейки: относительная роль цитохромов P450 1A5 и 3A37». Токсикология и прикладная фармакология. 254 (3): 349–54. Дои:10.1016 / j.taap.2011.05.010. PMID 21616088.
- ^ Goldblatt L (2012-12-02). Афлатоксин: научная основа, меры контроля и последствия. ISBN 9780323148498.
- ^ Отчет об инспекции FDA - завод Diamond Gaston SC, 12/21 / 2005-1 / 19/2006.
- ^ Напомним, 2005 г., FDA
- ^ Алмазные корма для домашних животных, загрязненные стандартным товаром AKC, и сроки годности сужены Akcstandard.com В архиве 7 июля 2011 г. Wayback Machine
- ^ Бао Л., Trucksess MW, White KD (2010). «Определение афлатоксинов B1, B2, G1 и G2 в оливковом масле, арахисовом масле и кунжутном масле». Журнал AOAC International. 93 (3): 936–42. Дои:10.1093 / jaoac / 93.3.936. PMID 20629398.
- ^ а б Ли Ф.К., Ли Ю.В., Ван Ю.Р., Ло XY (май 2009 г.). «Естественное наличие афлатоксинов в китайском арахисовом масле и кунжутной пасте». Журнал сельскохозяйственной и пищевой химии. 57 (9): 3519–24. Дои:10.1021 / jf804055n. PMID 19338351.
- ^ а б Махони Н., Молинье Р.Дж. (апрель 2010 г.). «Экспресс-аналитический метод определения афлатоксинов в пищевых добавках растительного происхождения и косметических маслах». Журнал сельскохозяйственной и пищевой химии. 58 (7): 4065–70. Дои:10.1021 / jf9039028. ЧВК 2858461. PMID 20235534.
- ^ Леонг Й.Х., Исмаил Н., Латифф А.А., Манаф Н.А., Росма А. (1 января 2011 г.). «Определение афлатоксинов в коммерческих орехах и ореховых продуктах с использованием тандемной масс-спектрометрии с жидкостной хроматографией». Всемирный журнал микотоксинов. 4 (2): 119–127. Дои:10.3920 / WMJ2010.1229.
- ^ а б «Угроза афлатоксина в Непале, Бангладеш». SciDev.Net Южная Азия. 2014-12-17. Получено 2016-10-17.
- ^ «Основные моменты Восточной и Южной Африки в 2011 году» (PDF). ИКРИСАТ. 2012. Получено 17 октября 2016.
- ^ «Отзыв корма для собак подчеркивает токсичность кукурузы в США, пострадавшей от засухи». Рейтер. 25 февраля 2013 года.
- ^ Мутахи Б. (15.11.2019). "Насколько безопасны основные продукты питания Кении?". Получено 2019-11-15.
