Эледуазин - Eledoisin
 | |
 | |
| Имена | |
|---|---|
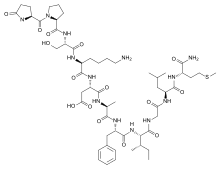
| Название ИЮПАК (3S)-3-[[(2S) -6-амино-2 - [[(2S) -3-гидрокси-2 - [[(2S)-1-[(2S) -5-оксопирролидин-2-карбонил] пирролидин-2-карбонил] амино] пропаноил] амино] гексаноил] амино] -4 - [[(2S)-1-[[(2S)-1-[[(2S,3S)-1-[[2-[[(2S)-1-[[(2S) -1-амино-4-метилсульфанил-1-оксобутан-2-ил] амино] -4-метил-1-оксопентан-2-ил] амино] -2-оксоэтил] амино] -3-метил-1-оксопентан -2-ил] амино] -1-оксо-3-фенилпропан-2-ил] амино] -1-оксопропан-2-ил] амино] -4-оксобутановая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C54ЧАС85N13О15S | |
| Молярная масса | 1188,40 г / моль |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Эледуазин является ундекапептид из моллюск происхождение, принадлежащий тачикинин семья нейропептиды.
Впервые он был изолирован от заднего слюнные железы двух видов моллюсков Eledone Muschata и Эледоне альдованди, которые принадлежат осьминог порядок Головоногие моллюски. [1]
Другие тахикинины из источников, не относящихся к млекопитающим, включают: кассинин и физалаэмин. Тахикинины млекопитающих вещество P, NKA и NKB обладают такими же эффектами, как тахикинины немлекопитающих, и были более широко изучены и охарактеризованы. Эти пептиды проявляют широкий и сложный спектр фармакологических и физиологических активностей, таких как расширение сосудов, гипертония, и стимуляция внесосудистого гладкая мышца.[2]
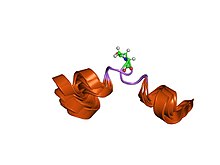
Eledoisin имеет аминокислотная последовательность pGlu-Pro-Ser-Lys-Asp-Ala-Phe-Ile-Gly-Leu-Met-NH2. Как и все пептиды тахикинина, эледоизин имеет одинаковую консенсусную С-концевую последовательность, то есть Phe-Xxx-Gly-Leu-Met-NH. Инвариантный остаток «Phe7», вероятно, необходим для связывания рецептора. «Ххх» представляет собой ароматическую (фенилаланин, тирозин) или разветвленную алифатическую (валин, изолейцин) боковую цепь и считается важным для селективности рецептора. Считается, что эта общая область, часто называемая «доменом сообщения», отвечает за активацию рецептора. Дивергентная N-концевая область или «адресный домен» различаются по аминокислотной последовательности и длине и, как полагают, играют роль в определении специфичности подтипа рецептора. [3]
Рекомендации
- ^ Де Марко, А. и Г. Гатти, «Спектры 1H- и 13C-ЯМР эледоизина и промежуточных олигопептидов». Int. J. Pep. Pro. Res. 7:437–444, 1975.
- ^ Р. Кристи Рани Грейс, Инду Р. Чандрашекар и Судха М. Ковсик, «Структура раствора тахикининового пептида эледоизина» В архиве 2008-10-11 на Wayback Machine, Биофизический журнал 84: 655-664 (2003), получено 5 декабря 2007 г. Эта публикация содержит отличную общую информацию о молекуле эледоизина.
- ^ Schwyzer, R., "Мембранно-вспомогательный молекулярный механизм выбора подтипа рецептора нейрокинина". EMBO J. 6:2255–2259, 1987
