Ламинин - Laminin
Ламинины высокие-молекулярный вес (От ~ 400 до ~ 900 кДа) белки внеклеточный матрикс. Они являются основным компонентом базальная пластинка (один из слоев базальная мембрана ), основу белковой сети для большинства клеток и органов. Ламинины - важная и биологически активная часть базальной пластинки, влияющая на дифференцировку, миграцию и адгезию клеток.[1][2]
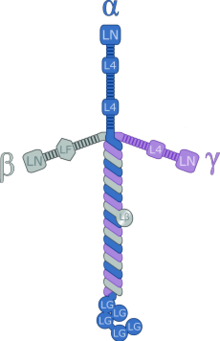
Ламинины - это гетеротримерные белки, которые содержат α-цепь, β-цепь и γ-цепь, встречающиеся в пяти, четырех и трех генетических вариантах соответственно. Молекулы ламинина названы в соответствии с их цепным составом. Таким образом, ламинин-511 содержит цепи α5, β1 и γ1.[3] Четырнадцать других комбинаций цепей были идентифицированы in vivo. Тримерные белки пересекаются, образуя крестообразную структуру, которая может связываться с другими молекулами клеточной мембраны и внеклеточного матрикса.[4] Три более коротких плеча особенно хорошо связываются с другими молекулами ламинина, что позволяет им образовывать листы. Длинное плечо способно связываться с клетками, что помогает прикрепить организованные тканевые клетки к мембране.
Семейство ламининов гликопротеины являются неотъемлемой частью структурного каркаса почти в каждой ткани организма. Они секретируются и включаются во внеклеточные матрицы, связанные с клетками. Ламинин жизненно важен для поддержания и выживания тканей. Дефектные ламинины могут вызывать неправильное формирование мышц, что приводит к форме мышечной дистрофии, смертельной болезни, связанной с образованием пузырей на коже (узловой буллезный эпидермолиз ) и дефекты почечного фильтра (нефротический синдром ).[5]
Типы
Идентифицировано пятнадцать тримеров ламинина. Ламинины представляют собой комбинации различных альфа-, бета- и гамма-цепей.[6]
- Пять форм альфа-цепей: LAMA1, LAMA2, LAMA3 (который имеет три формы сращивания), LAMA4, LAMA5
- Бета-цепочки включают: LAMB1, LAMB2, LAMB3, LAMB4 (обратите внимание, что ни один из известных тримеров ламинина не включает LAMB4, и его функция остается плохо изученной)
- Гамма-цепочки: LAMC1, LAMC2, LAMC3
Ламинины были ранее пронумерованы по мере их открытия, то есть ламинин-1, ламинин-2, ламинин-3 и т. Д., Но номенклатура была изменена, чтобы описать, какие цепи присутствуют в каждой изоформе (ламинин-111, ламинин-211 и т. Д.). ).[3] Кроме того, многие ламинины имели общие названия до того, как появилась номенклатура ламининов.[7][8]
| Старая номенклатура | Старые синонимы | Состав цепи | Новая номенклатура |
|---|---|---|---|
| Ламинин-1 | EHS ламинин | α1β1γ1 | Ламинин-111 |
| Ламинин-2 | Меросин | α2β1γ1 | Ламинин-211 |
| Ламинин-3 | S-ламинин | α1β2γ1 | Ламинин-121 |
| Ламинин-4 | S-мерозин | α2β2γ1 | Ламинин-221 |
| Ламинин-5 / Ламинин-5А | Калинин, эпилигрин, ницкин, ладсин | α3Aβ3γ2 | Ламинин-332 / Ламинин-3A32 |
| Ламинин-5Б | α3Bβ3γ2 | Ламинин-3B32 | |
| Ламинин-6 / Ламинин-6А | К-ламинин | α3Aβ1γ1 | Ламинин-311 / Ламинин-3A11 |
| Ламинин-7 / Ламинин-7А | КС-ламинин | α3Aβ2γ1 | Ламинин-321 / Ламинин-3A21 |
| Ламинин-8 | α4β1γ1 | Ламинин-411 | |
| Ламинин-9 | α4β2γ1 | Ламинин-421 | |
| Ламинин-10 | Дрозофила-подобный ламинин | α5β1γ1 | Ламинин-511 |
| Ламинин-11 | α5β2γ1 | Ламинин-521 | |
| Ламинин-12 | α2β1γ3 | Ламинин-213 | |
| Ламинин-14 | α4β2γ3 | Ламинин-423 | |
| α5β2γ2 | Ламинин-522 | ||
| Ламинин-15 | α5β2γ3 | Ламинин-523 |
Функция
Ламинины образуют независимые сети и связаны с коллаген IV типа сети через энтактин,[9] фибронектин,[10] и перлекан. Они также связываются с клеточными мембранами через интегрин рецепторы и другие плазматическая мембрана молекулы, такие как дистрогликан гликопротеиновый комплекс и гликопротеин лютеранской группы крови.[4] Посредством этих взаимодействий ламинины критически способствуют прикреплению и дифференцировке клеток, форме и движению клеток, поддержанию фенотипа ткани и обеспечению выживания ткани.[4][6] Некоторые из этих биологических функций ламинина связаны со специфическими аминокислотными последовательностями или фрагментами ламинина.[4] Например, пептид Последовательность [GTFALRGDNGDNGQ], которая расположена на альфа-цепи ламинина, способствует адгезии эндотелиальных клеток.[11]
Ламинин альфа4 распространяется в различных ткани включая периферические нервы, ганглий дорсального корня, скелетные мышцы и капилляры; в нервно-мышечный стык, это необходимо для синаптический специализация.[12] В структура домена ламинина-G было предсказано напоминать пентраксин.[13]
Роль в нервном развитии
Ламинин-111 является основным субстратом, вдоль которого будут расти нервные аксоны как in vivo, так и in vitro. Например, он прокладывает путь, по которому развивающиеся ганглиозные клетки сетчатки следуют от сетчатки до тектума. Он также часто используется в качестве субстрата в экспериментах с культурами клеток. Присутствие ламинина-1 может влиять на реакцию конуса роста на другие сигналы. Например, ростовые конусы отталкиваются нетрином при выращивании на ламинине-111, но притягиваются к нетрину при выращивании на фибронектине.[нужна цитата ] Этот эффект ламинина-111, вероятно, происходит за счет снижения внутриклеточного циклического АМФ.[нужна цитата ]
Роль в восстановлении периферических нервов
Ламинины обогащаются в месте поражения после повреждения периферического нерва и секретируются Шванновские клетки. Нейроны периферическая нервная система экспрессируют рецепторы интегрина, которые прикрепляются к ламининам и способствуют нейрорегенерация после травмы.[14]
Патология
Дисфункциональная структура одного конкретного ламинина, ламинина-211, является причиной одной формы врожденная мышечная дистрофия.[15] Ламинин-211 состоит из α2, а β1 и γ1 цепи. Распределение ламинина включает мозг и мышечные волокна. В мышцах он связывается с альфа-дистрогликан и интегрин альфа7 —beta1 через домен G, а через другой конец он связывается с внеклеточный матрикс.
Аномальный ламинин-332, который необходим для адгезии эпителиальных клеток к базальной мембране, приводит к состоянию, называемому узловой буллезный эпидермолиз, характеризуется генерализованными волдырями, обильными грануляциями кожи и слизистых оболочек и зубами с ямками.
Неисправный ламинин-521 в почечном фильтре вызывает утечку белка в мочу и нефротический синдром.[5]
Роль в раке
В этом разделе тон или стиль могут не отражать энциклопедический тон используется в Википедии. (Июль 2012 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
Некоторые изоформ ламинина вовлечены в патофизиологию рака. Большинство стенограмм, содержащих внутренний сайт входа рибосомы (IRES) участвуют в развитии рака через соответствующие белки. Важнейшее событие в прогрессировании опухоли, называемое эпителиально-мезенхимальный переход (EMT) позволяет клеткам карциномы приобретать инвазивные свойства. Недавно сообщалось о трансляционной активации компонента внеклеточного матрикса ламинина B1 (LAMB1) во время EMT, что позволяет предположить механизм, опосредованный IRES. В этом исследовании IRES-активность LamB1 определялась независимыми бицистронными репортерными анализами. Убедительные доказательства исключают влияние криптического промотора или сайтов сплайсинга на управляемую IRES трансляцию LamB1. Более того, не было обнаружено никаких других видов мРНК LamB1, возникающих из альтернативных сайтов старта транскрипции или сигналов полиаденилирования, которые объясняют его трансляционный контроль. Картирование 5'-нетранслируемой области LamB1 (UTR) выявило минимальный мотив IRES LamB1 между -293 и -1 перед стартовым кодоном. Примечательно, что аффинная очистка РНК показала, что белок La взаимодействует с LamB1 IRES. Это взаимодействие и его регуляция во время ЭМП были подтверждены иммунопреципитацией рибонуклеопротеидов. Кроме того, La был способен положительно модулировать трансляцию LamB1 IRES. Таким образом, эти данные показывают, что LamB1 IRES активируется путем связывания с La, что приводит к усилению трансляции во время гепатоцеллюлярной EMT.[16]
Использование в культуре клеток
Вместе с другими основными компонентами внеклеточного матрикса, такими как коллагены и фибронектин, ламинины использовались для улучшения культуры клеток млекопитающих, особенно в случае плюрипотентных стволовых клеток, а также некоторых первичных культур клеток, размножение которых может быть затруднено на других. субстраты. В продаже имеются два типа ламининов естественного происхождения. Ламинин-111, экстрагированный из сарком мышей, является одним из популярных типов ламинина, а также смеси ламининов из плаценты человека, которые в первую очередь могут соответствовать ламинину-211, 411 или 511, в зависимости от поставщика.[17] Различные изоформы ламинина практически невозможно выделить из тканей в чистом виде из-за обширного поперечного сшивания и необходимости жестких условий экстракции, таких как протеолитические ферменты или низкий pH, которые вызывают деградацию. Следовательно, рекомбинантный ламинины производятся с 2000 года.[18] Это позволило проверить, могут ли ламинины играть значительную роль. in vitro как в человеческом теле. В 2008 году две группы независимо друг от друга показали, что эмбриональные стволовые клетки мыши можно в течение нескольких месяцев выращивать на рекомбинантном ламинине-511.[19][20] Позже Роден и другие. показали, что рекомбинантный ламинин-511 можно использовать для создания полностью свободной от ксено и определенной среды для культивирования клеток для культивирования плюрипотентных ES-клеток человека и человеческих iPS-клеток.[21]
Ламининовые домены
| Ламинин Домен I | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | Ламинин_I | ||||||||
| Pfam | PF06008 | ||||||||
| ИнтерПро | IPR009254 | ||||||||
| |||||||||
| Ламинин Домен II | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | Ламинин_II | ||||||||
| Pfam | PF06009 | ||||||||
| ИнтерПро | IPR010307 | ||||||||
| |||||||||
| Ламинин B (домен IV) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | Ламинин_Б | ||||||||
| Pfam | PF00052 | ||||||||
| ИнтерПро | IPR000034 | ||||||||
| |||||||||
| Ламинин EGF-подобный (домены III и V) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 кристаллическая структура трех последовательных модулей ламинина типа эпидермального фактора роста (le) цепи ламинина гамма1, несущих сайт связывания нидогена | |||||||||
| Идентификаторы | |||||||||
| Символ | Ламинин_EGF | ||||||||
| Pfam | PF00053 | ||||||||
| Pfam клан | CL0001 | ||||||||
| ИнтерПро | IPR002049 | ||||||||
| PROSITE | PDOC00021 | ||||||||
| SCOP2 | 1шт / Объем / СУПФАМ | ||||||||
| |||||||||
| Домен Ламинина G | |||||||||
|---|---|---|---|---|---|---|---|---|---|
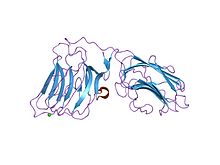 пара доменов lg4-5 ламинина альфа 2 цепи, мутант по сайту ca1 | |||||||||
| Идентификаторы | |||||||||
| Символ | Ламинин_G_1 | ||||||||
| Pfam | PF00054 | ||||||||
| Pfam клан | CL0004 | ||||||||
| ИнтерПро | IPR012679 | ||||||||
| SCOP2 | 1qu0 / Объем / СУПФАМ | ||||||||
| |||||||||
| Домен Ламинина G | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 структура лиганд-связывающего домена нейрексина 1beta: регуляция функции lns-домена путем альтернативного сплайсинга | |||||||||
| Идентификаторы | |||||||||
| Символ | Ламинин_G_2 | ||||||||
| Pfam | PF02210 | ||||||||
| Pfam клан | CL0004 | ||||||||
| ИнтерПро | IPR012680 | ||||||||
| УМНАЯ | ЦПН | ||||||||
| |||||||||
| N-конец ламинина (домен VI) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | Ламинин_N | ||||||||
| Pfam | PF00055 | ||||||||
| Pfam клан | CL0202 | ||||||||
| ИнтерПро | IPR008211 | ||||||||
| УМНАЯ | LamNT | ||||||||
| SCOP2 | 1кло / Объем / СУПФАМ | ||||||||
| |||||||||
Ламинины содержат несколько консервированный белковые домены.
Ламинин I и Ламинин II
Ламинины - это тримерные молекулы; ламинин-1 - это альфа1 бета1 гамма1 тример. Было высказано предположение, что домены I и II из ламинина A, B1 и B2 могут объединяться, образуя тройную спиральную спиральная катушка структура.[22]
Ламинин B
Домен ламинина B (также известный как домен IV) представляет собой внеклеточный модуль неизвестной функции. Он встречается в ряде различных белки которые включают, гепаран сульфат протеогликан из базальная мембрана, ламинин-подобный белок из Caenorhabditis elegans и ламинин. Домен ламинина IV не обнаруживается в коротких цепях ламинина (альфа4 или бета3).
Ламинин EGF-подобный
Помимо различных видов шаровидных домены каждая субъединица ламинина содержит в своей первой половине последовательные повторяет около 60 аминокислоты в длину, которые включают восемь консервированных цистеины.[23] Третичная структура этого домена отдаленно похожа по своему N-конец к тому из EGF-подобный модуль.[24][25] Он также известен как «LE» или «EGF-подобный домен ламининового типа». Число копий EGF-подобного домена ламинина в различных формах ламининов сильно варьирует; найдено от 3 до 22 экземпляров. В мышь цепь ламинина гамма-1, седьмой домен LE оказался единственным, который связывает с высокой близостью к нидоген.[26] Сайты связывания расположены на поверхности внутри петли C1-C3 и C5-C6.[24][25] Длинные последовательные массивы ламининовых EGF-подобных доменов в ламининах образуют стержневидные элементы ограниченной гибкости, которые определяют интервалы в формировании ламининовых сетей подвальные мембраны.[27][28]
Ламинин Г
Глобульный (G) домен ламинина, также известный как домен LNS (ламинин-альфа, нейрексин и глобулин, связывающий половые гормоны), составляет в среднем 177 аминокислоты в длину и может быть найден в количестве от одной до шести копий у различных членов семейства ламининов, а также у большого числа других внеклеточный белки.[29] Например, все альфа-цепи ламинина имеют пять доменов ламинина G, все коллаген белки семейства имеют один домен ламинина G, белки CNTNAP имеют четыре домена ламинина G, а нейрексин 1 и 2 каждый содержат шесть доменов ламинина G. В среднем примерно четверть белков, которые содержат домены ламинина G, захватываются этими доменами ламинина G сами по себе. Наименьший домен ламинина G можно найти в одном из белков коллагена (COL24A1; 77 AA), а самый большой домен - в TSPEAR (219 AA).
Точная функция ламинина G домены остается неуловимым, и различные связывающие функции были приписаны различным модулям Laminin G. Например, цепи ламинина альфа1 и альфа2 имеют по пять C-терминал домены ламинина G, где только домены LG4 и LG5 содержат участок связывания для гепарина, сульфатиды и рецептор клеточной поверхности дистрогликан.[30] Ламинин G-содержащий белки кажется, что они играют самые разные роли в клеточная адгезия, сигнализация, миграция, сборка и дифференциация.
Ламинин N-концевой
Базальная мембрана сборка - это совместный процесс, в котором ламинины полимеризовать через их N-концевой домен (LN или домен VI) и привязать к клетка поверхности через их G-домены. Нетрины могут также связываться с этой сетью через гетеротипные взаимодействия домена LN.[28] Это ведет к клеточная сигнализация через интегрины и дистрогликан (и, возможно, другие рецепторы) задействованы в прикрепленном ламинине. Эта самосборка, зависящая от домена LN, считается решающей для целостности базальных мембран, как подчеркивается генетический формы мышечная дистрофия содержащий делецию модуля LN из цепи альфа 2 ламинина.[31] N-концевой домен ламинина присутствует во всех ламинине и нетрине. подразделения кроме ламинина альфа 3А, альфа 4 и гамма 2.
Белки человека, содержащие домены ламинина
Ламинин Домен I
LAMA1; LAMA2; LAMA3; LAMA4; LAMA5;
Ламинин Домен II
LAMA1; LAMA2; LAMA3; LAMA4; LAMA5;
Ламинин B (домен IV)
HSPG2; LAMA1; LAMA2; LAMA3; LAMA5; LAMC1; LAMC2; LAMC3;
Ламинин EGF-подобный (домены III и V)
УСМЕШКА; ATRN; ATRNL1; CELSR1; CELSR2; CELSR3; CRELD1; HSPG2;LAMA1; LAMA2; LAMA3; LAMA4; LAMA5; LAMB1; LAMB2; LAMB3;LAMB4; LAMC1; LAMC2; LAMC3; MEGF10; MEGF12; MEGF6;MEGF8; MEGF9; NSR1; NTN1; NTN2L; NTN4; NTNG1; NTNG2;RESDA1; Шарф1; ШАРФ2; SREC; STAB1; USH2A;
Домен Ламинина G
УСМЕШКА; CELSR1; CELSR2; CELSR3; CNTNAP1; CNTNAP2; CNTNAP3; CNTNAP3B; CNTNAP4;CNTNAP5; COL11A1; COL11A2; COL12A1; COL14A1; COL15A1; COL16A1; COL18A1; COL19A1; COL20A1; COL21A1; COL22A1; COL24A1; COL27A1; COL5A1; COL5A3; COL9A1; CRB1; CRB2; CSPG4; EGFLAM; EYS; ТОЛСТЫЙ; FAT2; FAT3; FAT4; ГАЗ6; HSPG2; LAMA1; LAMA2; LAMA3; LAMA4; LAMA5; NELL1; NELL2; NRXN1; NRXN2; NRXN3;PROS1; SLIT1; SLIT2; SLIT3; КОПЬЕ; THBS1; THBS2; THBS3; THBS4; USH2A;
N-конец ламинина (домен VI)
LAMA1; LAMA2; LAMA3; LAMA5; LAMB1; LAMB2; LAMB3; LAMB4;LAMC1; LAMC3; NTN1; NTN2L; NTN4; NTNG1; NTNG2; USH2A;
Смотрите также
Рекомендации
- ^ Тимпл Р., Роде Х., Роби П.Г., Реннард С.И., Фойдарт Дж.М., Мартин Г.Р. (октябрь 1979 г.). «Ламинин - гликопротеин из базальных мембран». Журнал биологической химии. 254 (19): 9933–7. PMID 114518.
- ^ DOI 10.1007 / s00441-009-0838-2
- ^ а б Aumailley M, Bruckner-Tuderman L, Carter WG, Deutzmann R, Edgar D, Ekblom P, Engel J, Engvall E, Hohenester E, Jones JC, Kleinman HK, Marinkovich MP, Martin GR, Mayer U, Meneguzzi G, Miner JH, Миядзаки К., Патарройо М., Полссон М., Кваранта В., Санес Дж. Р., Сасаки Т., Секигучи К., Сорокин Л. М., Тальтс Дж. Ф., Трюггвасон К., Уитто Дж., Виртанен И., фон дер Марк К., Вевер Ю. М., Ямада Ю. Август 2005 г.). «Упрощенная номенклатура ламинина». Матричная биология. 24 (5): 326–32. Дои:10.1016 / j.matbio.2005.05.006. PMID 15979864.
- ^ а б c d М. А. Харальсон; Джон Р. Хасселл (1995). Внеклеточный матрикс: практический подход. Итака, Нью-Йорк: IRL Press. ISBN 978-0-19-963220-6.
- ^ а б Юрченко П.Д., Паттон Б.Л. (2009). «Онтогенетические и патогенетические механизмы сборки базальной мембраны». Текущий фармацевтический дизайн. 15 (12): 1277–94. Дои:10.2174/138161209787846766. ЧВК 2978668. PMID 19355968.
- ^ а б Colognato H, Yurchenco PD (июнь 2000 г.). «Форма и функция: семейство ламининов гетеротримеров». Динамика развития. 218 (2): 213–34. Дои:10.1002 / (SICI) 1097-0177 (200006) 218: 2 <213 :: AID-DVDY1> 3.0.CO; 2-R. PMID 10842354.
- ^ Ройс, Питер М., изд. (2002). Соединительная ткань и ее наследственные нарушения: молекулярные, генетические и медицинские аспекты (2-е изд.). Нью-Йорк: Вили-Лисс. п. 306. ISBN 9780471251859.
- ^ Кюн, Клаус (1997). «Составляющие внеклеточного матрикса как лиганды интегрина». На Эльбе, Йоханнес А. (ред.). Интегрин-лигандное взаимодействие. Нью-Йорк: Чепмен и Холл. п. 50. ISBN 9780412138614.
- ^ Смит Дж., Ockleford CD (январь 1994 г.). «Конфокальное исследование с помощью лазерного сканирования и сравнение нидогена (энтактина) с ламинином в условиях амниохориона человека». Плацента. 15 (1): 95–106. Дои:10.1016 / S0143-4004 (05) 80240-1. PMID 8208674.
- ^ Оклфорд К., Брайт Н., Хаббард А., Д'Лейси К., Смит Дж., Гардинер Л., Шейх Т., Альбентоса М., Черепаха К. (октябрь 1993 г.). «Микротрабекулы, макробляшки или базальные мини-мембраны в плодных оболочках доношенного человека?». Философские труды Лондонского королевского общества. Серия B, Биологические науки. 342 (1300): 121–36. Дои:10.1098 / rstb.1993.0142. PMID 7904354.
- ^ Бек и др., 1999.[уточнить ]
- ^ Итикава Н., Касай С., Судзуки Н., Ниси Н., Оиси С., Фуджи Н., Кадоя Ю., Хатори К., Мидзуно Ю., Номидзу М., Арикава-Хирасава Е. (апрель 2005 г.). «Идентификация активных участков роста нейритов на G-домене ламинина альфа4». Биохимия. 44 (15): 5755–62. Дои:10.1021 / bi0476228. PMID 15823034.
- ^ Бекманн Дж., Ханке Дж., Борк П., Райх Дж. Г. (февраль 1998 г.). «Слияние внеклеточных доменов: предсказание кратности для ламинин G-подобных и аминоконцевых тромбоспондин-подобных модулей на основе гомологии с пентраксинами». Журнал молекулярной биологии. 275 (5): 725–30. Дои:10.1006 / jmbi.1997.1510. PMID 9480764.
- ^ Nieuwenhuis, B .; Haenzi, B .; Andrews, M. R .; Verhaagen, J .; Фосетт, Дж. У. (2018). «Интегрины способствуют регенерации аксонов после травмы нервной системы». Биологические обзоры. 93 (3): 1339–1362. Дои:10.1111 / brv.12398. ЧВК 6055631. PMID 29446228.
- ^ Холл TE, Брайсон-Ричардсон Р.Дж., Бергер С., Джейкоби А.С., Коул Нью-Джерси, Холлуэй Г.Е., Бергер Дж., Карри П.Д. (апрель 2007 г.). «Мутант сахарной ваты у рыбок данио указывает на нарушение адгезии внеклеточного матрикса при врожденной мышечной дистрофии с дефицитом ламинина альфа2». Труды Национальной академии наук Соединенных Штатов Америки. 104 (17): 7092–7. Bibcode:2007PNAS..104.7092H. Дои:10.1073 / pnas.0700942104. ЧВК 1855385. PMID 17438294.
- ^ Petz M, Them N, Huber H, Beug H, Mikulits W. (январь 2012 г.). "La усиливает IRES-опосредованную трансляцию ламинина B1 во время перехода злокачественного эпителия в мезенхиму". Исследования нуклеиновых кислот. 40 (1): 290–302. Дои:10.1093 / nar / gkr717. ЧВК 3245933. PMID 21896617.
- ^ Вондиму З., Горфу Г., Каватаки Т., Смирнов С., Юрченко П., Трюггвасон К., Патарройо М. (март 2006 г.). «Характеристика коммерческих препаратов ламинина из плаценты человека по сравнению с рекомбинантными ламининами 2 (alpha2beta1gamma1), 8 (alpha4beta1gamma1), 10 (alpha5beta1gamma1)». Матричная биология. 25 (2): 89–93. Дои:10.1016 / j.matbio.2005.10.001. PMID 16289578.
- ^ Кортесмаа, Яркко; Юрченко, Петр; Трюггвасон, Карл (19 мая 2000 г.). «Рекомбинантный ламинин-8 (α4β1γ1)». Журнал биологической химии. 275 (20): 14853–14859. Дои:10.1074 / jbc.275.20.14853. PMID 10809728.
- ^ Домогацкая А., Роден С., Буто А., Трюггвасон К. (ноябрь 2008 г.). «Ламинин-511, но не -332, -111 или -411, делает возможным самообновление эмбриональных стволовых клеток мыши in vitro». Стволовые клетки. 26 (11): 2800–9. Дои:10.1634 / стволовые клетки.2007-0389. PMID 18757303.
- ^ Миядзаки Т., Футаки С., Хасэгава К., Кавасаки М., Сандзен Н., Хаяси М., Кавасе Е., Секигучи К., Накацудзи Н., Суэмори Х. (октябрь 2008 г.). «Рекомбинантные изоформы ламинина человека могут поддерживать недифференцированный рост эмбриональных стволовых клеток человека». Сообщения о биохимических и биофизических исследованиях. 375 (1): 27–32. Дои:10.1016 / j.bbrc.2008.07.111. PMID 18675790.
- ^ Родин С., Домогацкая А., Стрем С., Ханссон Е. М., Чиен К. Р., Инзунза Дж., Ховатта О., Трюггвасон К. (июнь 2010 г.). «Долгосрочное самообновление плюрипотентных стволовых клеток человека на рекомбинантном ламинине-511 человека». Природа Биотехнологии. 28 (6): 611–5. Дои:10.1038 / nbt.1620. HDL:10616/40259. PMID 20512123. S2CID 10801152.
- ^ Sasaki M, Kleinman HK, Huber H, Deutzmann R, Yamada Y (ноябрь 1988 г.). «Ламинин, мультидоменный белок. Цепь А имеет уникальный глобулярный домен и гомологию с протеогликаном базальной мембраны и цепями ламинина В». Журнал биологической химии. 263 (32): 16536–44. PMID 3182802.
- ^ Энгель Дж (июль 1989 г.). «EGF-подобные домены в белках внеклеточного матрикса: локализованные сигналы для роста и дифференцировки?». Письма FEBS. 251 (1–2): 1–7. Дои:10.1016/0014-5793(89)81417-6. PMID 2666164. S2CID 36607427.
- ^ а б Стетефельд Дж, Майер У., Тимпл Р., Хубер Р. (апрель 1996 г.). «Кристаллическая структура трех последовательных модулей ламинина типа эпидермального фактора роста (LE) цепи ламинина гамма1, несущих сайт связывания нидогена». Журнал молекулярной биологии. 257 (3): 644–57. Дои:10.1006 / jmbi.1996.0191. PMID 8648630.
- ^ а б Баумгартнер Р., Циш М., Майер У., Пёшль Э., Хубер Р., Тимпл Р., Холак Т.А. (апрель 1996 г.). «Структура нидоген-связывающего модуля LE ламинина гамма1 цепи в растворе». Журнал молекулярной биологии. 257 (3): 658–68. Дои:10.1006 / jmbi.1996.0192. PMID 8648631.
- ^ Mayer U, Pöschl E, Gerecke DR, Wagman DW, Burgeson RE, Timpl R (май 1995 г.). «Низкое сродство к нидогену ламинина-5 может быть связано с двумя остатками серина в EGF-подобном мотиве гамма 2III4». Письма FEBS. 365 (2–3): 129–32. Дои:10.1016 / 0014-5793 (95) 00438-Ф. PMID 7781764. S2CID 21559588.
- ^ Бек К., Хантер И., Энгель Дж. (Февраль 1990 г.). «Структура и функции ламинина: анатомия многодоменного гликопротеина». Журнал FASEB. 4 (2): 148–60. Дои:10.1096 / fasebj.4.2.2404817. PMID 2404817.
- ^ а б Юрченко П.Д., Ченг Ю.С. (август 1993 г.). «Самосборка и сайты связывания кальция в ламинине. Модель взаимодействия с тремя руками». Журнал биологической химии. 268 (23): 17286–99. PMID 8349613.
- ^ «Домен Ламинин Г». ИнтерПро. Европейский институт биоинформатики. Получено 22 февраля 2016.
- ^ Тиси Д., Тальтс Дж. Ф., Тимпл Р., Хоэнестер Э. (апрель 2000 г.). «Структура С-концевой пары ламинин-G-подобных доменов цепи альфа2 ламинина, несущей сайты связывания для альфа-дистрогликана и гепарина». Журнал EMBO. 19 (7): 1432–40. Дои:10.1093 / emboj / 19.7.1432. ЧВК 310212. PMID 10747011.
- ^ Xu H, Wu XR, Wewer UM, Engvall E (ноябрь 1994 г.). «Мышечная дистрофия мышей, вызванная мутацией в гене ламинина альфа 2 (Lama2)». Природа Генетика. 8 (3): 297–302. Дои:10.1038 / ng1194-297. PMID 7874173. S2CID 21549628.
внешняя ссылка
- Протеин ламинина
- Ламинин в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Обзор всей структурной информации, доступной в PDB за UniProt: P19137 (Субъединица ламинина альфа-1) на PDBe-KB.
- Обзор всей структурной информации, доступной в PDB за UniProt: P24043 (Субъединица ламинина альфа-2) на PDBe-KB.
- Обзор всей структурной информации, доступной в PDB за UniProt: O15230 (Субъединица ламинина альфа-5) на PDBe-KB.
