Диэтилкарбонат - Diethyl carbonate
 | |
| Имена | |
|---|---|
| Другие имена углекислый эфир; этилкарбонат; Юфин[1] | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.003.011 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 2366 |
| |
| |
| Характеристики | |
| C5ЧАС10О3 | |
| Молярная масса | 118.132 г · моль−1 |
| Внешность | Бесцветная прозрачная жидкость |
| Плотность | 0,975 г / см3 |
| Температура плавления | −74.3[2] ° С (-101,7 ° F, 198,8 К) |
| Точка кипения | От 126 до 128 ° C (от 259 до 262 ° F; от 399 до 401 K) |
| Нерастворимый | |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Предупреждение |
| H226, H315, H319, H335 | |
| P210, P233, P240, P241, P242, P243, P261, P264, P271, P280, P302 + 352, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P312, P321, P332 + 313, P337 + 313, P362, P370 + 378, P403 + 233, P403 + 235, P405, P501 | |
| точка возгорания | 33 ° С (91 ° F, 306 К) |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
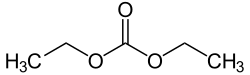
Диэтилкарбонат (иногда сокращенно DEC) является сложный эфир из угольная кислота и этиловый спирт с формулой OC (OCH2CH3)2. При комнатной температуре (25 ° C) диэтилкарбонат представляет собой прозрачную жидкость с низким точка возгорания.
Диэтилкарбонат используется как растворитель например, в эритромицин внутримышечные инъекции.[3][4] [5]Может использоваться как компонент электролиты в литиевые батареи. Он был предложен в качестве добавки к топливу для поддержки более чистого сгорания дизельного топлива, поскольку его высокая точка кипения может снизить летучесть смешанного топлива, сводя к минимуму накопление паров в теплую погоду, которое может блокировать топливопроводы.[6]
Производство
Это можно сделать, отреагировав фосген с этанолом, производя хлористый водород как побочный продукт. Потому что хлороформ может реагировать с кислородом с образованием фосгена, хлороформ можно стабилизировать для хранения путем добавления 1 части (по массе) этанола к 100 частям (по массе) хлороформа, так что любой образующийся фосген превращается в диэтилкарбонат.
Смотрите также
Рекомендации
- ^ «ДИЭТИЛКАРБОНАТ». Получено 2010-02-01.
- ^ Дин, Майкл (2001). «Диаграммы жидкой и твердой фаз бинарных карбонатов для литиевых батарей». Журнал Электрохимического общества. 148: A299 – A304. Дои:10.1149/1.1353568.
- ^ Андерсон, Роберт С .; Харрис, Пол Н .; Чен, К. К. (1955). «Дальнейшие токсикологические исследования с ilotycin® (Erythromycin, Lilly)». Журнал Американской фармацевтической ассоциации. 44 (4): 199–204. Дои:10.1002 / jps.3030440404. ISSN 1930-2304.
- ^ [1], "9-Дигидро-11,12-кетальные производные эритромицина А и эпиэритромицина А", выдано 01-03 1982
- ^ [2], «3», 4 «-Оксиаллилен, эритромицин и олеандомицин, состав и способ применения», выдан 1982-03-01
- ^ Уолтер К. Ученые открыли метод более чистого ископаемого топлива. Журнал MR&D. 18.09.2017 - 15:16
