Экологическая энтеропатия - Environmental enteropathy - Wikipedia
| Экологическая энтеропатия | |
|---|---|
| Другие имена | Тропическая энтеропатия или же Экологическая кишечная дисфункция |
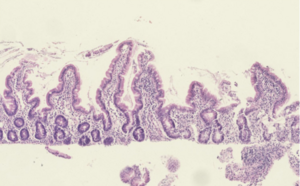 | |
| Гистологические свидетельства энтеропатии (воспалительный инфильтрат, притупление ворсинок), наблюдаемые в этой кишечной биопсии у ребенка с недоеданием.[1] | |
| Специальность | Гастроэнтерология |
| Симптомы | Бессимптомное течение (наиболее часто), изменение консистенции стула, учащение стула, потеря веса |
| Осложнения | Недоедание, мальабсорбция, задержка роста, задержка развития, нарушение реакции на пероральные вакцины |
| Продолжительность | Хронический |
| Причины | Антисанитарные источники пищи и воды, фекально-оральное заражение, хронические кишечные инфекции, воспаление слизистой оболочки |
| Диагностический метод | Биопсия кишечника (золотой стандарт), тест на аномальное всасывание сахара, клинический (значительно чаще) |
| Дифференциальная диагностика | Тропический литник |
| Профилактика | Санитария |
Экологическая энтеропатия (EE или же тропическая энтеропатия или же экологическая кишечная дисфункция) является заболеванием хронического воспаления кишечника.[2][3][1] ЭЭ чаще всего встречается среди детей, живущих в условиях ограниченных ресурсов.[2][3][1] Острые симптомы обычно минимальны или отсутствуют.[3] ЭЭ может привести к недоедание, анемия (железодефицитная анемия и анемия хронического воспаления ),[2] задержка роста, нарушение развития мозга,[4][5][6] и нарушение реакции на оральный прививки.[7][8]
Причина ЭЭ многофакторна. В целом, контакт с зараженной пищей и водой приводит к генерализованному состоянию воспаления кишечника.[2][3][1] Воспалительная реакция приводит к множественным патологическим изменениям желудочно-кишечного тракта: Меньшие ворсинки, большие склепы (называемые гиперплазия крипт ), повысился проницаемость и накопление воспалительных клеток в кишечнике.[3][1][9] Эти изменения приводят к плохому усвоению пищи, витаминов и минералов.
Стандартных клинически практических диагностических критериев не существует. Самый точный диагностический тест - биопсия кишечника. Однако этот тест является инвазивным и не нужен большинству пациентов.[2]
Профилактика - это самый сильный и надежный способ предотвратить ЭЭ и его последствия. Поэтому профилактику и лечение ЭЭ часто обсуждают вместе.[9][10][11]
Признаки и симптомы
Считается, что экологическая энтеропатия приводит к хроническим недоедание и последующие задержка роста (низкий рост к возрасту), а также другие нарушения развития ребенка.[нужна цитата ]
В ближайщем будущем
ЭЭ редко бывает симптоматическим и считается субклинический условие.[2][1][3] Однако у взрослых могут наблюдаться легкие симптомы или нарушение всасывания, такие как изменение консистенции стула, учащение стула и потеря веса.[нужна цитата ]
Долгосрочное
- Недоедание [2][3]
- ЭЭ причины недоедание посредством обоих нарушение всасывания и дефицит питательных веществ.
- Рост и физическое развитие [9]
- Первые два года (и предшествующие 9 месяцев жизни плода) имеют решающее значение для линейного роста. Замедление роста - это легко измеримый симптом таких нарушений развития ребенка.
- Нейрокогнитивные (развитие мозга) [5][6]
- Влияние на оральную вакцинацию [8][12]
- Многие устные вакцина, как живые, так и неживые, оказались менее иммуногенными или менее защитными при введении младенцы, дети или взрослые, живущие в низких социально-экономических условиях в развивающиеся страны чем они используются в промышленно развитые страны. Предполагается, что широко распространенная ЭЭ является одной из причин этого наблюдения.

Причины
Развитие ЭЭ является многофакторным, но в основном связано с хроническим воздействием загрязненной пищи и воды. Это особенно верно в средах, где широко распространены открытая дефекация и отсутствие санитария общие.[2][3][1]
Механизм
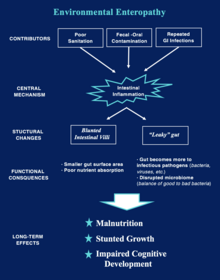
Длительное воздействие патогенов окружающей среды приводит к генерализованному состоянию воспаления кишечника. Хроническое воспаление приводит как к функциональным, так и к структурным изменениям, которые изменяют проницаемость кишечника и способность кишечника поглощать питательные вещества.[2][3][1]

В частности, структурные изменения в кишечнике включают: меньшие ворсинки, большие склепы (называемые гиперплазия крипт ), повышенной проницаемости и скоплением воспалительных клеток в кишечнике. Эти изменения приводят к плохому усвоению пищи, витаминов и минералов - или «скромному» нарушение всасывания ".[2][3][1]
Диагностика
В настоящее время золотым стандартом диагностики ЭЭ является биопсия кишечника и гистологический анализ. Наблюдаемые гистологические изменения включают:[1]
- Ворсинчатое притупление
- Гипертрофия склепа
- Ворсинчатый слияние
- Воспаление слизистой оболочки
Однако эта процедура считается слишком инвазивной, сложной и дорогостоящей, чтобы ее можно было применять в качестве стандартного лечения.[2] В результате ведутся различные исследования по выявлению биомаркеры связанные с ЭЭ, которые могут служить менее инвазивным, но репрезентативным инструментом для скрининга и идентификации ЭЭ по образцам стула.[2]
Чтобы определить простые и точные диагностические тесты на ЭЭ, Фонд Билла и Мелинды Гейтс (BMGF) учредила консорциум биомаркеров ЭЭ в рамках своей Глобальные великие испытания инициатива (в частности, задача «Обнаружить биомаркеры функции кишечника»).[2]
На данный момент были отобраны и изучены различные биомаркеры на основе современного понимания патофизиологии ЭЭ:[2]
- Проницаемость кишечника / барьерная функция
- Воспаление кишечника
- Экзокринный (гормональные) маркеры
- Маркеры бактериальной транслокации
- Антитело ядра эндотоксина
- Маркеры системного воспаления
Предполагается, что ограниченное понимание ЭЭ частично связано с нехваткой надежных биомаркеров, что затрудняет для исследователей отслеживание эпидемиологии заболевания и оценку эффективности вмешательств.[9]
Классификация
В 1960-х годах исследователи сообщили о синдроме неспецифической гистопатологический и функциональные изменения в тонкий кишечник у лиц, проживающих в антисанитарных условиях.[3] Этот синдром наблюдался преимущественно в тропических регионах Латинской Америки, Африки к югу от Сахары и Азии. Географическое распространение синдрома привело к оригинальному термину «тропическая энтеропатия» (иногда также «тропическая еюнопатия»).[3]
После первоначальных сообщений дальнейшее расследование показало, что эти симптомы не характерны для тропического климата. Например, у жителей более богатых тропических стран, таких как Катар и Сингапур, эти симптомы не проявлялись.[1] Точно так же последующие исследования показали, что это состояние широко распространено в развивающихся странах, тесно связано с бедными условиями, но не зависит от климата или географии.[1][9] В результате был введен термин «энтеропатия, связанная с окружающей средой», чтобы указать, что это состояние встречается не только в тропических регионах и, как полагают, вызвано факторами окружающей среды.[3]
Профилактика

Профилактика направлена на улучшение доступа к вода, санитария и гигиена (WASH).[14][15]
Еще одним важным фактором может быть зараженная почва в детских игровых площадках, часто вызываемая присутствием домашнего скота, например, кур. Таким образом, создание чистого игрового пространства может быть эффективной мерой профилактики ЭЭ у детей ясельного возраста.[16]
Уход
Лечение направлено на устранение центральных компонентов воспаления кишечника, избыточного бактериального роста и пищевых добавок.[2]
Эпидемиология
Экологическая энтеропатия (ЭЭ) в первую очередь поражает детей, живущих в странах с низким и средним уровнем доходов (СНСД).[17] Было обнаружено, что у детей, живущих в этих странах, на протяжении большей части раннего детства в их системах присутствовали кишечные патогены, связанные с ЭЭ.[17] Желудочно-кишечные аномалии, связанные с ЭЭ, не являются врожденными, но приобретаются в младенчестве и сохраняются в зрелом возрасте.[18][19] Такие аномалии имеют тенденцию развиваться после первого семестра жизни и отсутствуют у новорожденных.[18]
Исторически в СНСД преобладала экологическая энтеропатия.[19] Географическое распространение экологической энтеропатии показало рост заболеваемости в таких районах с плохой санитарией и гигиеной.[17] Впервые ЭЭ был описан в исследованиях 1960-70-х годов, проведенных в Азии, Африке, Индийском субконтиненте и Центральной Америке, в ходе которых было обнаружено, что признаки ЭЭ были высокими у здоровых взрослых и детей.[20] Исследование 1971 года, проведенное волонтерами Корпуса мира США, часто упоминается как первое исследование, демонстрирующее способность приобретать ЭЭ и восстанавливаться после него в зависимости от окружающей среды.[19] У участников возникли симптомы хронической кишечной инфекции во время и вскоре после возвращения из места пребывания в странах с низким и средним уровнем доходов.[17] Симптомы, с которыми столкнулись люди за границей, исчезли в течение одного-двух лет после возвращения домой в США.[19] Эти результаты приводят к предположению, что окружающая среда является причиной ЭЭ, и более позднее исследование в Замбии позволило сделать аналогичные выводы.[19] К началу 1990-х годов экологическая энтеропатия стала широко распространенной проблемой, затрагивающей младенцев и детей.[19] Сегодня кишечные инфекции и диарейные заболевания, такие как экологическая энтеропатия, являются причиной 760 000 смертей в год во всем мире, что делает ЭЭ второй ведущей причиной смерти среди детей в возрасте до пяти лет.[20]
Точные причины и последствия ЭЭ было трудно установить, отчасти из-за отсутствия четкого определения болезни.[17] Однако факторы риска действительно существуют, и они могут быть связаны как с окружающей средой, так и с питанием.[17] Существующие ранее состояния, такие как дефицит питательных микроэлементов, диарейные заболевания и различные хронические инфекции, служат факторами риска ЭЭ.[17] Условия окружающей среды, такие как плохая санитария и неулучшенные источники воды, также способствуют распространению ЭЭ.[17] Воздействие микробных агентов окружающей среды, подобных этим, считается наиболее важным фактором в развитии ЭЭ.[18]
Исследовательские инициативы
Существует множество крупных исследовательских инициатив в разных странах, посвященных стратегиям профилактики и лечения ЭЭ.[9]
- В MAL-ED проект
- В Живи и процветай проект питания
- В Исследование эффективности санитарии, гигиены и детского питания (SHINE) (Идентификатор ClinicalTrials.gov: NCT01824940 )
- В Преимущества WASH Изучать
Рекомендации
- ^ а б c d е ж грамм час я j k л Луи-Огюст Дж, Келли П. (июль 2017 г.). «Тропические энтеропатии». Текущие отчеты гастроэнтерологии. 19 (7): 29. Дои:10.1007 / s11894-017-0570-0. ЧВК 5443857. PMID 28540669.
- ^ а б c d е ж грамм час я j k л м п о Али А., Икбал Н.Т., Садик К. (январь 2016 г.). «Экологическая энтеропатия». Текущее мнение в гастроэнтерологии. 32 (1): 12–7. Дои:10.1097 / MOG.0000000000000226. PMID 26574871. S2CID 40064894.
- ^ а б c d е ж грамм час я j k л м Корпе П.С., Петри В.А. (июнь 2012 г.). «Экологическая энтеропатия: критические последствия плохо изученного состояния». Тенденции в молекулярной медицине. 18 (6): 328–36. Дои:10.1016 / j.molmed.2012.04.007. ЧВК 3372657. PMID 22633998.
- ^ Ngure FM, Reid BM, Humphrey JH, Mbuya MN, Pelto G, Stoltzfus RJ (январь 2014 г.). «Вода, санитария и гигиена (WASH), экологическая энтеропатия, питание и раннее развитие детей: установление связей». Летопись Нью-Йоркской академии наук. 1308 (1): 118–28. Bibcode:2014НЯСА1308..118Н. Дои:10.1111 / nyas.12330. PMID 24571214. S2CID 21280033.
- ^ а б Бхутта З.А., Геррант Р.Л., Нельсон Калифорния (апрель 2017 г.). «Нейроразвитие, питание и воспаление: эволюция глобального ландшафта детского здоровья». Педиатрия. 139 (Приложение 1): S12 – S22. Дои:10.1542 / пед.2016-2828d. PMID 28562245.
- ^ а б Джон СС, Блэк ММ, Нельсон Калифорния (апрель 2017 г.). «Нейроразвитие: влияние питания и воспаления в раннем и среднем детстве в условиях ограниченных ресурсов». Педиатрия. 139 (Приложение 1): S59 – S71. Дои:10.1542 / пед.2016-2828ч. ЧВК 5694688. PMID 28562249.
- ^ Ориа РБ, Мюррей-Колб Л.Е., Шарф Р.Дж., Пендергаст Л.Л., Ланг Д.Р., Коллинг Г.Л., Геррант Р.Л. (июнь 2016 г.). «Кишечные инфекции в раннем возрасте: связь между хроническим системным воспалением и плохой познавательной способностью у детей». Отзывы о питании. 74 (6): 374–86. Дои:10.1093 / Nutrit / nuw008. ЧВК 4892302. PMID 27142301.
- ^ а б Черкинский С., Холмгрен Дж. (Июнь 2015 г.). «Вакцины против кишечных инфекций для развивающихся стран». Философские труды Лондонского королевского общества. Серия B, Биологические науки. 370 (1671): 20150142. Дои:10.1098 / rstb.2015.0142. ЧВК 4527397. PMID 25964464.
- ^ а б c d е ж Прендергаст А., Келли П. (май 2012 г.). «Энтеропатии в развивающемся мире: игнорируемое влияние на глобальное здоровье». Американский журнал тропической медицины и гигиены. 86 (5): 756–63. Дои:10.4269 / ajtmh.2012.11-0743. ЧВК 3335677. PMID 22556071.
- ^ Хамфри Дж. Х. (сентябрь 2009 г.). «Детское недоедание, тропическая энтеропатия, туалеты и мытье рук». Ланцет. 374 (9694): 1032–1035. Дои:10.1016 / с0140-6736 (09) 60950-8. PMID 19766883. S2CID 13851530.
- ^ Мбуя М.Н., Хамфри Дж. Х. (май 2016 г.). «Предотвращение экологической кишечной дисфункции за счет улучшения водоснабжения, санитарии и гигиены: возможность сокращения задержки роста в развивающихся странах». Материнское и детское питание. 12 Дополнение 1: 106–20. Дои:10.1111 / mcn.12220. ЧВК 5019251. PMID 26542185.
- ^ Гилмартин А.А., Петри В.А. (июнь 2015 г.). «Изучение роли экологической энтеропатии в истощении, развитии младенцев и реакции на пероральные вакцины». Философские труды Лондонского королевского общества. Серия B, Биологические науки. 370 (1671): 20140143. Дои:10.1098 / rstb.2014.0143. ЧВК 4527388. PMID 25964455.
- ^ Луи-Огюст Дж, Келли П. (июль 2017 г.). «Тропические энтеропатии». Текущие отчеты гастроэнтерологии. 19 (7): 29. Дои:10.1007 / s11894-017-0570-0. ЧВК 5443857. PMID 28540669.
- ^ Мбуя М.Н., Хамфри Дж. Х. (май 2016 г.). «Предотвращение экологической кишечной дисфункции за счет улучшения водоснабжения, санитарии и гигиены: возможность для сокращения задержки роста в развивающихся странах». Материнское и детское питание. 12 Дополнение 1: 106–20. Дои:10.1111 / mcn.12220. ЧВК 5019251. PMID 26542185.
- ^ Нгуре FM, Рид Б.М., Хамфри Дж. Х., Мбуя М. Н., Пелто Дж., Штольцфус Р. Дж. (Январь 2014 г.). «Вода, санитария и гигиена (WASH), экологическая энтеропатия, питание и раннее развитие детей: установление связей». Летопись Нью-Йоркской академии наук. 1308 (1): 118–28. Bibcode:2014НЯСА1308..118Н. Дои:10.1111 / nyas.12330. PMID 24571214. S2CID 21280033.
- ^ Джордж К.М., Берроуз В., Перин Дж., Олджа Л., Бисвас С., Сак Д. и др. (Январь 2018). «Кишечные инфекции у детей младшего возраста связаны с экологической энтеропатией и нарушением роста». Тропическая медицина и международное здравоохранение. 23 (1): 26–33. Дои:10.1111 / tmi.13002. PMID 29121442.
- ^ а б c d е ж грамм час Tickell KD, Atlas HE, Walson JL (ноябрь 2019 г.). «Экологическая кишечная дисфункция: обзор потенциальных механизмов, последствий и стратегий управления». BMC Медицина. 17 (1): 181. Дои:10.1186 / s12916-019-1417-3. ЧВК 6876067. PMID 31760941.
- ^ а б c Мораис МБ, Сильва Г.А. (01.03.2019). «Экологическая кишечная дисфункция и рост». Jornal De Pediatria. 95 Дополнение 1: 85–94. Дои:10.1016 / j.jped.2018.11.004. PMID 30629923.
- ^ а б c d е ж Крейн Р.Дж., Джонс К.Д., Беркли Дж. А. (март 2015 г.). «Экологическая кишечная дисфункция: обзор». Бюллетень по продуктам питания и питанию. 36 (1 приложение): С76-87. Дои:10.1177 / 15648265150361S113. ЧВК 4472379. PMID 25902619.
- ^ а б Сайед С., Али А., Дагган С. (июль 2016 г.). «Экологическая кишечная дисфункция у детей». Журнал детской гастроэнтерологии и питания. 63 (1): 6–14. Дои:10.1097 / MPG.0000000000001147. ЧВК 4920693. PMID 26974416.
