Экзотермическая реакция - Exothermic reaction
An экзотермическая реакция "реакция, для которой общая стандартное изменение энтальпии ΔЧАС⚬ отрицательно. "[1][2] Экзотермические реакции обычно высвобождают высокая температура и влекут за собой замену слабых связей на более сильные.[3][4] Этот термин часто путают с экзэргоническая реакция, которую ИЮПАК определяет как «... реакцию, для которой общее стандартное изменение энергии Гиббса Δграмм⚬ отрицательно. "[2] Сильно экзотермическая реакция обычно также будет экергонической, потому что ΔЧАС⚬ вносит большой вклад в Δграмм⚬. Большинство впечатляющих химических реакций, которые демонстрируются в классах, являются экзотермическими и экзергоническими. Противоположным является эндотермическая реакция, который обычно нагревается и приводится в действие энтропия увеличение в системе.
Примеры
Примеры многочисленны: горение, то термитная реакция, сочетающий сильные кислоты и основания, полимеризация. Как пример из повседневной жизни, грелки для рук использовать окисление железа для достижения экзотермической реакции:
- 4Fe + 3O2 → 2Fe2О3 ΔЧАС⚬ = - 1648 кДж / моль
Особенно важным классом экзотермических реакций является сжигание углеводородного топлива, например сжигание природного газа:
- ΔЧАС⚬ = - 890 кДж / моль
В этих примерах большая часть выделенной энергии была сохранена в O2 с его относительно слабой двойной связью.[4] Большинство химических реакций включает в себя как разрыв существующих, так и создание новых, более прочных химических связей. Когда атомы объединяются, чтобы сформировать новые, более стабильные химические связи, объединяющие их электростатические силы оставляют связь с большим избытком энергии (обычно в форме колебаний и вращений). Если эта энергия не рассеивается, новая связь снова быстро развалится. Вместо этого новая связь может терять свою избыточную энергию - посредством излучения, путем передачи другим движениям в молекуле или другим молекулам посредством столкновений - а затем становиться стабильной новой связью. Эта избыточная энергия - это тепло, которое покидает молекулярную систему.
Неконтролируемые экзотермические реакции, приводящие к пожарам и взрывам, расточительны, потому что трудно улавливать выделяемую энергию. Природа осуществляет реакции горения в строго контролируемых условиях, избегая пожаров и взрывов, в аэробного дыхания чтобы улавливать высвобождаемую энергию, например для формирования АТФ.
Измерение
В энтальпия химической системы - это, по сути, ее энергия. Изменение энтальпии ΔЧАС для реакции равна теплоте q передается из (или внутрь) замкнутой системы при постоянном давлении без ввода или вывода электрической энергии. Производство или поглощение тепла в химической реакции измеряется с помощью калориметрия, например с калориметр бомбы. Одним из распространенных лабораторных инструментов является реакционный калориметр, где контролируется тепловой поток из реакционного сосуда или в него. Тепловыделение и соответствующее изменение энергии ΔЧАС, из горение реакция может быть измерена особенно точно.
Измеренная тепловая энергия, выделяемая в экзотермической реакции, преобразуется в ΔЧАС⚬ в Джоуль на моль (ранее кал / моль ). В стандарт изменение энтальпии ΔЧАС⚬ - это, по сути, изменение энтальпии, когда стехиометрический коэффициенты в реакции рассматриваются как количества реагентов и продуктов (в молях); обычно предполагается, что начальная и конечная температура составляет 25 ° C. Для газофазных реакций ΔЧАС⚬ значения связаны с энергии связи в хорошем приближении:
- ΔЧАС⚬ = общая энергия связи реагентов - общая энергия связи продуктов
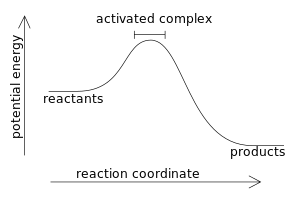
В экзотермической реакции изменение энтальпии по определению имеет отрицательное значение:
- ΔЧАС = ЧАСтовары - ЧАСреагенты < 0
где большее значение (более высокая энергия реагентов) вычитается из меньшего значения (более низкая энергия продуктов). Например, когда горит водород:
- 2H2 (г) + O2 (г) → 2H2O (г)
- ΔЧАС⚬ = −483,6 кДж / моль [5]
Смотрите также
- Химическая термодинамика
- Дифференциальная сканирующая калориметрия
- Эндергонический
- Экзергонический
- Эндергоническая реакция
- Экзэргоническая реакция
- Экзотермический процесс
- Эндотермический реакция
- Эндотерм
Рекомендации
- ^ «Экзотермическая реакция». ИЮПАК.
- ^ а б Лайдлер, К. Дж. (1996). «Глоссарий терминов, используемых в химической кинетике, включая динамику реакций (Рекомендации ИЮПАК 1996 г.)». Чистая и прикладная химия. 68: 149–192. Дои:10.1351 / pac199668010149. S2CID 98267946.
- ^ Галлей, Уильям К. (2004). «Разрыв экзотермической связи: стойкое заблуждение». Журнал химического образования. 81 (4): 523. Bibcode:2004JChEd..81..523G. Дои:10.1021 / ed081p523.
- ^ а б Шмидт-Рор, Клаус (2015). «Почему процессы горения всегда экзотермичны, давая около 418 кДж на моль O2». Журнал химического образования. 92 (12): 2094–2099. Bibcode:2015JChEd..92.2094S. Дои:10.1021 / acs.jchemed.5b00333.
- ^ «Архивная копия». Архивировано из оригинал на 2013-07-08. Получено 2013-07-20.CS1 maint: заархивированная копия как заголовок (связь)



