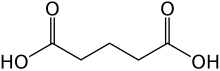
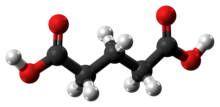
Глутаровая кислота - Glutaric acid
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Пентандиовая кислота | |
| Другие имена Глутаровая кислота Пропан-1,3-дикарбоновая кислота 1,3-пропандикарбоновая кислота Пентандиовая кислота н-Пиротартаровая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.003.471 |
| Номер ЕС |
|
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C5ЧАС8О4 | |
| Молярная масса | 132,12 г / моль |
| Температура плавления | От 95 до 98 ° C (от 203 до 208 ° F, от 368 до 371 K) |
| Точка кипения | 200 ° С (392 ° F, 473 К) / 20 мм рт. |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Глутаровая кислота это органическое соединение с формула C3ЧАС6(COOH)2 . Хотя родственный «линейный» дикарбоновые кислоты адипиновый и янтарные кислоты растворимы в воде только до нескольких процентов при комнатной температуре, растворимость в воде глутаровой кислоты составляет более 50% (мас. / мас.).
Биохимия
Глутаровая кислота естественным образом вырабатывается в организме во время метаболизм некоторых аминокислоты, включая лизин и триптофан. Дефекты в этом метаболическом пути может привести к расстройству, называемому глутаровая ацидурия, где накапливаются токсичные побочные продукты, которые могут вызвать серьезные энцефалопатия.
Производство
Глутаровая кислота может быть получена раскрытием цикла бутиролактон с цианистый калий дать смешанный карбоксилат калия-нитрил который гидролизуется до двухосновной кислоты.[1] В качестве альтернативы гидролиз с последующим окислением дигидропиран дает глутаровую кислоту. Его также можно приготовить из реакции 1,3-дибромпропан с натрий или же цианистый калий для получения динитрила с последующим гидролизом.
Использует
- 1,5-пентандиол, обычный пластификатор и предшественник полиэфиры производится гидрирование глутаровой кислоты и ее производных.[2]
- Сама глутаровая кислота использовалась в производстве полимеров, таких как полиэфир. полиолы, полиамиды. Нечетное число атомов углерода (т.е. 5) полезно для снижения эластичности полимера.[3]
- Увитоновая кислота получается действием аммиак по глутаровой кислоте.
- Пирогаллол может быть произведен из глутарового диэфира.[4]
Безопасность
Глутаровая кислота может вызывать раздражение кожи и глаз.[5] К острой опасности относится тот факт, что это соединение может быть вредным при проглатывании, вдыхании или абсорбции через кожу.[5]
Рекомендации
- ^ Г. Пэрис, Л. Берлингэ, Р. Годри, Дж. Инглиш младший и Дж. Э. Даян (1963). «Глутаровая кислота и глутарамид». Органический синтез.CS1 maint: несколько имен: список авторов (связь); Коллективный объем, 4, п. 496
- ^ Питер Верле и Маркус Моравиц «Спирты, многоатомные» в Энциклопедии промышленной химии Ульмана: 2002, Wiley-VCH: Weinheim. DOI 10.1002 / 14356007.a01_305
- ^ «Глутаровая кислота, пентандиовая кислота, 99%». Chemkits.eu. Получено 2020-09-29.
- ^ [1], «Способ синтеза пирогаллола», выдан 17.02.1976 г.
- ^ а б Глутаровая кислота, cameochemicals.com
