N-метилэтаноламин - N-Methylethanolamine
 | |
| Имена | |
|---|---|
| Название ИЮПАК 2-метиламиноэтанол | |
| Предпочтительное название IUPAC 2- (Метиламино) этан-1-ол | |
| Другие имена Метил-β-гидроксиэтиламин | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 1071196 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.003.374 |
| Номер ЕС |
|
| MeSH | N-метиламиноэтанол |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 2735 |
| |
| |
| Характеристики | |
| C3ЧАС9NО | |
| Молярная масса | 75.111 г · моль−1 |
| Внешность | Бесцветная жидкость |
| Запах | Аммиачный |
| Плотность | 0,935 г мл−1 |
| Температура плавления | -4,50 ° С; 23,90 ° F; 268,65 К |
| Точка кипения | 158,1 ° С; 316,5 ° F; 431,2 К |
| Смешиваемый | |
| бревно п | 1.062 |
| Давление газа | 70 Па (при 20 ° C) |
| 1.439 | |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасность |
| H302, H312, H314 | |
| P280, P305 + 351 + 338, P310 | |
| точка возгорания | 76 ° С (169 ° F, 349 К) |
| 350 ° С (662 ° F, 623 К) | |
| Пределы взрываемости | 1.6–19.8% |
| Родственные соединения | |
Родственные алканолы | |
Родственные соединения | Диэтилгидроксиламин |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
N-Метилэтаноламин является алканоламин с формулой CH3NHCH2CH2ОЙ. это легковоспламеняющийся, разъедающий, бесцветный, вязкий жидкость.[2] Это промежуточное звено в биосинтез из холин.
С обоими амин и гидроксил функциональные группы, это полезный промежуточный продукт в химический синтез различных продуктов, включая полимеры и фармацевтические препараты. Он также используется как растворитель, например при обработке натуральный газ, где используется вместе с аналогами этаноламин и диметилэтаноламин.
Производство
N-Метилэтаноламин получают в промышленных масштабах путем реакции окись этилена с избытком метиламин в водном растворе. Эта реакция дает смесь продукта присоединения 1: 1 NMEA (1) и - путем дальнейшего добавления другого оксида этилена - продукта присоединения 1: 2 метилдиэтаноламин (MDEA) (2):
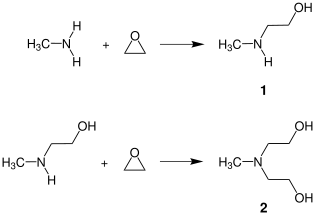
Чтобы получить высокие выходы желаемого целевого продукта, реагенты непрерывно подают в проточный реактор и реагируют с более чем двукратным избытком метиламина.[3] На последующих стадиях процесса избыток метиламина и воды удаляют, а NMEA (точка кипения 160 ° C) и MDEA (точка кипения 243 ° C) выделяют из смеси продуктов фракционной перегонкой. Поли (метилэтаноламин), образованный при дальнейшем добавлении оксида этилена к метилэтаноламину, остается в кубовых остатках после перегонки.
Характеристики
N-Метилэтаноламин - прозрачный, бесцветный, гигроскопичный, аминоподобная пахнущая жидкость, смешивающаяся с водой и этанолом в любом соотношении. Водные растворы сильно щелочны и поэтому вызывают коррозию. Вещество легко биоразлагаемо и не имеет потенциала биоаккумуляция из-за его смешиваемости с водой. NMEA не является мутагенным, но в присутствии нитрит, канцерогенный нитрозамины может быть образован из соединения, так как это вторичный амин.[4]
Использовать
Как и другие алкилалканоламины, N-метилэтаноламин используется в красках и покрытиях на основе воды и растворителей в качестве солюбилизатора для других компонентов, таких как пигменты, и в качестве стабилизатора.
В катодное покрытие погружением, N-метиламиноэтанол служит нейтрализатором катионов для частичной нейтрализации эпоксидная смола. Он также служит удлинителем цепи в реакции высокомолекулярных полиэпоксидов с полиолы.
Будучи базой, N-метиламиноэтанол образует нейтральные соли с жирные кислоты, которые используются в качестве поверхностно-активных веществ (мыла) с хорошими эмульгирующими свойствами и находят применение в текстильных изделиях и средствах личной гигиены. При отбеливании смесей хлопка и полиэстера в качестве отбеливателя используется NMEA.[5]
Путем метилирования N-метиламиноэтанол, диметиламиноэтанол и холин [(2-гидроксиэтил) -триметиламмонийхлорид] может быть получен.
В реакции N-метиламиноэтанол с жирными кислотами, длинноцепочечный N-метил-N- (2-гидроксиэтил) амиды образуются при удалении воды. Они используются как нейтральные поверхностно-активные вещества. Такие амиды также действуют как улучшители текучести и депрессорные присадки в тяжелые масла и средние дистилляты.[6]Каталитическим окислением N-метиламиноэтанол, непротеиногенная аминокислота саркозин получается.[7]
N-метиламиноэтанол играет роль структурный элемент для синтеза соединений для защиты растений и фармацевтических препаратов, например, на первой стадии последовательности реакции на антигистамин и антидепрессант миансерин (Толвин) и не болеутоляющим Нефопам (Аджан).[8]
По аналогии с другими азиридины, N-метилазиридин может быть получен Синтез Венкера из N-метиламиноэтанол. Это делается либо через эфир серной кислоты, либо после замены гидроксильная группа атомом хлора (например, тионилхлорид или же хлорсерная кислота[9]) к N-метил-2-хлорэтиламин, а затем с помощью сильного основания (отщепление HCl) в внутримолекулярное нуклеофильное замещение:

Он реагирует с сероуглерод давать N-метил-2-тиазолидинтион.
Смотрите также
Рекомендации
- ^ Индекс Merck, 12-е издание, 6096.
- ^ Маттиас Фрауенкрон, Иоганн-Петер Мельдер, Гюнтер Рюидер, Роланд Россбахер, Хартмут Хёке «Этаноламины и пропаноламины» в Энциклопедия промышленной химии Ульмана, 2002, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a10_001
- ^ Miura Trading & Finvest Pvt. ООО: Технология метилэтаноламинов В архиве 2016-03-06 в Wayback Machine (PDF; 152 кБ).
- ^ Оценка безопасности продукта, DOW N-метилэтаноламин, Компания Dow Chemical, Версия от 24. Март 2010 г.
- ^ Компания Dow Chemical: Алкил Алканоламины В архиве 2018-01-28 в Wayback Machine, Март 2003 г.
- ^ 30 238 США, Э. Specht, J.H. О’Мара
- ^ Патент США 8,227,638, Процесс приготовления креатина, моногидрата креатина и гуанидиноуксусной кислоты, Изобретатель: Ф. Тальхаммер, Т. Гастнер, Anmelder: Alzchem Trostberg GmbH, 24 июля 2012 г.
- ^ А. Климанн ты Дж. Энгель, Pharmazeutische Wirkstoffe: Synthese, Patente, Anwendungen, 2. überarb. ты эээ. Aufl., Georg Thieme Verlag, Штутгарт, Нью-Йорк, 1982, ISBN 3-13-558402-X.
- ^ J.H. Дрезе, Дизайн, синтез и характеристика адсорбентов аминосиликата для CO2 улавливание из разбавленных источников (PDF; 5,3 МБ), канд. Диссертация, Технологический институт Джорджии, декабрь 2010 г., С. 175.
