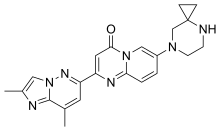
Рисдиплам - Risdiplam
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Эврисди |
| Другие имена | RG7916; RO7034067 |
| AHFS /Drugs.com | Монография |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | Устно |
| Код УВД |
|
| Легальное положение | |
| Легальное положение | |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Химические и физические данные | |
| Формула | C22ЧАС23N7О |
| Молярная масса | 401.474 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
Рисдиплам, продается под торговой маркой Эврисди, это лекарство, используемое для лечения спинальная мышечная атрофия (SMA)[2][3] и первый пероральные лекарства одобрен для лечения этого заболевания.[2][3]
Рисдиплам - это выживаемость мотонейрона 2 -направленный Модификатор сплайсинга РНК.[2][1][4]
Наиболее частые побочные эффекты включают жар, диарею, сыпь, язвы в области рта, боль в суставах (артралгию) и инфекции мочевыводящих путей.[2][1] Дополнительные побочные эффекты для младенческой популяции включают инфекцию верхних дыхательных путей, пневмонию, запор и рвоту.[2][1]
Он был одобрен США. Управление по контролю за продуктами и лекарствами (FDA) в августе 2020 года для лечения взрослых и детей в возрасте от двух месяцев и старше.[2][5] Разработано совместно с PTC Therapeutics и Фонд SMA,[3][5] он продается в США Genentech,[2] дочерняя компания Рош.[5]
Медицинское использование
В Соединенных Штатах рисдиплам показан для лечения людей в возрасте двух месяцев и старше со спинальной мышечной атрофией.[2][1]
Побочные эффекты
Наиболее частые побочные эффекты включают жар, диарею, сыпь, язвы в области рта, боль в суставах (артралгию) и инфекции мочевыводящих путей.[2][1] Дополнительные побочные эффекты для младенческой популяции включают инфекцию верхних дыхательных путей, пневмонию, запор и рвоту.[2][1]
Рисдиплам не следует принимать вместе с лекарствами, которые экструзия множественных лекарств и токсинов (MATE) субстратов, поскольку рисдиплам может повышать концентрацию этих препаратов в плазме.[2][1]
Фармакология
Механизм действия
Рисдиплам устраняет первопричину СМА: уменьшение количества двигательный нейрон выживания (SMN) белок. Белок кодируется SMN1 и SMN2 гены. SMA вызывается мутациями в SMN1 этот код для неактивных форм белка. Деятельность SMN2 Ген, который производит гораздо меньшие количества SMN, имеет тенденцию определять тяжесть заболевания.[3][6]
Соединение представляет собой пиридазин производная, изменяющая сращивание из SMN2 информационная РНК,[7][4] что приводит к увеличению концентрации функционального белка SMN до 2 раз. in vivo.[8]
Нусинерсен, первый препарат, одобренный для лечения СМА, действует аналогичным образом.[9]
Эффективность
Безопасность и эффективность риздиплама при СМА с младенческим и более поздним началом оценивалась в двух продолжающихся исследованиях. клинические испытания.[3][10][11]
В исследовании СМА с младенческим началом, открытом испытании с 41 участником, эффективность была установлена на основании способности сидеть без поддержки не менее пяти секунд. После 12 месяцев лечения 29% участников смогли самостоятельно сидеть более пяти секунд. После 23 и более месяцев лечения 81% участников остались живы без постоянной вентиляции. Хотя в исследовании не проводилось прямых сравнений с детьми, получавшими плацебо (неактивное лечение), эти результаты выгодно отличаются от типичного течения нелеченого заболевания.[10][2]
Изучение позднего СМА представляло собой рандомизированное контролируемое исследование, в котором приняли участие 180 участников в возрасте от 2 до 25 лет с менее тяжелыми формами заболевания. Участники, получавшие рисдиплам в течение 12 месяцев, показали улучшение двигательной функции по сравнению с участниками, получавшими плацебо.[11][2][3]
По состоянию на август 2020 года ведутся еще два клинических исследования.[3][5]
Общество и культура
Легальное положение
Соединенные штаты Управление по контролю за продуктами и лекарствами (FDA) предоставило компании Genentech разрешение на маркетинг 7 августа 2020 г. FDA ранее удовлетворило заявку на получение рисдиплама. быстрый трек, приоритетный обзор, и орфанный препарат обозначения.[2][3][5] Genentech также был награжден ваучер на приоритетное рассмотрение редких детских заболеваний.[2]
В Европейское агентство по лекарствам (EMA) присвоило рисдипламу звание приоритетного лекарства в 2018 году[5][12][13] и орфанный препарат обозначение в 2019 году.[14][5]
По состоянию на август 2020 г.[Обновить], Рош подала заявку на разрешение на продажу в Бразилии, Чили, Китае, Евросоюзе, Индонезии, России, Южной Корее и Тайване.[5][15]
Имена
Рисдиплам - это Международное непатентованное название (ГОСТИНИЦА).[16]
Сострадательное использование
С конца 2019 года компания Рош предлагает препарат во всем мире бесплатно для правомочных людей через расширенная программа доступа.[17]
использованная литература
- ^ а б c d е ж г час «Эврисдирисдиплам порошок для раствора». DailyMed. 18 августа 2020 г.. Получено 24 сентября 2020.
- ^ а б c d е ж г час я j k л м п о п «FDA одобряет пероральное лечение спинальной мышечной атрофии». НАС. Управление по контролю за продуктами и лекарствами (FDA) (Пресс-релиз). 7 августа 2020 г.. Получено 7 августа 2020.
 Эта статья включает текст из этого источника, который находится в всеобщее достояние.
Эта статья включает текст из этого источника, который находится в всеобщее достояние. - ^ а б c d е ж г час «Эврисди (Рисдиплам)». smanewstoday.com. 7 августа 2020 г.. Получено 8 августа 2020.
- ^ а б Чжао Х, Фэн З., Линг К.К., Моллин А., Шиди Дж., Йе С. и др. (Май 2016). «Фармакокинетика, фармакодинамика и эффективность низкомолекулярного модификатора сплайсинга SMN2 на мышиных моделях спинальной мышечной атрофии». Молекулярная генетика человека. 25 (10): 1885–99. Дои:10.1093 / hmg / ddw062. ЧВК 5062580. PMID 26931466.
- ^ а б c d е ж г час «FDA одобрило Evrysdi (рисдиплам) компании Genentech для лечения спинальной мышечной атрофии (СМА) у взрослых и детей от 2 месяцев и старше». Genentech (Пресс-релиз). 7 августа 2020 г.. Получено 7 августа 2020.
- ^ Рамдас, Ситхара; Серве, Лоран (24 января 2020 г.). «Новые методы лечения спинальной мышечной атрофии: обзор имеющихся в настоящее время данных». Мнение эксперта по фармакотерапии. Informa UK Limited. 21 (3): 307–315. Дои:10.1080/14656566.2019.1704732. ISSN 1465-6566. PMID 31973611. S2CID 210880199.
- ^ Мария Жоао Алмейда (2016-09-08). "RG7916". BioNews Services. Получено 2017-10-08.
- ^ Ратни, Хасане; Эбелинг, Мартин; Бэрд, Джон; Бендельс, Стефани; Bylund, Johan; Чен, Карен С .; Денк, Нора; Фэн, Чжихуа; Грин, Люк; Герар, Мелани; Яблонски, Филипп; Якобсен, Бьорн; Ходжа, Омар; Клецл, Хайдемари; Ко, Чиен-Пинг; Кустерманн, Стефан; Марке, Энн; Мецгер, Фридрих; Мюллер, Барбара; Нарышкин Николай А .; Паушкин, Сергей В .; Пинар, Эммануэль; Пуарье, Аньес; Рейтлингер, Майкл; Уитолл, Марла; Зеллер, Андреас; Чжао, Синь; Мюллер, Лутц (25 июля 2018 г.). «Открытие Рисдиплама, селективного выживания модификатора сплайсинга гена моторного нейрона-2 (SMN2) для лечения спинальной мышечной атрофии (СМА)». Журнал медицинской химии. Американское химическое общество (ACS). 61 (15): 6501–6517. Дои:10.1021 / acs.jmedchem.8b00741. ISSN 0022-2623. PMID 30044619.
- ^ Занетта С., Низардо М., Симоне С., Монгуцци Е., Брезолин Н., Коми Г.П. и др. (Январь 2014). «Молекулярные терапевтические стратегии для спинальных мышечных атрофий: текущие и будущие клинические испытания». Клиническая терапия. 36 (1): 128–40. Дои:10.1016 / j.clinthera.2013.11.006. PMID 24360800.
- ^ а б Baranello G, Servais L, Day J, Deconinck N, Mercuri E, Klein A и др. (Октябрь 2019 г.). «P.353FIREFISH, часть 1: безопасность и исследовательские результаты в течение 16 месяцев лечения рисдипламом (RG7916) у младенцев со спинальной мышечной атрофией 1 типа». Нервно-мышечные расстройства. 29: S184. Дои:10.1016 / j.nmd.2019.06.515. ISSN 0960-8966.
- ^ а б Mercuri E, Baranello G, Kirschner J, Servais L, Goemans N, Pera MC и др. (Апрель 2019 г.). «Обновленная информация из SUNFISH, часть 1: Безопасность, переносимость и PK / PD из исследования по подбору дозы, включая исследовательские данные по эффективности у пациентов со спинальной мышечной атрофией (СМА) 2 или 3 типа, получавших рисдиплам (RG7916) (S25.007)». Неврология. 92 (15 приложение). ISSN 0028-3878.
- ^ Инасио П. (21 декабря 2018 г.). «Рисдиплам получил премию EMA за потенциал при спинальной мышечной атрофии». Новости SMA сегодня. Получено 8 августа 2020.
- ^ «Знак PRIME, предоставленный Европейским агентством по лекарственным средствам для риздиплама компании Roche для лечения спинальной мышечной атрофии (СМА)». Рош (Пресс-релиз). 17 декабря 2018 г.. Получено 12 августа 2020.
- ^ "EU / 3/19/2145". Европейское агентство по лекарствам (EMA). 9 апреля 2019 г.. Получено 12 августа 2020.
- ^ «PTC объявляет о приеме заявки на получение европейского регистрационного удостоверения на препарат Эврисди (рисдиплам) для лечения спинальной мышечной атрофии». PTC Therapeutics, Inc. Получено 2020-08-18.
- ^ Всемирная организация здравоохранения (2018 г.). «Международные непатентованные наименования фармацевтических субстанций (МНН): рекомендованные МНН: список 80». Информация ВОЗ о лекарствах. 32 (3): 482. HDL:10665/330907.
- ^ «Рош объявляет о глобальной программе благотворительного использования рисдиплама». Спинальная мышечная атрофия Великобритания. Получено 2020-04-08.
внешние ссылки
- «Рисдиплам». Портал информации о наркотиках. Национальная медицинская библиотека США.
- Номер клинического исследования NCT02913482 для «Исследовать безопасность, переносимость, PK, PD и эффективность рисдиплама (RO7034067) у младенцев со спинальной мышечной атрофией 1 типа (FIREFISH)» при ClinicalTrials.gov
- Номер клинического исследования NCT02908685 для «Исследования по изучению безопасности, переносимости, фармакокинетики, фармакодинамики и эффективности рисдиплама (RO7034067) у участников с мышечной атрофией позвоночника 2 и 3 типа (SMA)» (SUNFISH) » ClinicalTrials.gov
