Стрептавидин - Streptavidin - Wikipedia
| Стрептавидин | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Идентификаторы | |||||||
| Организм | |||||||
| Символ | ? | ||||||
| UniProt | P22629 | ||||||
| |||||||
Стрептавидин /ˌsтрɛпˈтævɪdɪп/ 52,8 (тетрамер) кДа белок очищен от бактерия Streptomyces avidinii. Стрептавидин гомотетрамеры иметь необычайно высокую склонность к биотин (также известный как витамин B7 или витамин H). С константа диссоциации (Kd) порядка ≈10−14 Молл,[1] Связывание биотина со стрептавидином является одним из самых сильных нековалентных взаимодействий, известных в природе. Стрептавидин широко используется в молекулярной биологии и бионанотехнологии из-за устойчивости комплекса стрептавидин-биотин к органическим растворителям, денатурантам (например, гуанидин хлорид ), моющие средства (например, SDS, Тритон Х-100 ), протеолитические ферменты и экстремальные значения температуры и pH.
Структура
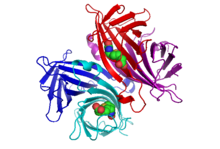
Кристаллическая структура стрептавидина со связанным биотином была описана двумя группами в 1989 году. Структура была решена с использованием много длинноволновой аномальной дифракции Hendrickson et al.[2] в Колумбийский университет и с использованием множественной изоморфной замены Weber et al.[3] в Центральном отделе исследований и разработок E. I. DuPont. По состоянию на сентябрь 2017 года на хранении находится 171 структура. Банк данных белков. Видеть эта ссылка для полного списка. N- и C-концы полноразмерного белка из 159 остатков процессируются с образованием более короткого «ядра» стрептавидина, обычно состоящего из остатков 13–139; удаление N- и C-концов необходимо для наивысшего сродства связывания биотина. Вторичная структура мономера стрептавидина состоит из восьми антипараллельных β-цепей, которые складываются, образуя антипараллельный β-ствол третичная структура. А биотин сайт связывания расположен на одном конце каждого β-цилиндра. Четыре идентичных мономера стрептавидина (т.е. четыре идентичных β-барабанчика) связываются с образованием тетрамерной четвертичной структуры стрептавидина. Сайт связывания биотина в каждом цилиндре состоит из остатков из внутренней части цилиндра вместе с консервативным Trp120 из соседней субъединицы. Таким образом, каждая субъединица вносит свой вклад в сайт связывания на соседней субъединице, и поэтому тетрамер также можно рассматривать как димер функциональных димеров.
Истоки высокой близости
Многочисленные кристаллические структуры комплекса стрептавидин-биотин пролили свет на происхождение удивительного сродства. Во-первых, существует высокая комплементарность формы связывающего кармана и биотина. Во-вторых, в сайте связывания с биотином образуется обширная сеть водородных связей. Есть восемь водородные связи непосредственно связаны с остатками в сайте связывания (так называемая «первая оболочка» водородной связи), включая остатки Asn23, Tyr43, Ser27, Ser45, Asn49, Ser88, Thr90 и Asp128. Существует также «вторая оболочка» водородных связей, включающая остатки, которые взаимодействуют с остатками первой оболочки. Однако сродство стрептавидина к биотину превышает то, которое можно было бы предсказать только на основе взаимодействий водородных связей, предполагая другой механизм, способствующий высокому сродству.[4] Карман, связывающий биотин, гидрофобный, и существует множество сила Ван дер Ваальса -опосредованные контакты и гидрофобные взаимодействия с биотином, когда он находится в кармане, что также считается причиной высокого сродства. В частности, карман выстлан консервативными остатками триптофана. Наконец, связывание биотина сопровождается стабилизацией гибкой петли, соединяющей β-цепи 3 и 4 (L3 / 4), которая закрывает связанный биотин, действуя как «крышка» над связывающим карманом и способствуя чрезвычайно медленному биотину. скорость диссоциации.
Большинство попыток мутации стрептавидина приводят к снижению аффинности связывания биотина, чего и следовало ожидать в такой высокооптимизированной системе. Однако было обнаружено, что недавно созданный мутант стрептавидина, названный траптавидином, помимо более высокой термической и механической стабильности, имеет более чем в десять раз более медленную диссоциацию биотина.[5] Это снижение скорости диссоциации сопровождалось двукратным уменьшением скорости ассоциации.
Аффинность связывания биотина может быть нарушена из-за химической маркировки стрептавидина, например, амино-реактивным флуорофоры. Флавидин представляет собой мутант стрептавидина без боковых цепей лизина, который сохраняет хорошие характеристики связывания биотина после такого мечения флуоресцентным красителем.[6]
Использование в биотехнологии
Среди наиболее распространенных применений стрептавидина - очистка или обнаружение различных биомолекул. Сильное взаимодействие стрептавидин-биотин можно использовать для прикрепления различных биомолекул друг к другу или на твердой основе. Чтобы нарушить взаимодействие стрептавидин-биотин, которое часто денатурирует очищаемый интересующий белок, необходимы суровые условия. Однако было показано, что короткая инкубация в воде при температуре выше 70 ° C обратимо нарушает взаимодействие (по крайней мере, для биотинилированной ДНК) без денатурации стрептавидина, что позволяет повторно использовать твердую подложку из стрептавидина.[7] Еще одно применение стрептавидина - очистка и обнаружение белков, генетически модифицированных Стреп-тег пептид. Стрептавидин широко используется в Вестерн-блоттинг и иммуноанализы, конъюгированные с некоторой репортерной молекулой, такой как пероксидаза хрена. Стрептавидин также использовался в развивающихся областях Нанобиотехнологии, использование биологических молекул, таких как белки или липиды, для создания наноразмер устройства / конструкции. В этом контексте стрептавидин можно использовать в качестве строительного блока для связывания биотинилированных молекул ДНК с образованием одностенных. углеродная нанотрубка строительные леса[8] или даже сложные многогранники ДНК.[9]Тетрамерный стрептавидин также использовался в качестве концентратора, вокруг которого могут быть расположены другие белки, либо с помощью аффинной метки, такой как Стреп-тег или же AviTag или путем генетического слияния SpyTag.[10] Fusion to SpyTag позволяет создавать сборки с 8 или 20 субъединицами стрептавидина. А также зонд молекулярной силы для атомно-силовая микроскопия исследования[11] новые материалы, такие как трехмерные кристаллические решетки[12] также были созданы. Стрептавидин имеет умеренно кислый изоэлектрическая точка (pI) ~ 5, но рекомбинантный форма стрептавидина с почти нейтральным pI также имеется в продаже.
- Предварительно нацеленная иммунотерапия
В предварительно направленной иммунотерапии используется стрептавидин, конъюгированный с моноклональным антителом против антигенов раковых клеток, с последующей инъекцией радиоактивно меченного биотина для доставки излучения только к раковой клетке. Первоначальные препятствия включают насыщение участков связывания биотина на стрептавидине эндогенным биотином вместо введенного радиоактивно меченного биотина и высокую степень радиоактивного воздействия на почки из-за сильных адсорбционных свойств стрептавидина. В настоящее время считается, что такой высокий уровень связывания с прикрепленными типами клеток, такими как активированные тромбоциты и меланомы, является результатом интегрин связывание опосредовано последовательностью RYD в стрептавидине.[13]
Варианты с контролируемым количеством сайтов связывания
- Моновалентные и мономерные

Стрептавидин представляет собой тетрамер, и каждая субъединица связывает биотин с равным сродством. Многовалентность является преимуществом в некоторых приложениях, например, когда эффекты авидности улучшают способность молекул, прикрепленных к стрептавидину, обнаруживать специфические Т-клетки.[14] В других случаях, таких как использование стрептавидина для визуализации определенных белков на клетках, поливалентность может нарушить функцию интересующего белка. Моновалентный стрептавидин представляет собой сконструированную рекомбинантную форму стрептавидина, которая представляет собой тетрамер, но только один из четырех сайтов связывания является функциональным. Этот единственный сайт привязки имеет 10−14 моль / л и не может вызывать сшивание.[15] Применения моновалентного стрептавидина включают флуоресцентное отслеживание рецепторы клеточной поверхности, украшения ДНК оригами, и действует как указатель для определения конкретных регионов для криоэлектронная микроскопия.
Мономерный стрептавидин представляет собой рекомбинантную форму стрептавидина с мутациями для разрушения тетрамера на мономер и повышения растворимости полученной изолированной субъединицы. Мономерные версии стрептавидина имеют сродство к биотину 10−7моль / л 10−8моль / л и поэтому не идеальны для этикетирования, но полезны для очистки, где желательна обратимость.[16][17]
- Двухвалентный

Стрептавидин с точно двумя сайтами связывания биотина на тетрамер может быть получен путем смешивания субъединиц с функциональным сайтом связывания биотина и без него и очистки с помощью ионообменная хроматография. Функциональные сайты связывания здесь обладают такой же стабильностью связывания биотина, как стрептавидин дикого типа. Двухвалентный стрептавидин с двумя сайтами связывания биотина вместе (цис-двухвалентный) или отдельно (транс-двухвалентный) может быть очищен отдельно.[18]
- Трехвалентный
Стрептавидин с точно тремя сайтами связывания биотина на тетрамер также может быть получен с использованием того же принципа, что и получение двухвалентных стрептавидинов.[19]
- Стрептавидины с высокой валентностью
Стрептавидины более высокой валентности были получены с использованием химии изопептидная связь спряжение с использованием SpyTag / SpyCatcher технологии.[20] Это включает наличие тетрамера стрептавидина с тремя сайтами связывания биотина и мертвого стрептавидина, слитого либо со SpyTag, либо со SpyCatcher. Когда разные тетрамеры смешиваются вместе, происходит ковалентная связь, позволяющая увеличить количество сайтов связывания биотина. С помощью этого метода были созданы шесть и двенадцать сайтов связывания биотина на молекулу.
Сравнение с авидином
Стрептавидин - не единственный белок, способный связываться с биотином с высоким сродством. Авидин является другим наиболее заметным биотин-связывающим белком. Первоначально выделенный из яичного желтка, авидин имеет только 30% идентичности последовательности со стрептавидином, но почти идентичен вторичной, третичной и четвертичной структуре. Авидин имеет более высокое сродство к биотину (Kd ~ 10−15M), но в отличие от стрептавидина авидин гликозилирован, положительно заряжен, обладает псевдокаталитической активностью (авидин может усиливать щелочной гидролиз сложноэфирной связи между биотином и нитрофенильной группой) и имеет более высокую склонность к агрегации. С другой стороны, стрептавидин является лучшим связывающим веществом конъюгата биотина; Авидин имеет более низкую аффинность связывания, чем стрептавидин, когда биотин конъюгирован с другой молекулой, несмотря на то, что авидин имеет более высокое сродство к свободному, неконъюгированному биотину. Поскольку в стрептавидине отсутствуют углевод модификации и имеет почти нейтральный число Пи, он имеет то преимущество, что неспецифическое связывание чем авидин. Дегликозилированный авидин (NeutrAvidin) более сопоставим с размером, pI и неспецифическим связыванием стрептавидина.
Смотрите также
Рекомендации
- ^ Грин Н.М. (1975). «Авидин». Достижения в химии белков. 29: 85–133. Дои:10.1016 / s0065-3233 (08) 60411-8. PMID 237414.
- ^ Хендриксон В.А., Пэлер А., Смит Дж. Л., Сатов Ю., Мерритт Е.А., Физакерли Р.П. (апрель 1989 г.). «Кристаллическая структура основного стрептавидина, определенная на основе многоволновой аномальной дифракции синхротронного излучения». Труды Национальной академии наук Соединенных Штатов Америки. 86 (7): 2190–4. Дои:10.1073 / pnas.86.7.2190. ЧВК 286877. PMID 2928324.
- ^ Weber PC, Ohlendorf DH, Wendoloski JJ, Salemme FR (январь 1989 г.). «Структурное происхождение связывания биотина с высоким сродством к стрептавидину». Наука. 243 (4887): 85–8. Дои:10.1126 / science.2911722. PMID 2911722.
- ^ ДеЧанси Дж., Хоук К.Н. (май 2007 г.). «Истоки связывания фемтомолярного белка с лигандом: кооперативность водородных связей и энергия десольватации в сайте связывания биотина (стрепта) авидина». Журнал Американского химического общества. 129 (17): 5419–29. Дои:10.1021 / ja066950n. ЧВК 2527462. PMID 17417839.
- ^ Чиверс К.Э., Крозат Э., Чу С., Мой В.Т., Шерратт Д.Д., Ховарт М. (май 2010 г.). «Вариант стрептавидина с более медленной диссоциацией биотина и повышенной механостабильностью». Методы природы. 7 (5): 391–3. Дои:10.1038 / nmeth.1450. ЧВК 2862113. PMID 20383133.
- ^ Jacobsen MT, Fairhead M, Fogelstrand P, Howarth M (август 2017 г.). «Аминовый ландшафт для максимизации флуоресценции белок-краситель и сверхстабильного взаимодействия белок-лиганд». Клеточная химическая биология. 24 (8): 1040–1047.e4. Дои:10.1016 / j.chembiol.2017.06.015. ЧВК 5563079. PMID 28757182.
- ^ Холмберг А., Бломстергрен А., Норд О, Лукач М., Лундеберг Дж., Улен М. (февраль 2005 г.). «Взаимодействие биотин-стрептавидин может быть обратимо нарушено с использованием воды при повышенных температурах». Электрофорез. 26 (3): 501–10. Дои:10.1002 / elps.200410070. PMID 15690449.
- ^ Остойч Г.Н., Херсам М.С. (июнь 2012 г.). «Биомолекулярно-направленная сборка самоподдерживающихся, нанопористых, проводящих и люминесцентных одностенных каркасов из углеродных нанотрубок». Маленький. 8 (12): 1840–5. Дои:10.1002 / smll.201102536. PMID 22461319.
- ^ Чжан Ц., Тиан Ц., Го Ф, Лю Цз., Цзян В., Мао Ц. (апрель 2012 г.). «ДНК-направленная трехмерная белковая организация». Angewandte Chemie. 51 (14): 3382–5. Дои:10.1002 / anie.201108710. PMID 22374892.
- ^ Fairhead M, Veggiani G, Lever M, Yan J, Mesner D, Robinson CV, Dushek O, van der Merwe PA, Howarth M (сентябрь 2014 г.). «Хабы SpyAvidin обеспечивают точную и сверхстабильную ортогональную наносборку». Журнал Американского химического общества. 136 (35): 12355–63. Дои:10.1021 / ja505584f. ЧВК 4183622. PMID 25111182.
- ^ Ким М., Ван СС, Бенедетти Ф., Маршалек ЧП (февраль 2012 г.). «Наноразмерный датчик силы для измерения межмолекулярных взаимодействий». Angewandte Chemie. 51 (8): 1903–6. Дои:10.1002 / anie.201107210. ЧВК 3279624. PMID 22253141.
- ^ Синклер Дж. К., Дэвис К. М., Веньен-Брайан С., Благородный МЭ (июль 2011 г.). «Создание белковых решеток путем слияния белков с соответствующей вращательной симметрией». Природа Нанотехнологии. 6 (9): 558–62. Дои:10.1038 / nnano.2011.122. PMID 21804552.
- ^ Алон Р., Байер Э.А., Вильчек М. (август 1992 г.). «Клеточно-адгезивные свойства стрептавидина опосредуются воздействием RGD-подобного сайта RYD». Европейский журнал клеточной биологии. 58 (2): 271–9. PMID 1425765.
- ^ Сюй XN, Screaton GR (октябрь 2002 г.). «Исследования функции Т-клеток на основе MHC / пептидных тетрамеров». Журнал иммунологических методов. 268 (1): 21–8. Дои:10.1016 / S0022-1759 (02) 00196-5. PMID 12213339.
- ^ Ховарт М., Чиннапен Д.И., Герроу К., Доррестейн П.С., Гранди М.Р., Келлехер Н.Л., Эль-Хуссейни А., Тинг А.Ю. (апрель 2006 г.). «Моновалентный стрептавидин с одним фемтомолярным сайтом связывания биотина». Методы природы. 3 (4): 267–73. Дои:10.1038 / nmeth861. ЧВК 2576293. PMID 16554831.
- ^ Ву С.К., Вонг С.Л. (июнь 2005 г.). «Разработка растворимого мономерного стрептавидина с обратимой способностью связывать биотин». Журнал биологической химии. 280 (24): 23225–31. Дои:10.1074 / jbc.M501733200. PMID 15840576.
- ^ Лим К.Х., Хуанг Х., Pralle A, Park S (октябрь 2011 г.). «Разработанный мономер и димер стрептавидина с улучшенной стабильностью и функцией». Биохимия. 50 (40): 8682–91. Дои:10.1021 / bi2010366. PMID 21892837.
- ^ Fairhead M, Krndija D, Lowe ED, Howarth M (январь 2014 г.). «Спаривание по принципу Plug-and-play через определенные двухвалентные стрептавидины». Журнал молекулярной биологии. 426 (1): 199–214. Дои:10.1016 / j.jmb.2013.09.016. ЧВК 4047826. PMID 24056174.
- ^ Дубачева, Галина В .; Арая-Каллис, Каролина; Герт Волбеда, Энн; Fairhead, Майкл; Коди, Джерун; Ховарт, Марк; Рихтер, Ральф П. (9 марта 2017 г.). «Контроль поливалентного связывания с помощью химии поверхности: модельное исследование стрептавидина». Журнал Американского химического общества. 139 (11): 4157–4167. Дои:10.1021 / jacs.7b00540. ЧВК 5364436. PMID 28234007.
- ^ Fairhead, Майкл; Веггиани, Джанлука; Рычаг, Мелисса; Ян, июнь; Меснер, Деян; Робинсон, Кэрол В .; Душек, Омер; ван дер Мерве, П. Антон; Ховарт, Марк (21 августа 2014 г.). «Концентраторы SpyAvidin обеспечивают точную и сверхстабильную ортогональную наносборку». Журнал Американского химического общества. 136 (35): 12355–12363. Дои:10.1021 / ja505584f. ЧВК 4183622. PMID 25111182.
дальнейшее чтение
- Hutchens TW, Porath JO (сентябрь 1987 г.). «Распознавание белком иммобилизованных лигандов: содействие избирательной адсорбции». Клиническая химия. 33 (9): 1502–8. PMID 3621554.
- Ходош Л.А., Буратовский С. (2001). «Очистка ДНК-связывающих белков с использованием систем сродства биотин / стрептавидин». Текущие протоколы в науке о белке. 9.7.1–9.7.13. Дои:10.1002 / 0471140864.ps0907s12. ISBN 978-0-471-14086-3.
- Циммерманн Р.М., Кокс ЕС (февраль 1994 г.). «Растяжение ДНК на функционализированных золотых поверхностях». Исследования нуклеиновых кислот. 22 (3): 492–7. Дои:10.1093 / nar / 22.3.492. ЧВК 523609. PMID 8127690.
внешняя ссылка
- Запись Swiss-Prot для предшественника стрептавидина из Streptomyces avidinii
- Стрептавидин в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Полезное взаимодействие с яйцом и яйцом Достаточно интересная статья о структуре PDB на PDBe
Группы, исследующие и разрабатывающие стрептавидин или белки семейства авидина (в алфавитном порядке)
